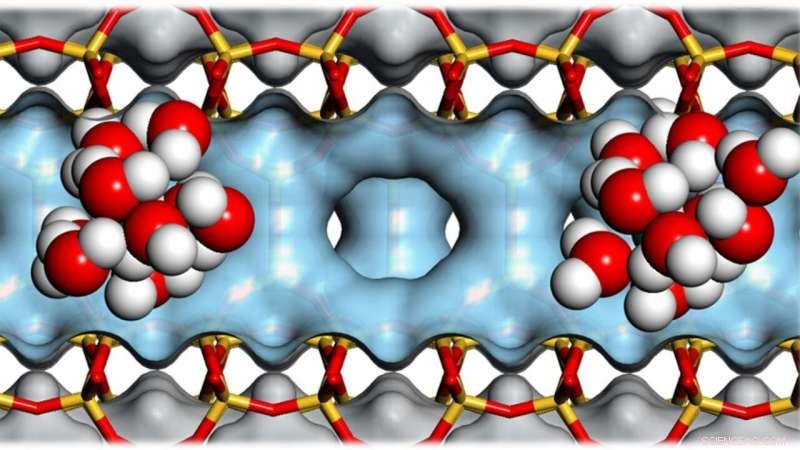
Los grupos de moléculas de agua dentro de las cavidades de las zeolitas ayudan a catalizar la conversión de biomasa en biocombustible. Crédito:Andreas Jentys / TUM
Las zeolitas son materiales extremadamente porosos:diez gramos pueden tener una superficie interna del tamaño de un campo de fútbol. Sus cavidades los hacen útiles para catalizar reacciones químicas y así ahorrar energía. Un equipo de investigación internacional ha realizado nuevos hallazgos sobre el papel de las moléculas de agua en estos procesos. Una aplicación importante es la conversión de biomasa en biocombustible.
El combustible elaborado a partir de biomasa se considera climáticamente neutro. aunque todavía se necesita energía para producirla:las reacciones químicas deseadas requieren altos niveles de temperatura y presión.
"Si queremos prescindir de las fuentes de energía fósil en el futuro y hacer un uso eficiente a gran escala de la biomasa, también tendremos que encontrar formas de reducir la energía necesaria para procesar la biomasa, "dice Johannes Lercher, profesor de Tecnología Química en la Universidad Técnica de Munich (TUM) y Director del Instituto de Catálisis Integrada en el Laboratorio Nacional del Noroeste del Pacífico en Richland, Washington (Estados Unidos).
Trabajando junto con un equipo de investigación internacional, Lercher ha examinado más de cerca el papel de las moléculas de agua en las reacciones dentro de los poros de la zeolita. que tienen menos de un nanómetro de tamaño.
Todo comienza con ácidos
Una característica de un ácido es que fácilmente dona protones. Por lo tanto, cuando se agrega al agua, el ácido clorhídrico se divide en aniones cloruro cargados negativamente, como los que se encuentran en los cristales de sal de mesa, y protones cargados positivamente que se unen a las moléculas de agua. Esto da como resultado un ion hidronio cargado positivamente, que busca transmitir más este protón, por ejemplo a una molécula orgánica.
Cuando la molécula orgánica se ve "obligada" a aceptar un protón, trata de estabilizarse. Por lo tanto, un alcohol puede dar lugar a una molécula con un doble enlace, un paso de reacción típico en el camino de la biomasa al biocombustible. Las paredes de zeolita estabilizan los estados de transición que ocurren durante la conversión y, por lo tanto, ayudar a minimizar la cantidad de energía requerida para que ocurra la reacción.

Prof. Lercher en su laboratorio del Departamento de Química de la Universidad Técnica de Munich. Crédito:Andreas Heddergott / TUM
Zeolitas que actúan como ácidos
Las zeolitas contienen átomos de oxígeno en su estructura cristalina que ya llevan un protón. Al igual que los ácidos moleculares, forman iones de hidronio a través de las interacciones con el agua.
Sin embargo, mientras que los iones de hidronio se dispersan en el agua, permanecen estrechamente asociados con la zeolita. El pretratamiento químico puede variar el número de estos centros activos y, por lo tanto, establecen una cierta densidad de iones hidronio en los poros de la zeolita.
La zeolita ideal para cada reacción
Variando sistemáticamente el tamaño de las cavidades, la densidad de los sitios activos y la cantidad de agua, el equipo de investigación pudo dilucidar los tamaños de los poros y las concentraciones de agua que catalizaron mejor las reacciones de ejemplo seleccionadas.
"En general, es posible aumentar la velocidad de reacción reduciendo los poros y aumentando la densidad de carga, "Explica Johannes Lercher." Sin embargo, este aumento tiene sus límites:cuando las cosas se llenan demasiado y las cargas están demasiado cerca unas de otras, la velocidad de reacción vuelve a bajar. Esto permite encontrar las condiciones óptimas para cada reacción ".
"Las zeolitas son generalmente adecuadas como nanoreactores para todas las reacciones químicas cuyos componentes de reacción encajan en los poros y en las que se utiliza un ácido como catalizador, "enfatiza Lercher." Estamos en el comienzo de un desarrollo con el potencial de aumentar la reactividad de las moléculas incluso a bajas temperaturas y, por lo tanto, para ahorrar cantidades considerables de energía en la producción de combustibles o productos químicos ".