-. Crédito:Tecnología de Tokio
La actual emergencia climática global y nuestros recursos energéticos en rápido retroceso hacen que la gente busque alternativas más limpias como el combustible de hidrógeno. Cuando se quema en presencia de oxígeno, El gas hidrógeno genera enormes cantidades de energía, pero ninguno de los gases de efecto invernadero nocivos. a diferencia de los combustibles fósiles. Desafortunadamente, la mayor parte del combustible de hidrógeno que se produce hoy en día proviene de gas natural o combustibles fósiles, lo que en última instancia aumenta su huella de carbono.
Amoníaco (NH 3 ), un compuesto de hidrógeno neutro en carbono, ha atraído mucha atención recientemente, debido a su alta densidad energética y alta capacidad de almacenamiento de hidrógeno. Puede descomponerse para liberar nitrógeno e hidrógeno. El amoníaco se puede licuar fácilmente, almacenado transportado, y convertido en combustible de hidrógeno cuando sea necesario. Sin embargo, la producción de hidrógeno a partir de amoniaco es una reacción lenta con demandas energéticas muy elevadas. Para acelerar la producción, a menudo se utilizan catalizadores metálicos, que también ayudan a reducir el consumo total de energía durante la producción de hidrógeno.
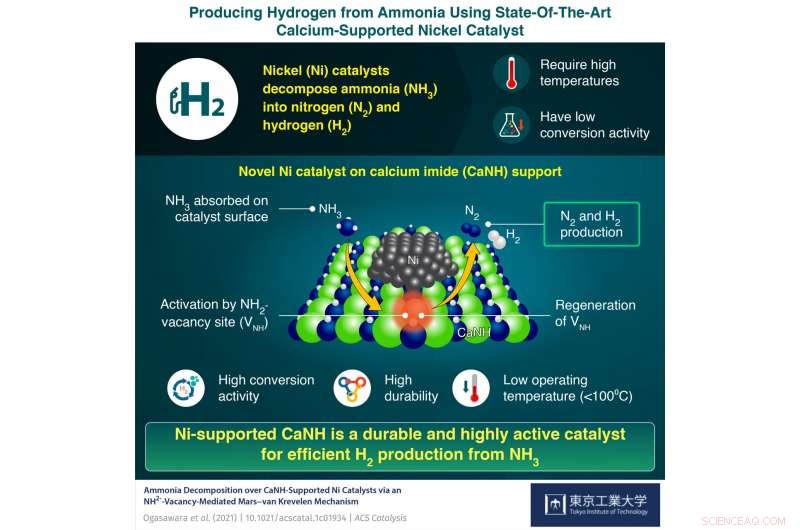
Estudios recientes han encontrado que el níquel (Ni) es un catalizador prometedor para dividir el amoníaco. El amoníaco se adsorbe en la superficie de los catalizadores de Ni, después de lo cual los enlaces entre el nitrógeno y el hidrógeno en el amoníaco se rompen y se liberan como gases individuales. Sin embargo, La obtención de una buena conversión de amoniaco utilizando un catalizador de Ni implica a menudo temperaturas de funcionamiento muy elevadas.
En un estudio reciente publicado en Catálisis ACS , un equipo de investigadores de Tokyo Tech, dirigido por el profesor asociado Masaaki Kitano, describió una solución para superar los problemas que enfrentan los catalizadores a base de Ni. Desarrollaron un catalizador de Ni con soporte de imida de calcio (CaNH) de última generación que puede lograr una buena conversión de amoníaco a temperaturas de funcionamiento más bajas. El Dr. Kitano explica:"Nuestro objetivo era desarrollar un catalizador altamente activo que fuera energéticamente eficiente. Nuestra adición de la imida metálica al sistema catalítico no solo mejoró su actividad catalítica, sino que también nos ayudó a desentrañar el elusivo mecanismo de trabajo de tales sistemas".
El equipo descubrió que la presencia de CaNH resultó en la formación de NH 2- vacantes (V NUEVA HAMPSHIRE ) en la superficie del catalizador. Estas especies activas dieron como resultado un rendimiento catalítico mejorado del Ni / CaNH a temperaturas de reacción que eran 100 ° C más bajas que las necesarias para el funcionamiento de los catalizadores basados en Ni. Los investigadores también desarrollaron modelos computacionales y realizaron el etiquetado de isótopos para comprender lo que estaba sucediendo en la superficie del catalizador. Los cálculos propusieron un mecanismo de Mars-van Krevelen que implicaba la adsorción de amoníaco en la superficie de CaNH, su activación en el NH 2- lugares vacantes, formación de nitrógeno e hidrógeno gaseoso, y finalmente la regeneración de lugares vacantes promovida por nanopartículas de Ni.
El catalizador de Ni / CaNH altamente activo y duradero se puede implementar con éxito para la generación de gas hidrógeno a partir de amoníaco. También, La comprensión del mecanismo de catálisis proporcionada por este estudio se puede utilizar para desarrollar una nueva generación de catalizadores. "Dado que todo el mundo trabaja en conjunto para construir un futuro sostenible, Nuestra investigación tiene como objetivo resolver los contratiempos que enfrentamos en nuestro camino hacia una economía de combustible de hidrógeno más limpia, "concluye el Dr. Kitano.
Este es un rayo de esperanza para la misión mundial de bajas emisiones de carbono.