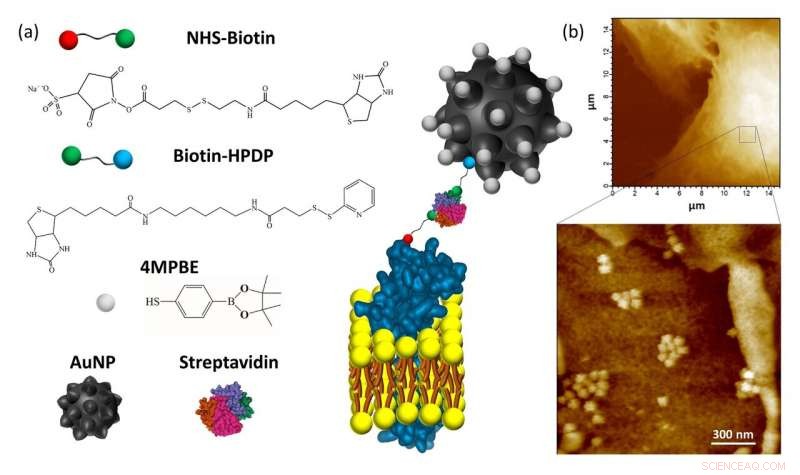
Figura 1:(a) Esquema explicativo del nanosensor anclado a la membrana plasmática. Los compuestos utilizados para la conjugación de nanopartículas de oro (AuNP) son el éster de pinacol 4-mercaptofenilborónico sensible al H2O2 (4MPBE) y la biotina-HPDP. La biotinilación de los ectodominios de la proteína de la membrana plasmática se obtiene usando NHS-Biotina. El anclaje de la AuNP conjugada y la NHS-Biotina viene dada por la estreptavidina que reacciona con los dos restos de biotina. (b) El análisis de AFM se realizó en células de cáncer de pulmón A549 después del anclaje y la fijación del nanosensor. Las imágenes AFM de alta resolución confirmaron la presencia del nanosensor, que está en contacto con la superficie celular y es capaz de detectar H2O2 endógeno en una región muy poco profunda (es decir, 90 nm) del líquido extracelular en contacto con la membrana plasmática. Crédito:Universidad de Kanazawa
Investigadores de la Universidad de Kanazawa informan en Biosensores y bioelectrónica una prueba exitosa de un sensor para medir las concentraciones de peróxido de hidrógeno cerca de las membranas celulares. El sensor tiene el potencial de convertirse en una herramienta para nuevas terapias contra el cáncer.
Varios procesos en el cuerpo humano están regulados por reacciones bioquímicas que involucran peróxido de hidrógeno (H 2 O 2 ). Aunque puede actuar como un 'mensajero secundario, "retransmitir o amplificar determinadas señales entre células, H 2 O 2 es generalmente tóxico debido a su carácter oxidante. Esto último significa que convierte (oxida) moléculas bioquímicas como proteínas y ADN. La propiedad oxidante de H 2 O 2 es de posible relevancia terapéutica para el cáncer, sin embargo:causar deliberadamente que las células tumorales aumenten su H 2 O 2 la concentración sería una forma de destruirlos. A la luz de esta, sino también para el seguimiento de patologías asociadas a H 2 O 2 superproducción, es fundamental disponer de un medio para cuantificar de forma fiable las concentraciones de peróxido de hidrógeno en el entorno extracelular. Ahora, Leonardo Puppulin del Nano Life Science Institute (WPI-NanoLSI), La Universidad de Kanazawa y sus colegas han desarrollado un sensor para medir las concentraciones de H 2 O 2 en las proximidades de las membranas celulares, con resolución nanométrica.
El biosensor consta de una nanopartícula de oro con moléculas orgánicas adheridas. Todo el grupo está diseñado para que se ancle fácilmente al exterior de la membrana de una célula, que es exactamente donde están las moléculas de peróxido de hidrógeno a detectar. Como moléculas de unión, los científicos utilizaron un compuesto llamado 4MPBE, se sabe que tiene una fuerte respuesta de dispersión Raman:cuando se irradia con un láser, las moléculas consumen parte de la energía de la luz láser. Midiendo el cambio de frecuencia de la luz láser, y trazar la intensidad de la señal en función de este cambio, Se obtiene un espectro único:una firma de las moléculas de 4MPBE. Cuando una molécula de 4MPBE reacciona con una H 2 O 2 molécula, su espectro Raman cambia. Basado en este principio, comparando espectros Raman, Puppulin y sus colegas pudieron obtener una estimación de la H 2 O 2 concentración cerca del biosensor.
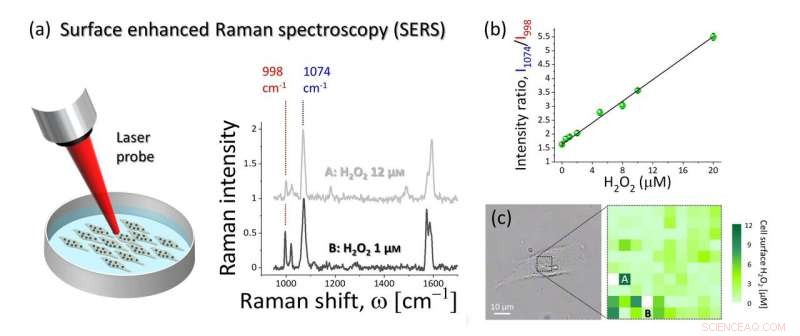
Figura 2:(a) Se usó espectroscopía Raman mejorada de superficie para detectar y cuantificar la modificación inducida por H2O2 de moléculas de 4MPBE ensambladas en la superficie de oro del nanosensor anclado a las células. La intensidad de la banda Raman a 998 cm-1 depende de la concentración de H2O2, mientras que la banda a 1074 cm-1 no mostró modificación y se puede utilizar para la normalización de las líneas espectrales. (b) Resultados de la calibración del nanosensor. La relación de la intensidad a 1074 cm-1 a la intensidad a 998 cm-1 mostró una dependencia lineal con respecto a la concentración de H2O2. (C) Ejemplo de mapa hiperespectral SERS de H2O2 endógeno extracelular recogido de la superficie de la célula A549 que se muestra en la imagen de campo claro. Los espectros SERS que se muestran en (a) se obtuvieron de las ubicaciones A y B. Crédito:Universidad de Kanazawa
Después de desarrollar un procedimiento de calibración para su nanosensor, relacionando el H 2 O 2 concentración a un cambio en el espectro Raman de una manera cuantitativa no es sencillo:los científicos pudieron producir un mapa de concentración con una resolución de aproximadamente 700 nm para muestras de células de cáncer de pulmón. Finalmente, también lograron extender su técnica para obtener medidas de la H 2 O 2 variación de la concentración a través de las membranas celulares.
Puppulin y sus colegas concluyen que su "enfoque novedoso puede ser útil para el estudio de H real 2 O 2 concentraciones implicadas en la proliferación o muerte celular, fundamentales para dilucidar por completo los procesos fisiológicos y diseñar nuevas estrategias terapéuticas ".
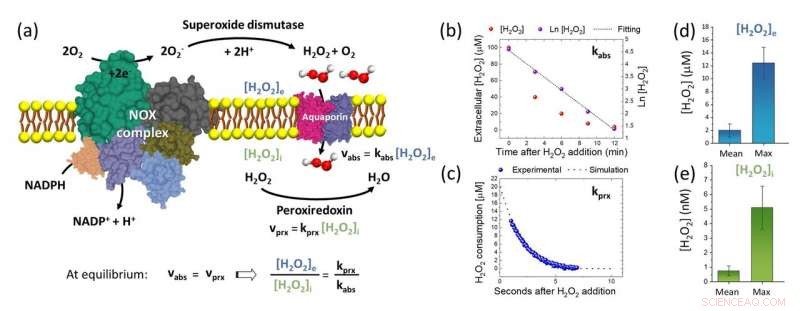
Figura 3:(a) Esquema explicativo de la producción extracelular de H2O2 por el complejo NOX, la consiguiente absorción a través del canal de acuaporina y la reacción con peroxiredoxina intracelular. En condición de estado estacionario, la relación de concentración de H2O2 extracelular a H2O2 intracelular se puede estimar mediante la relación entre la constante de velocidad de reducción de H2O2 por peroxiredoxina (kprx) y la constante de velocidad de absorción de H2O2 a través de la membrana plasmática (kabs). (b) - (c) Resultados típicos de experimentos de biología redox con líneas de ajuste a partir de las cuales medimos kabs y kprx, respectivamente. (d) [H2O2] e extracelular de superficie media y el máximo típico de [H2O2] e medido en células A549 utilizando el nanosensor de nuevo diseño. (e) [H2O2] i intracelular media y el máximo típico de [H2O2] i estimados en células A549 de acuerdo con el modelo informado en (a) y utilizando los resultados de (b) - (d). Crédito:Universidad de Kanazawa
El biosensor desarrollado por Leonardo Puppulin de la Universidad de Kanazawa y sus colegas se basa en un método llamado espectroscopía Raman mejorada en superficie (SERS). El principio se deriva de la espectroscopia Raman, en el que se analizan las diferencias entre las frecuencias de entrada y salida de la luz láser irradiada sobre una muestra. El espectro obtenido al graficar la fuerza de la señal en función de la diferencia de frecuencia es característico de la muestra, que en principio puede ser una sola molécula. Típicamente, sin embargo, la señal proveniente de una molécula es demasiado débil para detectarla, pero el efecto puede mejorarse cuando la molécula se absorbe en una superficie metálica rugosa. Puppulin y sus colegas aplicaron la técnica para detectar (indirectamente) el peróxido de hidrógeno; su molécula que responde a Raman es un compuesto llamado 4MPBE, que se modifica cuando se expone al peróxido de hidrógeno.