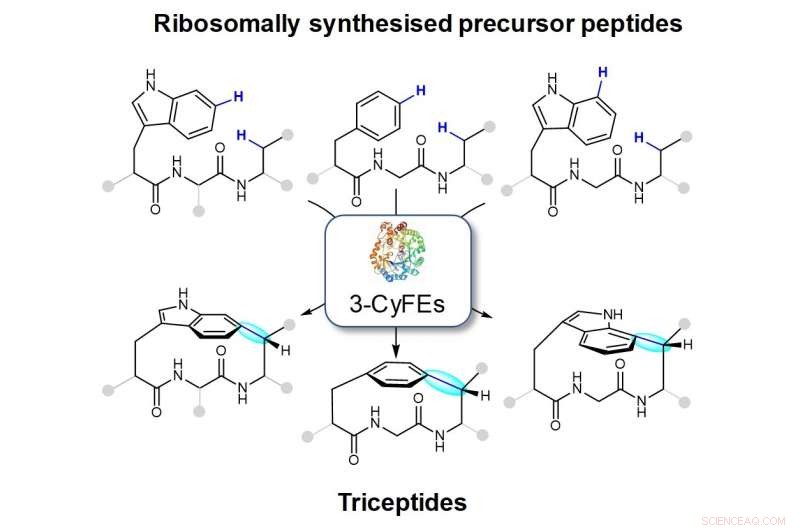
La Figura muestra macrociclos que son creados por las enzimas formadoras de ciclofano de tres residuos (3-CyFE). El nuevo enlace se muestra en azul y resaltado en cian. La familia de productos naturales que son producidos por 3-CyFE se conoce como triceptidos.
Los investigadores de NUS han identificado enzimas modificadoras postraduccionales en bacterias que pueden crear una nueva familia de péptidos cíclicos para nuevas terapias.
Los péptidos cíclicos son una clase bien conocida de moléculas que poseen una gama de actividades biológicas que incluyen antibacterianas, propiedades inmunosupresoras y anticancerígenas. El desafío de crear nuevos tipos de péptidos cíclicos radica en el descubrimiento de nuevas reacciones catalíticas mediante síntesis química o mediante el uso de enzimas. Una estrategia para lograr esto implica la formación de enlaces carbono-carbono (C-C). Sin embargo, Las reacciones de formación de enlaces C-C en enlaces carbono-hidrógeno (C-H) no activados son difíciles porque estas posiciones son inertes, y la selectividad no es fácil de controlar. Superar estas barreras permitirá la creación de una nueva gama de péptidos cíclicos de una manera eficiente y predecible.
El equipo de investigación dirigido por el profesor Brandon Morinaka del Departamento de Farmacia, NUS ha encontrado reacciones catalizadas por un conjunto de enzimas modificadoras postraduccionales de varias bacterias que potencialmente pueden usarse para desarrollar importantes moléculas de fármacos. Estas enzimas pueden catalizar la formación de un C (aril) -C ( sp 3 ) enlazan entre las cadenas laterales de dos aminoácidos. Esta disposición molecular es la característica definitoria de una clase de productos naturales denominados triceptidos (tres residuos en péptidos de ciclofano) (ver figura). La reacción de cierre del anillo da como resultado la formación de ciclofanos peptídicos tensos. Aunque estas enzimas están codificadas en varios cientos de genomas bacterianos, su función y sus productos finales han permanecido en gran parte desconocidos.
Estas enzimas ofrecen una nueva estrategia para la modificación de péptidos y se pueden aplicar para generar péptidos terapéuticos que muestran una unión única a dianas moleculares. La ciclación de péptidos es una estrategia general utilizada en la naturaleza y la química sintética para prevenir la degradación por las enzimas digestivas. La prevención de la degradación es un atributo esencial necesario para que los fármacos alcancen su objetivo y representa un obstáculo para el uso de péptidos como fármacos.
Estas enzimas pueden instalar los anillos en una variedad de patrones con diferentes aminoácidos. Esto significa que la variedad de productos es potencialmente grande y se puede aplicar a diversos objetivos en el descubrimiento de fármacos. Se encontró que diversas bacterias de una variedad de microbiomas codifican las enzimas formadoras de ciclofano. La diversidad de productos sugiere que los ciclofanos peptídicos son más frecuentes de lo que se conocía anteriormente y pueden conferir un uso o función general entre esta clase de productos naturales.
El equipo planea producir productos naturales de triceptidos adicionales y comprender el mecanismo de la enzima. Sus objetivos a largo plazo son generar una amplia gama de productos peptídicos de ciclofano que se pueden utilizar como punto de partida para atacar enfermedades de interés.
El profesor Morinaka dijo:"Las enzimas formadoras de ciclofano postraduccionales ofrecen un nuevo método para crear diversos péptidos cíclicos que brindan nuevas oportunidades en la ingeniería de péptidos y el descubrimiento de fármacos".