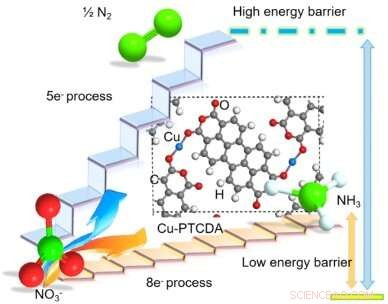
Estructura propuesta de PTCDA con Cu incorporado y diagrama esquemático que ilustra su ventaja de reducir selectivamente NO3− en NH3 a través de la transferencia directa de 8 eletrones. Rojo, blanco, gris, azul brillante, y esferas verdes representan la O, H C, Cu, y N átomos, respectivamente. Crédito:Chen et al.
Amoníaco (NH 3 ) es un incoloro, compuesto gaseoso y soluble en agua utilizado en varios sectores, incluida la agricultura, el sector energético, y una variedad de industrias. Por mas de un siglo, la principal forma de producir grandes cantidades de amoníaco ha sido a través del proceso Haber-Bosch, lo que implica el uso de alta presión para producir una reacción química que permite la síntesis directa de amoníaco a partir de hidrógeno y nitrógeno.
Mientras que el proceso Haber-Bosch permite la producción masiva de amoníaco, se sabe que es dañino tanto para los seres humanos como para el medio ambiente, ya que implica el consumo de combustibles fósiles y por tanto agrava el efecto invernadero. Debido a estos efectos indeseables, Los investigadores han buscado métodos alternativos para producir amoníaco a través de N 2 −H 2 O reacciones químicas en condiciones ambientales, algunos de los cuales utilizan fuentes de energía renovables.
Se ha descubierto que algunas de estas nuevas técnicas para la producción de amoniaco son eficaces y relativamente económicas. Sin embargo, por lo general, solo permitían a los investigadores producir cantidades limitadas de amoníaco y exhibían una selectividad pobre, debido al enlace N≡N inerte y la solubilidad ultrabaja de N 2 en agua.
Investigadores de la Universidad Tecnológica del Sur de China y el Laboratorio Nacional Argonne han ideado recientemente una nueva estrategia electroquímica para producir amoníaco mediante la reducción de nitratos. Su método, introducido en un artículo publicado en Energía de la naturaleza , se basa en el uso de un catalizador sólido molecular de cobre.
"Obtención de NH 3 directamente de no-N 2 fuentes se considera una estrategia revolucionaria para abordar las preocupaciones asociadas con los procesos de producción de amoníaco anteriores, "Haihui Wang, uno de los investigadores que realizó el estudio, dijo Phys.org. "En la búsqueda de alternativas que contengan nitrógeno distintas del N 2 para sintetizar NH 3 , el anión nitrato (NO 3 - ) se destaca por el hecho de que la menor energía de disociación del enlace N =O (204 kJ mol -1 ) en comparación con el triple enlace N-N (941 kJ mol -1 ), y el enriquecimiento de NO 3 - en los recursos hídricos causó contaminación ambiental y amenaza la salud humana ".
Conversión selectiva de NO 3 - a NH 3 en condiciones ambientales y en una H 2 El sistema basado en O podría ser una alternativa más ecológica para la producción masiva de NH 3 . Esta conversión alternativa aliviaría los problemas ambientales asociados con los métodos actuales para producir amoníaco a gran escala. al mismo tiempo que disminuye el consumo de energía.
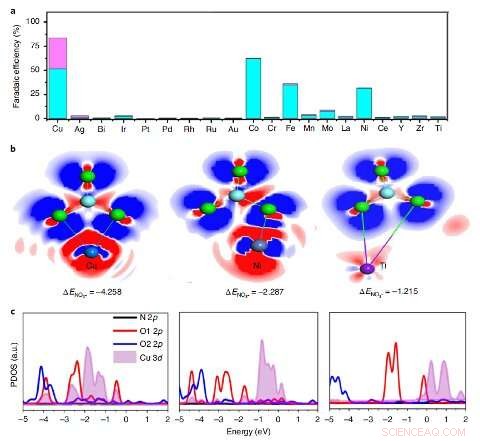
Proyección del elemento de mayor actividad. a, La eficiencia faradaica de NH3 (azul) y NO2− (malva) de varios elementos incorporados en PTCDA bajo un potencial de −0,4 V frente a RHE. B, El EDD de NO3– en 1Cu – PTCDA (¬103) (izquierda), 1Ni – PTCDA (¬103) (centro) y 1Ti – PTCDA (¬103) (derecha). Azul, azul oscuro, púrpura, esferas azul cielo y verde representan el Cu, Ni, Ti, Átomos de N y O, respectivamente. La nube electrónica azul indica acumulación de carga y la nube electrónica roja indica agotamiento de carga. C, La densidad proyectada de estados (PDOS) de * NO3 en 1Cu – PTCDA (¬103) (izquierda), 1Ni – PTCDA (¬103) (centro) y 1Ti – PTCDA (¬103) (derecha). Crédito:Chen et al.
"Conversión NO 3 - en NH 3 está lejos de ser una tarea fácil, ya que requiere una reacción de transferencia de ocho electrones, así como un potencial de reacción ligeramente menor (es decir, 1.20 V versus el electrodo de hidrógeno reversible o RHE) que el de la conversión de cinco electrones de NO 3 - a N 2 (1,25 V frente a RHE), "Wang explicó." Varios sistemas electrocatalíticos con diferentes catalizadores heterogéneos (como Cu, Ag, Au, y así sucesivamente) se han propuesto en el pasado, pero la mayoría de ellos tienden a producir N 2 mediante la reducción de cinco electrones de NO 3 - en lugar de la reducción deseada de ocho electrones ".
El potencial práctico de convertir NO 3 - a NH 3 está por debajo de lo que se conoce como potencial de reacción de desprendimiento de hidrógeno (HER), que conduce a la generación de H 2 . Esto puede reducir la eficiencia general de la producción de NH 3 .
En su estudio, Wang y sus colegas pudieron lograr la reducción directa de ocho electrones de NO 3 - a NH 3, catalizado por 3 cristalino incorporado en Cu, 4, 9, Dianhídrido 10-perilentetracarboxílico (PTCDA) con una forma de barrera de baja energía. El catalizador que utilizaron exhibió una alta tasa de rendimiento y una selectividad sobresaliente, suprimiéndola eficazmente.
"Seleccionamos catalizadores con la preparación de una serie de metales incorporados en PTCDA, como Cu, Ag, Au, Ru Rh, Ir, Pd, Pt, Bi, Ti, Cr Minnesota, Fe, Co, Ni, Y, Zr, Mes, La y Ce, "Explicó Wang." Descubrimos que el alto rendimiento de nuestro catalizador se puede atribuir a la configuración electrónica única de Cu 3 D orbital que muestra una mayor superposición con el nitrato O 2 pag orbitales para mejorar la transferencia de carga, así como la estructura de PTCDA, que ayuda a regular la transferencia de protones y electrones a los centros activos de Cu y luego a inhibir HER y promover la unión de H-N ".
El método electroquímico introducido por Wang y sus colegas podría abordar los desafíos actualmente asociados con el NH en masa 3 producción. En las pruebas iniciales, este método logró eficiencias faradaicas entre 60% y 86% y NH 3 tasas de producción entre aproximadamente 400 y 900 μg h –1 cm –2 a potenciales aplicados de −0,4 a −0,6 V frente a RHE.
Los resultados son significativamente mejores que los obtenidos con otros métodos para la reducción electroquímica de N 2 a NH 3 . Por ejemplo, métodos mediados por litio, que son los más conocidos por lograr tasas de rendimiento relativamente altas en la electrorreducción de N 2 -to-NH 3 , achieved a production rate of less than 36 μg h -1 cm.
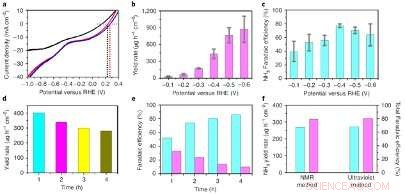
Electrocatalytic performances of O-Cu–PTCDA. a, Linear sweep voltammetry curves of O-Cu–PTCDA tested in 0.1 M PBS (black), 0.1 M PBS thatcontained NO2− (red) and 0.1 M PBS that contained NO3− (blue). B, NH3 yield rate at different potentials at the second hour. C, NH3 Faradaic efficiency at different potentials at the second hour. d, NH3 yield rate at different times at −0.4 V versus RHE up to 4 h. mi, NH3 (blue) and NO2− (mauve) Faradaic efficiencies at different times at −0.4 V versus RHE up to 4 h. F, The overall NH3 yield rate (blue) and total Faradaic efficiency (mauve) detected by 1H NMR spectroscopy and an indophenol blue method after the 4-h experiment. Credit:Chen et al.
The recent study by Wang and his colleagues also opens up new possibilities for the recycling of nitrogen (NO 3 - ) in wastewater. For several years, NO 3 - was considered to be a toxic water contaminant and was usually transferred into gaseous nitrogen and returned to the air. Recent studies, sin embargo, suggest that the high amount of nitrogen in wastewater could in fact be recycled for fertilization.
"The total nitrogen discharged into the water per year is 14.5 ± 3.1 million tons in China, which is about 50% of the annual consumption of synthetic nitrogen (300.5 million tons in 2016), " Wang said. "In 2016, the United States planted 94 million acres of corn, using about 8.9 billion kilograms of nitrogen annually, which accounts for 40% of the annual nitrogen use in the United States. Sin embargo, it is worth noting that 2.4 billion kilograms of nitrogen is available in wastewater each year. The statistics prove that nitrogen in wastewaters could be a valuable resource."
In addition to allowing the large-scale production of ammonia in ways that are more environmentally friendly, the recent work by Wang and his colleagues could pave the way toward the development of wastewater management systems with nitrogen conversion capabilities. These systems would enable the recycling of large quantities of nitrogen, ultimately optimizing the use of global resources and protecting the environment.
While the results are promising, the researchers still need to overcome two technical challenges before their method can be applied in real-world settings. These challenges will be the main focus of their next set of studies.
"Por un lado, our future studies will be aimed at enhancing the catalyst's structure to further improve its long-term stability, " Wang said. "In this work, the NH 3 yield rate decreased from 337.8 μg h -1 cm -2 to 140.3 μg h -1 cm -2 after 15 hours, after which it was substantially stable and maintained an NH 3 yield rate of 130.8 μg h -1 cm -2 after 40 hours. Por otra parte, we will work on the large-scale application of NH 3 electrosynthesis, developing an electric-driving flow device for the direct and continuous mass production of high-purity liquid ammonia or ammonium salt. We plan to devise a simple method for the direct purification and collection of the products, which removes the need for additional purification, transportation and other procedures."
© 2020 Science X Network