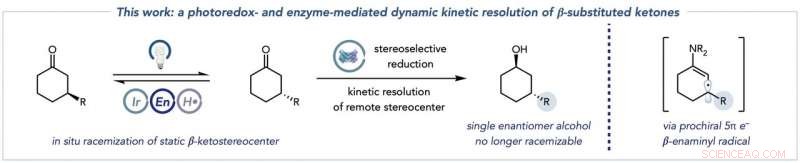
La transformación general que combina la racemización de los sustratos de cetonas (izquierda) con la reducción biocatalítica a productos alcohólicos enantioméricamente puros (centro), y las especies de radicales enaminilo clave que esta química desbloquea para permitir la racemización de β-cetoestereocentros típicamente estáticos (derecha). Crédito:Jacob DeHovitz
Una colaboración entre dos laboratorios del Departamento de Química de la Universidad de Princeton ha producido una nueva plataforma sorprendente que permite a los químicos reinterpretar las reglas de la estereoquímica y el estereocontrol con importantes implicaciones para las industrias farmacéutica y agroquímica.
La investigación demuestra la capacidad de la catálisis fotoredox para tomar estereocentros tradicionalmente estáticos y hacerlos dinámicos rompiendo y reformando de forma continua y controlada enlaces moleculares. Es prometedor para los científicos establecer los estereocentros de un compuesto objetivo complejo en un resumen, paso eficiente en lugar de un estereocentro a la vez. (Un estereocentro da una asimetría de imagen especular de una molécula, que es importante para determinar las propiedades biológicamente activas durante la síntesis).
La colaboración combina la experiencia del laboratorio MacMillan y el laboratorio Hyster. El papel, "Estéreocontrol estático a indudablemente dinámico:el uso convergente de cetonas sustituidas en β racémicas, " aparece en Ciencias esta semana.
"Normalmente, cuando estás pensando en construir moléculas con estereocentros en ellas, piensa en configurar el estereocentro en el evento de formación de enlace, "dijo Todd Hyster, profesor asistente de química. "Y lo que hemos descubierto es que si utiliza la catálisis fotorredox, Básicamente, puedes desbloquear mecanismos para crear estereocentros que de otro modo serían estáticos, o fijo. Puede convertirlos en dinámicos.
"Cuando se combinan con enzimas altamente selectivas, puedes pensar en construir moléculas estereoquímicamente complejas de formas completamente nuevas ".
La estereoquímica implica la disposición espacial de los átomos y cómo se pueden manipular en la estructura molecular para obtener los resultados deseados. Se deriva del hecho de que el carbono tiene cuatro sustituyentes. Esos cuatro sustituyentes son diferentes; tienen que existir como imágenes especulares entre sí. Estas imágenes especulares se denominan enantiómeros. Nuestras manos son enantiómeros, por ejemplo; son imágenes especulares el uno del otro. Lo que eso significa en la práctica es que no se pueden superponer:un guante de la mano izquierda no cabe en la mano derecha.
El cuerpo humano responde a los medicamentos exactamente de la misma manera. Nuestra materia biológica está formada por una serie de imágenes especulares y no por la otra. El cuerpo puede reconocer la diferencia entre dos medicamentos que parecen idénticos aunque uno sea una imagen especular y el otro no. Ese reconocimiento influye en la aceptación y, por tanto, en la eficacia de las terapias.
Lo que la investigación de MacMillan y Hyster descubrió es una forma de desacoplar la configuración del estereocentro del paso en el que se forma, o racemizado. Poder controlar esta racemización es importante para el desarrollo de los medicamentos más eficaces.
"Hay muchos, muchas razones por las que se trata de una investigación apasionante, no menos importante es que básicamente puedes hacer una molécula y puedes decir, tal vez realmente me gustaría cambiar ese estereocentro para convertirlo en otra cosa. De hecho, puedes volver atrás y hacer eso, "dijo David MacMillan, el Profesor Distinguido de Química de la Universidad James S. McDonnell. "Esto es algo que no creemos que realmente se haya hecho de esta manera antes en química orgánica y, por lo tanto, abre algunas oportunidades notables".
Las enzimas mejoran los resultados
Fue la introducción de enzimas altamente selectivas en el proceso lo que impulsó los avances de la investigación de la investigación "B + a A +", Dijo MacMillan.
"Las enzimas tienen esta forma de poder impartir lo que se llama estereocontrol, o introduciendo formas muy específicas para hacer química que los catalizadores ordinarios simplemente no pueden hacer, ", dijo." Al unir estas dos ideas, permite un enfoque completamente nuevo sobre cómo se construye la estereoquímica ".
Están sucediendo muchas cosas bajo el capó en este proceso. Cuando los científicos sintetizan un compuesto con varios estereocentros, suponen que el centro no puede voltear o volverse dinámico una vez que está "establecido". Las moléculas se sintetizan secuencialmente:se forma un centro, y luego está bloqueado; y luego se forma otro, y luego está bloqueado, etcétera.
Jacob DeHovitz, estudiante de quinto año en el laboratorio de Hyster y autor principal del artículo, explicó cómo la reacción descrita en esta investigación permite a los científicos desbloquear ese escenario.
Hay dos partes importantes de la reacción. En la primera mitad, dos especies clave se forman a partir de un material de partida cetona. La primera especie se llama enamina, clave porque puede ser el objetivo del catalizador fotorredox. Una segunda especie, un radical enaminilo, resulta de ese paso, y destruye el estereocentro molecular original y establece el siguiente paso en el proceso.
"La segunda mitad es la reacción biocatalítica. La enzima en solución, en este caso, principalmente cetoreductasas:reduce uno de esos enantiómeros de cetona, que de nuevo están constantemente racemizando en solución, para formar un producto alcohólico que no pueda sufrir racemización en nuestras condiciones. Críticamente, el otro enantiómero de cetona no reacciona con la cetoreductasa porque no puede encajar en el sitio activo de la enzima. Este sesgo para un enantiómero es importante porque evita que la cetoreductasa se forme indeseablemente otros estereoisómeros de alcohol.
"Si la reacción biocatalítica se combina con las nuevas condiciones de racemización en las que los enantiómeros del material de partida se racemizan constantemente, entonces, teóricamente, un químico puede permitirse hasta el 100% del producto deseado, duplicando la eficiencia, "Dijo DeHovitz.
Esta investigación representa tres años de investigación colaborativa de los dos laboratorios.