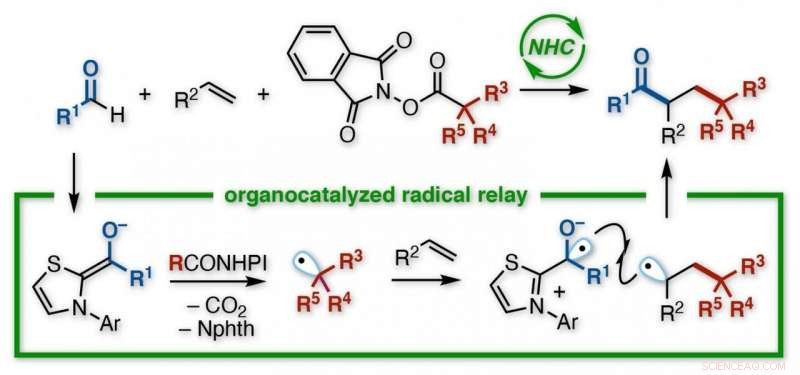
Un equipo de investigación japonés de la Universidad de Kanazawa desarrolló una reacción para crear cetonas funcionalizadas. Usando un organocatalizador de carbeno N-heterocíclico (NHC), sin necesidad de metales o irradiación de luz, se añaden un grupo acilo y un grupo alquilo a través del doble enlace de un alqueno. El NHC proporciona un control regioselectivo sobre un proceso de relevo que implica la transferencia de electrones seguida de la adición sucesiva de dos radicales al alqueno. Los diversos productos son bloques de construcción útiles para futuras síntesis. Crédito:Universidad de Kanazawa
Los químicos orgánicos son arquitectos moleculares, diseñando estructuras sofisticadas. A medida que las moléculas utilizadas en la ciencia y la medicina se vuelven cada vez más complejas, se necesitan nuevas herramientas para reconstruir los bloques de construcción. Ahora, un equipo japonés de la Universidad de Kanazawa ha desarrollado una reacción que une tres componentes a la vez utilizando la química de los radicales libres.
Dobles enlaces carbono-carbono, conocidos como alquenos, son más reactivos que los enlaces simples. Esto los hace útiles para conectar diferentes grupos:si el doble enlace está roto, se pueden agregar dos nuevas moléculas en cada extremo, unidos por el antiguo alqueno ahora unificado.
El equipo de Kanazawa buscó formas de lograr esta transformación utilizando aldehídos, que contienen un doble enlace entre oxígeno y carbono, como una de las dos moléculas injertadas en un alqueno. Como se informó en el Revista de la Sociedad Química Estadounidense , el objetivo era crear cetonas altamente funcionalizadas, una importante familia de compuestos en síntesis orgánica.
Su método elegido fue una reacción conocida, bastante evocativamente, como relevo radical. Que contiene un electrón desapareado, y así un orbital medio vacío, los radicales (o radicales libres) tienden a ser vorazmente reactivos. Tan reactivo Por supuesto, que no se pueden almacenar, pero debe generarse in situ extrayendo un electrón de algún lugar durante una reacción, provocando una cascada de ruptura de vínculos y creación.
Los químicos pueden producir radicales de varias formas, pero el equipo de Kanazawa quería probar un catalizador de orágano, denominado carbeno N-heterocíclico (NHC). Con un aldehído como reactivo, y un éster redox funcionalizado como el otro, el NHC desencadenó su transformación en radicales. Estudios anteriores insinuaron que ambos radicales reaccionarían más rápido con un alqueno que entre sí.
"El desafío con los radicales es que, siendo tan inestable, a menudo reaccionan consigo mismos, ", dice el coautor del estudio, Kazunori Nagao." Luego, recuperas tus materiales de partida, o un subproducto, en lugar del objetivo. Minimizamos esto aquí. De hecho, la reacción procedió como un relevo:primero el radical alquilo agregado a un carbono del alqueno, y luego el radical acilo añadido al otro ".
El compuesto resultante tenía una cetona y un grupo derivado de éster unido a dos carbonos adyacentes, en un llamado arreglo vecinal. Aunque también ocurrió una reacción directa entre los diferentes radicales, dando un producto de dos componentes no deseado, en lugar del objetivo de tres componentes con puentes de alqueno, era menor. Es más, una amplia gama de materiales de partida eran compatibles con el proceso.
"Vale la pena mencionar dos puntos cruciales, "dice Hirohisa Ohmiya, autor correspondiente del estudio. "Primero, a diferencia de algunas reacciones, el nuestro está libre de catalizadores metálicos y no necesita una fuente de luz para producir radicales, haciéndolo ecológico y versátil. Segundo, el NHC controla con precisión el relé, para que podamos ser selectivos en las posiciones de los grupos funcionales. Ahora estamos trabajando en una versión asimétrica para productos quirales ".