
Instantáneas de una simulación que revelan el mecanismo por el cual la helicasa del virus de la hepatitis C rompe las hebras dobles de ADN. Los dos dominios motores caminan a lo largo de la hebra superior empleando el mecanismo de translocación del gusano de pulgada. Los terceros dominios actúan como una cuña que separa mecánicamente el dúplex (de la Fig. 14). Crédito:Universidad de Kanazawa
La célula viva puede verse como una fábrica donde las máquinas de proteínas se encargan de varios procesos, como el transporte de material dentro de la célula u operaciones con otras macromoléculas como el ADN. Su funcionamiento suele estar impulsado por moléculas de ATP, el principal portador de energía en las células biológicas. La energía química obtenida a través de la hidrólisis de ATP es utilizada por una máquina de proteínas para cambiar cíclicamente su forma y así realizar una función particular. Por eso, resolver los cambios funcionales de la conformación en las proteínas es un desafío importante, con una importancia fundamental para la comprensión y el control de motores y máquinas biológicos de una sola molécula.
La complejidad de las interacciones entre átomos en una máquina de proteínas es tan alta que incluso las mejores supercomputadoras del mundo no pueden reproducir solo uno de sus ciclos operativos. En este artículo de revisión, Sin embargo, está demostrado que los aspectos esenciales del funcionamiento de tales nanodispositivos naturales ya pueden ser revelados mediante la exploración de modelos mecánicos muy simples de proteínas. es decir, tratando tales macromoléculas como redes elásticas obtenidas conectando partículas con un conjunto de resortes elásticos.
Los autores, el profesor Alexander Mikhailov y el profesor asistente Holger Flechsig del Nano Life Science Institute de la Universidad de Kanazawa en Japón, argumentan que las redes elásticas correspondientes a las máquinas de proteínas con dinámica funcional tienen propiedades especiales, surgió en el proceso de evolución biológica. A pesar de una aparente complejidad, los movimientos internos en tales sistemas proceden de manera ordenada, como si lo guiaran a lo largo de vías férreas ocultas. Por lo tanto, una máquina molecular se comporta de manera similar a los dispositivos mecánicos macroscópicos con movimientos altamente coordinados de sus partes. Esto asegura que la fábrica celular pueda funcionar de manera robusta a pesar de las fuertes fluctuaciones presentes en las nanoescalas.
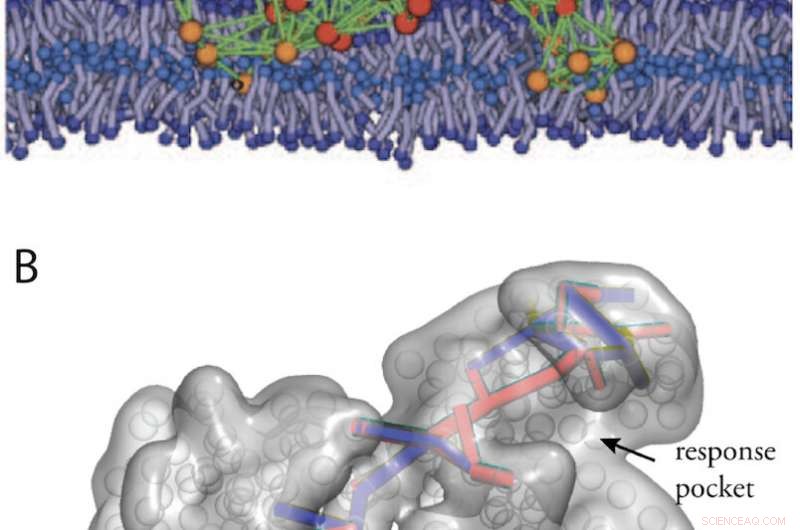
Estructuras similares a proteínas artificiales obtenidas por in-silico evolución. (A) Un modelo de máquina de proteínas en una membrana biológica (de la Fig. 11). (B) Vías de comunicación en una estructura alostérica diseñada (de la Ref. 34). Crédito:Universidad de Kanazawa
Usando este enfoque, Se pudieron realizar simulaciones que cubrían ciclos completos de operación y así se obtuvieron las primeras películas moleculares de máquinas de proteínas. Como ejemplo, La figura 1 de la publicación original de 2010 de los autores muestra cómo la proteína motora helicasa del virus de la hepatitis C, una parte principal de su maquinaria de replicación y un objetivo farmacológico importante para los fármacos antivirales, se mueve activamente a lo largo del ADN y lo descomprime mecánicamente.
Además, se podrían diseñar estructuras similares a proteínas artificiales con propiedades de máquina ejecutando una evolución informática de redes elásticas. En la Fig.2 se muestran dos ejemplos, una máquina modelo diseñada que opera dentro de una membrana biológica, y una máquina que exhibe comunicación alostérica.
Este artículo de revisión presenta una nueva perspectiva en la comprensión de la compleja maquinaria de las células biológicas. También allana el camino para enfoques novedosos en el diseño de nano-máquinas artificiales, una tarea de gran potencial para futuras aplicaciones biotecnológicas.