Los químicos de la RUDN descubrieron cómo evitar los subproductos en la síntesis de perovskitas Crédito:Natalia Deryugina
Un profesor de la RUDN, junto con sus colegas de otras universidades de Moscú, ha descrito el mecanismo de los subproductos producidos en el curso de la síntesis de perovskitas, minerales que tienen numerosas aplicaciones prospectivas, p.ej. como superconductores. El descubrimiento podría hacer que su producción sea más rápida y eficiente. El artículo fue publicado en Química de Materiales .
Las perovskitas son sustancias cristalinas que constan de dos o más metales y contienen tres átomos de oxígeno. Estos materiales se utilizan como superconductores, en celdas solares, láseres y sensores. La estructura cristalina de las perovskitas se forma en disolventes como el dimetilsulfóxido (DMSO), dimetilformamida (DMF), y gamma-butirolactona (GBL). El principal problema de su síntesis radica en la formación de compuestos intermedios entre las sustancias iniciales y las moléculas de un disolvente. Esto complica el proceso de cristalización y reduce los volúmenes del producto final.
Los autores estudiaron la estructura de los intermedios que se formaron en el curso de la síntesis de perovskitas en GBL. El estudio se basó en perovskitas que contienen plomo y átomos de diferentes halógenos (cloro, bromo, y yodo). Para ver los compuestos formados en el curso de la reacción, los investigadores utilizaron espectroscopía de dispersión Raman. Durante el experimento, los químicos cambiaron las proporciones de los componentes de síntesis iniciales y estudiaron las estructuras formadas en cada caso.
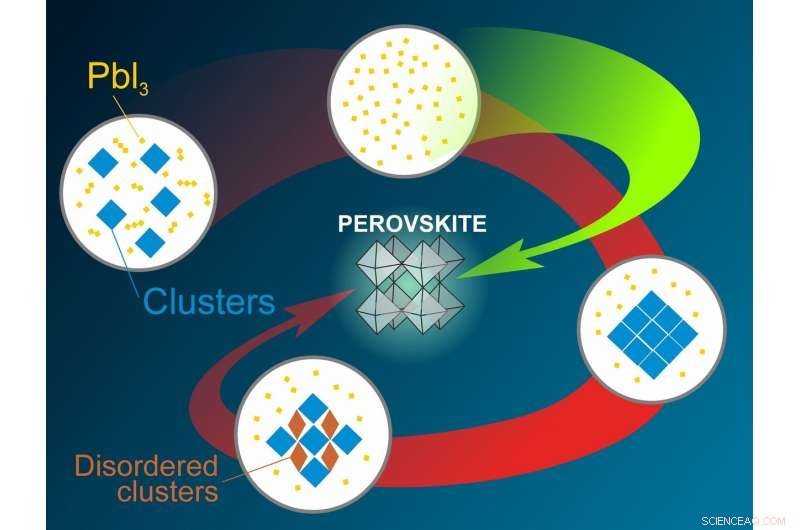
"Fuimos los primeros en encontrar tres tipos de fases intermedias que se forman en el curso de la cristalización de perovskita en gamma-butirolactona. El primer tipo es similar a las estructuras que ya nos son familiares, mientras que los tipos dos y tres son nuevas formaciones super-octaédricas. También descubrimos por qué sucede. A altas concentraciones de iones de yodo en una solución, la estructura está dominada por moléculas de pequeño tamaño que constan de un átomo de plomo y tres de yodo. Sin embargo, a medida que disminuye la concentración de iones de yodo, el solvente comienza a jugar el papel principal. Las formas complejas super-octaédricas de los intermediarios se forman bajo su influencia, "dice Viktor Khrustalyov, un coautor del estudio, Doctor. en Quimica, y jefe del Departamento de Química Inorgánica de la RUDN.
Habiendo estudiado cómo los productos intermedios que ralentizan la reacción y reducen los volúmenes del producto final ocurren en el curso de una reacción, los químicos desarrollaron un método para evitarlo. Para hacerlo sugirieron depositar perovskitas como películas delgadas y también usar soluciones iniciales con concentraciones más altas de yodo.