Crédito:Angewandte Chemie
La vinculación de moléculas terapéuticamente activas con anticuerpos específicos puede ayudar a pilotarlos hacia sus objetivos designados y minimizar los efectos secundarios, especialmente cuando se tratan tumores. En el diario Angewandte Chemie , Los científicos ahora han descrito nuevos conjugados hechos a partir de anticuerpos y un inhibidor de la proteína del huso de la cinesina. Cambiar el enlazador entre los dos componentes permite ajustar la actividad de este fármaco citostático, que es eficaz contra una amplia gama de cánceres.
Los medicamentos deben ser muy eficaces, pero relativamente libre de efectos secundarios. Esto es particularmente importante en el tratamiento del cáncer. debido a que los fármacos citostáticos utilizados interfieren con los mecanismos de regulación de todas las células del cuerpo, causando síntomas como deterioro de las defensas inmunitarias, perdida de cabello, y náuseas. Por tanto, los tratamientos tienen como objetivo introducir fármacos citostáticos directamente en las células tumorales antes de desencadenar su efecto tóxico. Una de las formas de lograr esto es unir moléculas de fármaco tan pequeñas a un anticuerpo para hacer un conjugado. El componente puente, llamado el enlazador, debe mantener el conjugado unido mientras circule en la sangre. El anticuerpo se une específicamente a los sitios de unión (antígenos) que son especialmente numerosos en las superficies de las células tumorales diana. El acoplamiento del anticuerpo desencadena la captación del conjugado dentro de las células cancerosas. Allí, el fármaco es liberado por enzimas para llevar a cabo su tarea destructiva específicamente en la célula cancerosa. Las células sanas permanecen en gran parte sin ser molestadas.
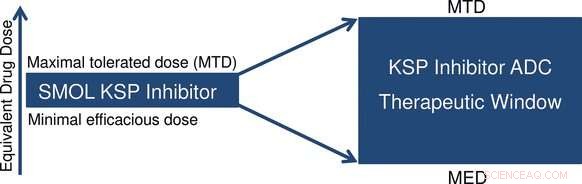
Hasta ahora, el número de fármacos citostáticos que se han incorporado con éxito a tales conjugados de anticuerpos ha sido limitado. Los investigadores dirigidos por Hans-Georg Lerchen (Bayer AG) ahora han probado esto con una citotoxina que utiliza un mecanismo diferente al de los fármacos citostáticos clásicos para atacar el ciclo celular. Es un nuevo inhibidor de la proteína del huso de quinesina (KSP) a base de pirrol. KSP juega un papel clave en la separación del centrosoma durante la división celular. El bloqueo de este paso provoca un fuerte efecto antitumoral. Incluso dosis muy bajas del inhibidor fueron muy eficaces contra una amplia gama de líneas celulares cancerosas. Lerchen y sus colaboradores han demostrado que esta técnica se puede utilizar para fabricar conjugados de anticuerpos muy activos. El uso de diferentes anticuerpos les permite dirigirse a una variedad de tipos de tumores.
Los investigadores pudieron conectar el inhibidor en una variedad de puntos de unión mediante enlaces estables al anticuerpo, lo que impidió la división prematura. Solo dentro de las células tumorales, los conjugados son metabolizados por enzimas, liberando el inhibidor. La variación del enlazador permite una variación controlada de las moléculas inhibidoras resultantes para que su actividad se pueda adaptar a requisitos específicos. Los inhibidores que no se pueden expulsar de las células se acumulan en las células tumorales, alargando su período activo. Los inhibidores que pueden ser expulsados pueden ingresar a las células tumorales vecinas, que es especialmente útil en el tratamiento de tumores que contienen un patrón heterogéneo de sitios de unión de anticuerpos.
Los nuevos conjugados son altamente efectivos in vitro y se demostró que son efectivos en modelos tumorales para diversas indicaciones in vivo. En experimentos con ratones, llevaron a la remisión completa de un modelo de tumor de vejiga humana, con efectos secundarios mínimos.