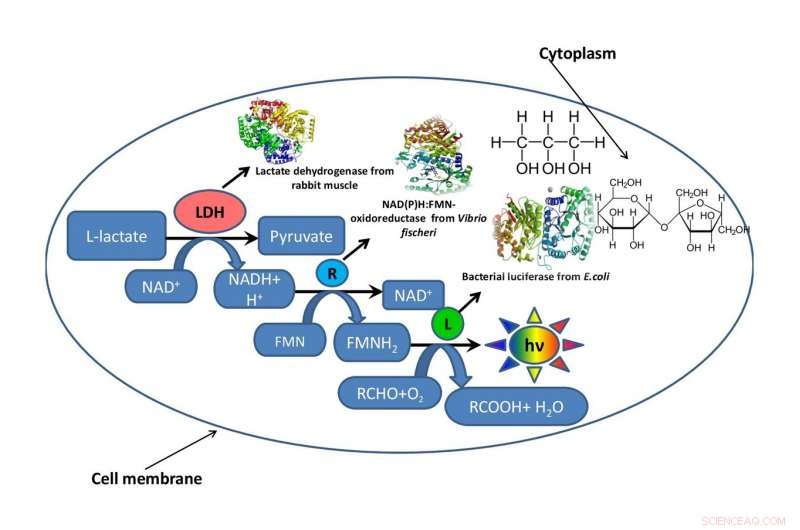
Esquema de una célula bacteriana con un fragmento de una cadena metabólica funcionando en su interior rodeada de glicerol o sacarosa que imitan el entorno intracelular. Crédito:Oleg Sutormin.
Un equipo del Instituto de Biología Fundamental y Biotecnología de SFU utilizó glicerol y sacarosa para simular el entorno intracelular de bacterias luminiscentes y llevó a cabo una serie de reacciones enzimáticas. Esperan desarrollar fragmentos de cadenas metabólicas con diferentes longitudes y estudiar reacciones fermentativas en condiciones cercanas a las intracelulares. La investigación fue publicada en el Catálisis molecular diario.
Cientos de reacciones que involucran enzimas ocurren constantemente en las células. Para estudiarlos con más detalle, los científicos intentan crear modelos experimentales completos del entorno intracelular. Una característica interesante de estos modelos de entornos artificiales es la posibilidad de ajustar sus parámetros para comprender cómo reaccionaría una determinada reacción enzimática y las diferencias entre las reacciones enzimáticas en una célula y las que se encuentran en las condiciones del tubo.
Para comprender cómo la viscosidad de la mezcla de reacción afecta la velocidad de los procesos enzimáticos, un equipo del Instituto de Biología Fundamental y Biotecnología de SFU simuló el ambiente intracelular usando dos solventes orgánicos:glicerol y sacarosa. Para probar el efecto de la viscosidad de la mezcla de reacción, los científicos utilizaron un fragmento de una cadena metabólica bioluminiscente.
El trabajo consta de tres etapas. En la primera etapa, los biofísicos desarrollaron varios sistemas de modelos artificiales hechos de glicerol y sacarosa con diferentes concentraciones de componentes, pero los mismos niveles de viscosidad del medio de reacción. En la segunda etapa, determinaron cómo la viscosidad de la mezcla de reacción afectó la velocidad de una reacción enzimática en el sistema acoplado de tres enzimas:LDH, NAD (P) H:FMN-oxidorreductasa, y luciferasa. En la tercera etapa, los investigadores evaluaron la estabilidad térmica del sistema de triple enzima en el rango de temperaturas de 15 a 80 grados.
Como resultado del estudio, los científicos concluyeron que la sacarosa limitaba la movilidad de las enzimas de manera más eficiente que el glicerol. La limitación de la movilidad puede provocar cambios en la velocidad de reacción o incluso en el mecanismo. Los investigadores recomiendan estudiar más a fondo la creciente estabilidad térmica de las enzimas en entornos de mezcla de reacción viscosa y el aumento de temperatura. También proponen un enfoque para construir las cadenas metabólicas celulares de múltiples enzimas dentro de la célula bacteriana luminosa.
"Debido a la gran cantidad de reacciones enzimáticas dentro de una célula real, para que el proceso del metabolismo avance rápida y continuamente dentro de él, las enzimas deben tener una alta cooperatividad. Por lo tanto, cuanto más cambia la estabilidad térmica de las enzimas en presencia de viscógenos, Cuanto mejor sea la cooperación de los sistemas enzimáticos estudiados dentro de las condiciones de la célula real, y mayor es la posibilidad de que un fragmento artificial de una cadena metabólica sea natural para una célula bacteriana. Es extremadamente importante estudiar la influencia de los disolventes orgánicos viscosos sobre la velocidad y la estabilidad térmica de las reacciones enzimáticas. La singularidad de nuestro estudio es que utilizamos compuestos naturales:glicerol y sacarosa que se encuentran realmente en la célula real, a diferencia de los agentes de hacinamiento que se utilizan en estudios similares por otros investigadores, "dice Oleg Sutormin, un coautor del estudio, e investigador asociado junior del Laboratorio de Biotecnologías Bioluminiscentes de SFU.