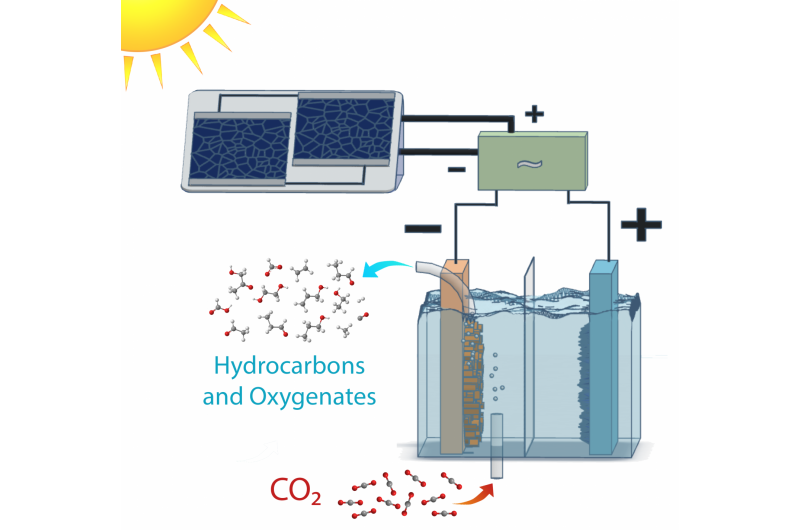
Esquema de una celda de electrólisis alimentada por energía solar que convierte el dióxido de carbono en hidrocarburos y productos oxigenados con una eficiencia mucho mayor que la fotosíntesis natural. La electrónica de adaptación de potencia permite que el sistema funcione en una variedad de condiciones solares. Crédito:Clarissa Towle / Berkeley Lab
Los científicos del Laboratorio Nacional Lawrence Berkeley del Departamento de Energía (Berkeley Lab) han aprovechado el poder de la fotosíntesis para convertir el dióxido de carbono en combustibles y alcoholes con eficiencias mucho mayores que las de las plantas. El logro marca un hito significativo en el esfuerzo por avanzar hacia fuentes sostenibles de combustible.
Muchos sistemas han reducido con éxito el dióxido de carbono a precursores químicos y combustibles, como el monóxido de carbono o una mezcla de monóxido de carbono e hidrógeno conocida como gas de síntesis. Este nuevo trabajo descrito en un estudio publicado en la revista Ciencias de la energía y el medio ambiente , es el primero en demostrar con éxito el enfoque de pasar del dióxido de carbono directamente a los productos objetivo, a saber, etanol y etileno, en eficiencias de conversión de energía que rivalizan con sus contrapartes naturales.
Los investigadores hicieron esto optimizando cada componente de un sistema fotovoltaico-electroquímico para reducir la pérdida de voltaje, y crear nuevos materiales cuando los existentes no fueran suficientes.
"Este es un desarrollo emocionante, "dijo el investigador principal del estudio, Joel Ager, un científico de Berkeley Lab con nombramientos conjuntos en las divisiones de Ciencias de los Materiales y Ciencias Químicas. "A medida que los crecientes niveles de CO2 atmosférico cambian el clima de la Tierra, la necesidad de desarrollar fuentes de energía sostenibles se ha vuelto cada vez más urgente. Nuestro trabajo aquí muestra que tenemos un camino plausible para producir combustibles directamente a partir de la luz solar ".
Ese camino del sol al combustible se encuentra entre los objetivos clave del Centro Conjunto para la Fotosíntesis Artificial (JCAP), un Centro de Innovación Energética del DOE establecido en 2010 para avanzar en la investigación de combustibles solares. El estudio se realizó en el campus de Berkeley Lab de JCAP.
El enfoque inicial de la investigación de JCAP fue abordar la división eficiente del agua en el proceso de fotosíntesis. Habiendo logrado en gran medida esa tarea utilizando varios tipos de dispositivos, Los científicos de JCAP que realizan una reducción de dióxido de carbono impulsada por la energía solar comenzaron a fijarse en lograr eficiencias similares a las demostradas para la división del agua. considerado por muchos como el próximo gran desafío en la fotosíntesis artificial.
Otro grupo de investigación en Berkeley Lab está abordando este desafío centrándose en un componente específico en un sistema fotovoltaico-electroquímico. En un estudio publicado hoy, describen un nuevo catalizador que puede lograr la conversión de dióxido de carbono a multicarbonos utilizando insumos de energía récord bajos.
No solo para el mediodía
Para este estudio de JCAP, los investigadores diseñaron un sistema completo para trabajar en diferentes momentos del día, no solo a un nivel de energía lumínica de iluminación de 1 sol, que es equivalente al pico de brillo al mediodía en un día soleado. Variaron el brillo de la fuente de luz para mostrar que el sistema seguía siendo eficiente incluso en condiciones de poca luz.
Cuando los investigadores acoplaron los electrodos a células fotovoltaicas de silicio, lograron eficiencias de conversión solar de 3 a 4 por ciento para iluminación de 0,35 a 1 sol. Cambiar la configuración a una de alto rendimiento, La celda solar en tándem conectada en tándem produjo una eficiencia de conversión a hidrocarburos y compuestos oxigenados superior al 5 por ciento a una iluminación de 1 sol.

A la izquierda hay una vista de la superficie de un cátodo nanocoral bimetálico de cobre y plata tomado de una micrografía electrónica de barrido. A la derecha hay una imagen de rayos X de dispersión de energía del cátodo con el cobre (en rosa / rojo) y plata (en verde) resaltados. Crédito:Gurudayal / Berkeley Lab
"Hicimos un pequeño baile en el laboratorio cuando llegamos al 5 por ciento, "dijo Ager, quien también tiene un nombramiento como profesor adjunto en el Departamento de Ciencia e Ingeniería de Materiales de UC Berkeley.
Entre los nuevos componentes desarrollados por los investigadores se encuentran un cátodo nanocoral de cobre-plata, que reduce el dióxido de carbono a hidrocarburos y oxigenados, y un ánodo de nanotubos de óxido de iridio, que oxida el agua y crea oxígeno.
"La buena característica del nanocoral es que, como plantas, puede fabricar los productos de destino en una amplia gama de condiciones, y es muy estable, "dijo Ager.
Los investigadores caracterizaron los materiales en el Centro Nacional de Microscopía Electrónica de Molecular Foundry, una instalación para usuarios de la Oficina de Ciencias del DOE en Berkeley Lab. Los resultados les ayudaron a comprender cómo funcionaban los metales en el cátodo bimetálico. Específicamente, aprendieron que la plata ayuda a reducir el dióxido de carbono a monóxido de carbono, mientras que el cobre se recupera de allí para reducir aún más el monóxido de carbono a hidrocarburos y alcoholes.
Buscando mejor rupturas de baja energía
Dado que el dióxido de carbono es una molécula obstinadamente estable, romperlo normalmente implica una importante aportación de energía.
"Reducir el CO2 a un producto final de hidrocarburo como el etanol o el etileno puede requerir hasta 5 voltios, Empezar a acabar, "dijo el autor principal del estudio, Gurudayal, becario postdoctoral en Berkeley Lab. "Nuestro sistema redujo eso a la mitad manteniendo la selectividad de los productos".
Notablemente, los electrodos funcionaron bien en agua, un ambiente de pH neutro.
"Los grupos de investigación que trabajan en ánodos lo hacen principalmente en condiciones alcalinas, ya que los ánodos suelen requerir un entorno de pH alto, que no es ideal para la solubilidad del CO2, ", dijo Gurudayal." Es muy difícil encontrar un ánodo que funcione en condiciones neutrales ".
Los investigadores personalizaron el ánodo haciendo crecer los nanotubos de óxido de iridio en una superficie de óxido de zinc para crear un área de superficie más uniforme para soportar mejor las reacciones químicas.
"Al trabajar en cada paso con tanto cuidado, estos investigadores demostraron un nivel de rendimiento y eficiencia que la gente no creía posible en este momento, "dijo Frances Houle, química del Berkeley Lab, Subdirector de Integración de la Ciencia y la Investigación de la JCAP, que no formó parte del estudio. "Este es un gran paso adelante en el diseño de dispositivos para la reducción eficiente de CO2 y la prueba de nuevos materiales, y proporciona un marco claro para el futuro avance de los dispositivos de reducción de CO2 impulsados por energía solar totalmente integrados ".