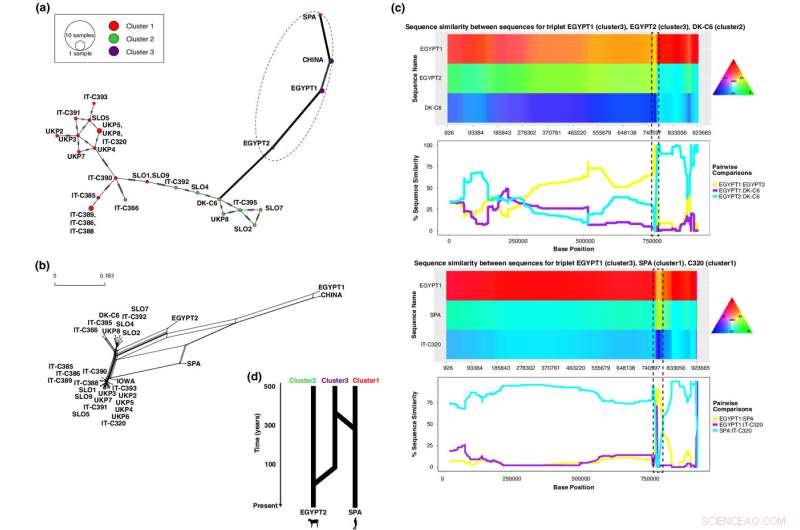
El análisis de recombinación del cromosoma 1 identifica dos secuencias híbridas, Spa1 (un aislado humano del grupo 1) y Egypt 2 (un aislado de ternera del grupo 3). ( a ) Red que muestra que los haplotipos de los aislados híbridos Spa1 y Egypt2 divergen del resto de los aislados y están estrechamente asociados con sus secuencias parentales menores (aislados del grupo 3). ( b ) Red filogenética que muestra bucles entre aislados híbridos, que representan una recombinación potencial. (c) Gráficas de similitud de secuencia obtenidas con HybridCheck para diferentes tripletes de aislamientos involucrados en un evento de recombinación (híbrido, padre principal, padre menor). La similitud de secuencia se muestra a lo largo de las posiciones cromosómicas (eje x) mediante un mapa de colores en el que las regiones con el mismo polimorfismo comparten colores (arriba) y mediante gráficos de líneas que informan el porcentaje de similitud en el eje y (abajo). Los gráficos de las regiones recombinantes que presentan una gran similitud entre los aislados híbridos y sus secuencias parentales menores en las regiones recombinantes están encerrados entre recuadros discontinuos. ( d ) Representación esquemática de eventos de recombinación en aislados híbridos, que muestra que Egypt2 y Spa1 recibieron variación genética de un grupo 3, alrededor de 49 (21-96; 95% IC) y 289 (204-395; 95% IC) años hace, respectivamente. Crédito:Ecología Molecular (2022). DOI:10.1111/mec.16556
Es probable que los parásitos que causan diarrea severa se vuelvan más virulentos debido a la velocidad a la que intercambian su ADN y evolucionan, según una nueva investigación de la Universidad de East Anglia.
Los investigadores estudiaron los genomas de Cryptosporidium parvum, un parásito zoonótico que causa diarrea severa tanto en humanos como en animales.
Descubrieron que diferentes linajes de estos parásitos están intercambiando cada vez más su ADN, lo que ha ayudado a que el parásito evolucione más rápido, lo que podría dar como resultado cepas más virulentas y mejor adaptadas.
El nuevo estudio muestra que los linajes de Cryptosporidium parvum han intercambiado más ADN en los últimos 200 años que en todo el tiempo anterior.
Y lo atribuyen a la globalización y nuestro contacto cada vez más cercano con los animales, lo que aumenta la tasa de eventos indirectos.
Uno de los investigadores principales, el profesor Cock Van Oosterhout, de la Facultad de Ciencias Ambientales de la UEA, dijo:"Cryptosporidium es un género importante de parásitos zoonóticos, y es uno de varios microorganismos que causan enfermedades diarreicas tanto en humanos como en algunos animales. En humanos, es responsable de alrededor de 57 000 muertes cada año, el 80 % de las cuales son de niños menores de cinco años.
"La gran mayoría de estos se encuentran en países de bajos ingresos, pero también se producen brotes en el Reino Unido y en otros lugares de Europa. No hay ningún fármaco o vacuna eficaz disponible, por lo que es fundamental comprender la transmisión y evolución de este parásito.
"Sabemos que hay varios linajes del parásito Cryptosporidium parvum, pero queríamos saber más sobre cómo evolucionan y, en particular, por qué esta especie puede volverse más virulenta que en el pasado".
El equipo, dirigido por la UEA en colaboración con científicos de Italia y Australia, utilizó el análisis de la secuencia del genoma completo para obtener más información sobre estos intercambios genéticos.
Compararon 32 secuencias genómicas completas de cepas humanas y animales recolectadas en Europa, EE. UU., Egipto y China.
El profesor Van Oosterhout dijo:"Descubrimos que diferentes linajes de estos parásitos están intercambiando cada vez más su ADN. En los últimos 200 años, se ha intercambiado alrededor del 22 por ciento del genoma de estos parásitos".
"Esto es significativamente más que el ADN que han intercambiado todo el tiempo antes. Los genes que están involucrados en la virulencia parecen verse particularmente afectados por tales intercambios genéticos. El genoma de los parásitos que infectan a los humanos posee algo de ADN de los parásitos que normalmente se encuentran en vacas y corderos.
"Creemos que estos intercambios genéticos ayudan a que el parásito evolucione más rápido y que esto puede resultar en parásitos humanos más virulentos y mejor adaptados. Esto es realmente importante porque, como nos ha demostrado el COVID-19, los parásitos humanos pueden evolucionar rápidamente.
"Presumimos que la tasa de evolución se acelera aún más porque el parásito puede evolucionar en múltiples especies hospedadoras. Esto significa que las adaptaciones novedosas que han evolucionado en parásitos que infectan a una especie hospedante ahora pueden ser utilizadas por parásitos que infectan a otra especie de hospedantes.
"La mayor conectividad en nuestro mundo globalizado y el contacto cercano entre humanos y animales domésticos aumenta la tasa de eventos indirectos y indirectos.
"Usando el análisis de la secuencia del genoma completo, ahora podemos estudiar estos intercambios genéticos e identificar cuándo y dónde tienen lugar. Esto nos ayudará a controlar mejor estas enfermedades infecciosas emergentes de parásitos y patógenos zoonóticos", agregó.
"Los intercambios genéticos recientes y la mezcla dan forma al genoma y la estructura de la población de un parásito zoonótico" se publica en la revista Molecular Ecology .