Los reactores de flujo llenos de enzimas pueden producir ciertas sustancias químicas de forma suave y cuidadosa. Sin embargo, su desempeño hasta ahora ha sido limitado. Un equipo de investigación del Helmholtz-Zentrum Hereon y de la Universidad RWTH de Aquisgrán ha conseguido multiplicar por mil el rendimiento.
Utilizando una nanomembrana hecha a medida, han logrado que las moléculas que se van a convertir entren en contacto mucho más estrecho con las enzimas, aumentando así drásticamente la velocidad de reacción. El nuevo proceso podría utilizarse, entre otras cosas, para la producción sostenible de fosfato. El grupo de trabajo presenta sus resultados en la revista Nature Communications .
Las enzimas son biocatalizadores que pueden utilizarse para producir sustancias químicas de forma respetuosa con el medio ambiente y ahorrando energía. Sin embargo, el proceso no siempre facilita su uso eficiente. Uno de los conceptos son los reactores de flujo continuo. Consisten en pequeños canales a cuyas paredes se adhieren las enzimas. Cuando una solución fluye a través de estos canales, las moléculas contenidas en la solución pueden acoplarse a los biocatalizadores para reaccionar con su ayuda para formar el producto deseado.
Hasta ahora, estos reactores no han funcionado de forma óptima, ya que normalmente tienen canales de tamaño milimétrico; las enzimas, en cambio, son de tamaño nanométrico. Como resultado, muchas de las moléculas que fluyen ni siquiera entran en contacto con los biocatalizadores y, por lo tanto, no tienen oportunidad de reaccionar químicamente.
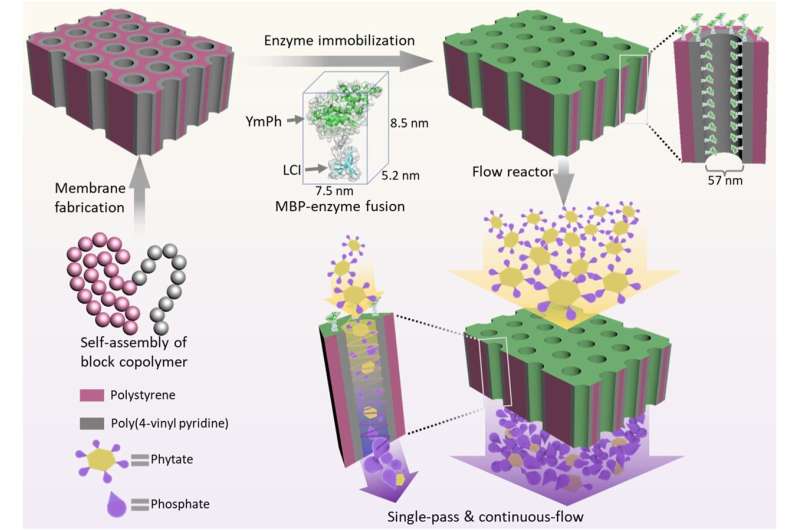
Para solucionar este problema, el grupo de trabajo utilizó una membrana especial desarrollada en el Helmholtz-Zentrum Hereon en Geesthacht. "Esta membrana se crea mediante el autoensamblaje de los llamados copolímeros en bloque", explica el Dr. Volker Abetz, director del Instituto Hereon de Investigación de Membranas y profesor de Química Física de la Universidad de Hamburgo. "Su superficie tiene una alta densidad de poros cilíndricos del mismo tamaño". Son diminutos, con un diámetro de sólo 50 nanómetros. Debajo de la superficie hay una estructura porosa más abierta hecha del mismo copolímero en bloque.
Los científicos utilizaron una molécula auxiliar especialmente diseñada, una especie de péptido adhesivo, para unir estas paredes de poros con enzimas. "Se une a la pared de los poros por un lado y a la enzima por el otro", explica el Dr. Ulrich Schwaneberg, profesor de biotecnología en la Universidad RWTH de Aquisgrán y miembro de la dirección científica del Instituto Leibniz de Materiales Interactivos. "El péptido actúa como una especie de amortiguador que mantiene la enzima a cierta distancia de la pared del poro en todo momento."
El equipo utilizó una enzima llamada fitasa para su prototipo. Provoca la descomposición del fitato, un compuesto que contiene fósforo y que se encuentra, entre otros, en los cereales. En la práctica, la enzima fitasa se añade, por ejemplo, a los piensos para animales. Esto promueve la liberación de fosfato biogénico, que luego puede usarse como fertilizante sostenible.
"El prototipo de nuestro reactor de flujo tiene un diseño relativamente sencillo", afirma el investigador de Hereon, el Dr. Zhenzhen Zhang. "La membrana tiene aproximadamente el tamaño de una hoja de papel, además de un sistema que permite que la solución de fitato fluya a través de la membrana".
Gracias a los poros estrechos, densamente llenos de enzimas, se pudieron convertir en fosfato unas mil veces más moléculas de fitato que en los reactores de flujo continuo anteriores:un rendimiento notable. También fue útil que los poros de la membrana estuvieran cargados eléctricamente positivamente y las moléculas de fitato cargadas negativamente. Las fuerzas de atracción resultantes también ayudaron a poner las moléculas en contacto con las enzimas.
"Probamos la membrana durante 30 días y perdió muy poco de su eficiencia", dice Zhang. "Sin duda, debería ser posible ampliar nuestro reactor a escala industrial". Como el proceso Hereon también se puede utilizar para producir membranas con poros más pequeños o más grandes, también debería ser posible equipar el reactor con otras enzimas que luego puedan acelerar otras reacciones químicas.
Sin embargo, todavía quedan preguntas sin respuesta por aclarar. "Aún no hemos comprendido en detalle cómo se forman las estructuras de las membranas", explica Abetz. "Si lo logramos, esperamos poder producir los poros cilíndricos de la membrana de una manera mucho más específica que antes."
Más información: Zhenzhen Zhang et al, Un reactor enzimático de flujo continuo basado en una membrana de copolímero de bloque nano e isoporoso de tamaño de poro coincidente, Nature Communications (2024). DOI:10.1038/s41467-024-47007-y
Información de la revista: Comunicaciones sobre la naturaleza
Proporcionado por la Asociación Helmholtz de Centros de Investigación Alemanes