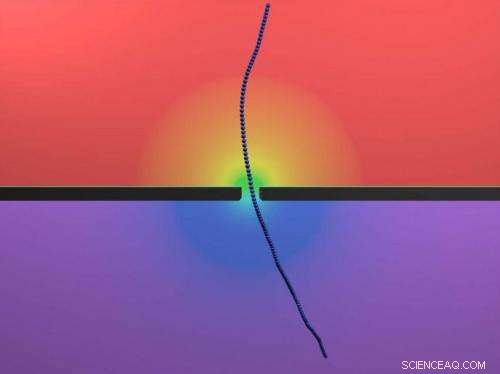
Una simulación por computadora muestra un virus fd que se desplaza a través de un nanoporo. A diferencia del ADN, que se enreda en solución, el fd permanece rígido y recto, permitiendo a los investigadores estudiar la física de la translocación a través de nanoporos. Crédito:Hendrick de Haan / Stein lab / Brown University
Los nanoporos pueden algún día liderar una revolución en la secuenciación del ADN. Al deslizar las moléculas de ADN de una en una a través de pequeños orificios en una membrana delgada, puede ser posible decodificar largos tramos de ADN a la velocidad del rayo. Científicos, sin embargo, No he descubierto la física de cómo las cadenas de polímeros como el ADN interactúan con los nanoporos. Ahora, con la ayuda de un tipo particular de virus, Los investigadores de la Universidad de Brown han arrojado nueva luz sobre esta física a nanoescala.
"Lo que nos interesó en esto fue que todos en el campo estudiaron el ADN y desarrollaron modelos de cómo interactúan con los nanoporos, "dijo Derek Stein, profesor asociado de física e ingeniería en Brown que dirigió la investigación. "Pero incluso las cosas más básicas que esperarías que los modelos pudieran predecir a partir de las propiedades básicas del ADN, no podrías hacerlo. La única forma de salir de esa rutina era estudiar algo diferente".
Los resultados, publicado hoy en Comunicaciones de la naturaleza , podría no solo ayudar en el desarrollo de dispositivos de nanoporos para la secuenciación del ADN, también podrían conducir a una nueva forma de detectar patógenos peligrosos.
Enderezando la física
El concepto detrás de la secuenciación de nanoporos es bastante simple. Se perfora un agujero de unas pocas mil millonésimas de metro de ancho en una membrana que separa dos charcos de agua salada. Se aplica una corriente eléctrica al sistema, que ocasionalmente atrapa una hebra de ADN cargada y la empuja a través del poro, un fenómeno llamado translocación. Cuando una molécula se transloca, provoca variaciones detectables en la corriente eléctrica a través del poro. Al observar cuidadosamente esas variaciones en la corriente, los científicos pueden distinguir nucleótidos individuales:las A, C's, G y T codificados en moléculas de ADN.
Los primeros secuenciadores de nanoporos disponibles comercialmente pueden estar a solo unos años de distancia, pero a pesar de los avances en el campo, sorprendentemente, se sabe poco sobre la física básica involucrada cuando los polímeros interactúan con los nanoporos. Eso se debe en parte a las complejidades involucradas en el estudio del ADN. En solución, Las moléculas de ADN forman bolas de garabatos aleatorios, lo que hace que la comprensión de su comportamiento físico sea extremadamente difícil.
Por ejemplo, los factores que gobiernan la velocidad de la translocación del ADN no se comprenden bien. A veces, las moléculas atraviesan un poro rápidamente; otras veces se deslizan más despacio, y nadie entiende completamente por qué.
Una posible explicación es que la configuración ondulada del ADN hace que cada molécula experimente diferencias en el arrastre a medida que se empuja a través del agua hacia el poro. "Si una molécula se arruga junto al poro, tiene una distancia más corta para viajar y experimenta menos resistencia, "dijo Angus McMullen, estudiante de posgrado en física en Brown y autor principal del estudio. "Pero si se estira, se sentiría arrastrado a lo largo de toda la longitud y eso haría que fuera más lento".
El efecto de arrastre es imposible de aislar experimentalmente usando ADN, pero el virus que estudiaron McMullen y sus colegas ofreció una solución.

El virus fd, rígido y parecido a una varilla, ayuda a los científicos a comprender la física de los nanoporos. Los nanoporos podrían ser útiles para detectar otros virus que compartan esas características, entre ellos el Ébola y Marburg.
Los investigadores observaron fd, un virus inofensivo que infecta e. bacterias coli. Dos cosas hacen que el virus sea un candidato ideal para el estudio con nanoporos. Primero, Los virus fd son todos clones idénticos entre sí. Segundo, a diferencia del ADN ondulado, El virus fd es rígido, Molécula en forma de varilla. Debido a que el virus no se enrolla como lo hace el ADN, el efecto del arrastre en cada uno debe ser esencialmente el mismo cada vez.
Con el arrastre eliminado como fuente de variación en la velocidad de translocación, los investigadores esperaban que la única fuente de variación fuera el efecto del movimiento térmico. Las diminutas moléculas de virus chocan constantemente contra las moléculas de agua en las que están inmersas. Unas cuantas patadas térmicas aleatorias desde la parte trasera acelerarían el paso del virus a medida que atraviesa el poro. Unas cuantas patadas de frente lo frenarían.
Los experimentos mostraron que, si bien el movimiento térmico explica gran parte de la variación en la velocidad de translocación, no lo explicó todo. Para sorpresa de los investigadores, encontraron otra fuente de variación que aumentaba cuando aumentaba el voltaje a través del poro.
"Pensamos que la física sería muy clara, "dijo Jay Tang, profesor asociado de física e ingeniería en Brown y uno de los coautores del estudio. "Tienes este [virus] rígido con un diámetro y tamaño bien definidos y esperarías una señal muy clara. Como resultado, encontramos una física desconcertante que sólo podemos explicar parcialmente ".
Los investigadores no pueden decir con certeza qué está causando la variación que observaron, pero tienen algunas ideas.
"Se ha predicho que, dependiendo de dónde se encuentre [un objeto] dentro del poro, podría tirar más fuerte o más débil, ", Dijo McMullen." Si está en el centro del poro, tira un poco más débil que si estuviera justo en el borde. Eso ha sido predicho pero nunca verificado experimentalmente. Esto podría ser una prueba de que eso sucedió, pero todavía estamos haciendo un trabajo de seguimiento ".
Hacia un secuenciador de nanoporos y más
Una mejor comprensión de la velocidad de translocación podría mejorar la precisión de la secuenciación de nanoporos, Dice McMullen. También sería útil en la tarea crucial de medir la longitud de las cadenas de ADN. "Si puede predecir la velocidad de translocación, "McMullen dijo, "entonces se puede obtener fácilmente la longitud del ADN a partir de la duración de su translocación".
La investigación también ayudó a revelar otros aspectos del proceso de translocación que podrían ser útiles en el diseño de dispositivos futuros. El estudio mostró que la corriente eléctrica tiende a alinear la cabeza de los virus con el poro, pero en ocasiones cuando no están alineados, tienden a rebotar en el borde del poro hasta que el movimiento térmico los alinea para atravesarlos. Sin embargo, cuando el voltaje se elevó demasiado, los efectos térmicos se suprimieron y el virus se adhirió a la membrana. Eso sugiere un punto óptimo en el voltaje donde es más probable la translocación de cabeza por delante.
Nada de esto es observable directamente:el sistema es simplemente demasiado pequeño para ser visto en acción. Pero los investigadores pudieron inferir lo que estaba sucediendo al observar cambios leves en la corriente a través del poro.
"Cuando los virus fallan, traquetean y vemos estos pequeños baches en la corriente, "Dijo Stein." Así que con estos pequeños bultos, estamos empezando a tener una idea de lo que hace la molécula antes de deslizarse. Normalmente, estos sensores están ciegos a todo lo que está sucediendo hasta que la molécula se desliza a través de ellos ".
Eso habría sido imposible de observar usando ADN. La flexibilidad de la molécula de ADN le permite atravesar un poro en una configuración plegada incluso si no está alineada de frente. Pero debido a que el virus es rígido, no se puede doblar para pasar. Eso permitió a los investigadores aislar y observar esas dinámicas de contacto.
"Estos virus son únicos, "Dijo Stein." Son como pequeñas varas de medida perfectas ".
Además de arrojar luz sobre la física básica, el trabajo también puede tener otra aplicación. Si bien el virus fd en sí mismo es inofensivo, las bacterias que infecta — e. coli — no lo es. Basado en este trabajo, podría ser posible construir un dispositivo nanoporo para detectar la presencia de fd, y por poder, mi. coli. Otros virus peligrosos —Ebola y Marburg entre ellos— comparten la misma estructura en forma de varilla que fd.
"Esta podría ser una forma fácil de detectar estos virus, ", Dijo Tang." Así que esa es otra aplicación potencial para esto ".