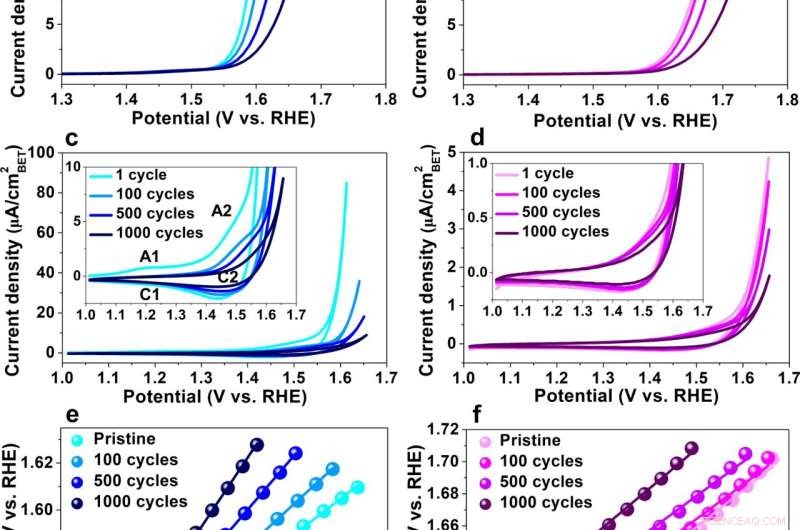
Fig. 1:Actividad REA de Co2 FeO4 y CoFe2 O4 nanopartículas. a, b Curvas de voltamperometría de barrido lineal (LSV) registradas a una velocidad de barrido de 10 mV/s en KOH 1,0 M en electrodos de carbón vítreo depositados con Co2 FeO4 y CoFe2 O4 nanopartículas en estado prístino y después de 100, 500 y 1000 ciclos de mediciones de voltamperometría cíclica (CV), c, d CV de Co2 FeO4 y CoFe2 O4 después de uno, 100, 500 y 1000 ciclos registrados a una velocidad de barrido de 50 mV/s en 1,0 M KOH en condiciones OER, e, f Tafel pendientes de Co2 FeO4 y CoFe2 O4 en el prístino y después de 100, 500 y 1000 ciclos, derivadas de las curvas LSV en a, b. Los datos de origen se proporcionan como un archivo de datos de origen. Las barras de error de las pendientes de Tafel en e, f se midieron mediante ajuste de curva lineal. Crédito:DOI:10.1038/s41467-021-27788-2
Investigadores de la Ruhr-Universität Bochum, la Universidad de Duisburg-Essen y el Instituto Max Planck para la Conversión de Energía Química en Mülheim an der Ruhr cooperaron en el proyecto como parte del Centro de Investigación Colaborativo "Catálisis de oxidación heterogénea en fase líquida".
En RUB, un equipo encabezado por Weikai Xiang y el profesor Tong Li de Caracterización a escala atómica trabajó junto con la Cátedra de Electroquímica y Materiales a Nanoescala y la Cátedra de Química Industrial. También participaron institutos en Shanghai, China, y Didcot, Reino Unido. El equipo presenta sus hallazgos en la revista Nature Communications , publicado en línea el 10 de enero de 2022.
Partículas observadas durante el proceso de catálisis
Los investigadores estudiaron dos tipos diferentes de nanopartículas hechas de óxido de hierro y cobalto que tenían alrededor de diez nanómetros. Analizaron las partículas durante la catálisis de la llamada reacción de evolución de oxígeno. Esta es una reacción media que ocurre durante la división del agua para la producción de hidrógeno:el hidrógeno se puede obtener dividiendo el agua usando energía eléctrica; En el proceso se producen hidrógeno y oxígeno. El cuello de botella en el desarrollo de procesos de producción más eficientes es la reacción parcial en la que se forma el oxígeno, es decir, la reacción de evolución del oxígeno. Esta reacción cambia la superficie del catalizador que se vuelve inactivo con el tiempo. Los cambios estructurales y composicionales en la superficie juegan un papel decisivo en la actividad y estabilidad de los electrocatalizadores.
Para las nanopartículas pequeñas con un tamaño de alrededor de diez nanómetros, obtener información detallada sobre lo que sucede en la superficie del catalizador durante la reacción sigue siendo un desafío. Usando tomografía de sonda atómica, el grupo visualizó con éxito la distribución de los diferentes tipos de átomos en los catalizadores de óxido de cobalto y hierro en tres dimensiones. Al combinarlo con otros métodos, mostraron cómo la estructura y la composición de la superficie cambiaban durante el proceso de catálisis y cómo este cambio afectaba el rendimiento catalítico.
"La tomografía con sonda atómica tiene un enorme potencial para proporcionar información atómica sobre los cambios de composición en la superficie de las nanopartículas de catalizadores durante reacciones catalíticas importantes, como la reacción de evolución de oxígeno para la producción de hidrógeno o CO2 reducción", concluye Tong Li. + Explore más