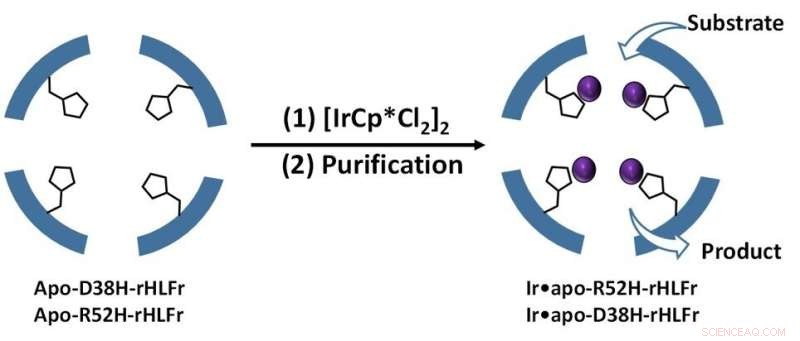
Figura 1. La jaula se diseñó con reemplazos de aminoácidos mediante la introducción de mutaciones específicas del sitio que permitieron una mayor captación de IrCp*. Crédito:Takafumi Ueno del Instituto de Tecnología de Tokio
Una nueva nanojaula de ferritina híbrida con residuos de histidina muestra una absorción de iones metálicos 1,5 veces mayor y una eficiencia catalítica mejorada para la producción de alcohol, según los investigadores de Tokyo Tech en un nuevo estudio. Sus hallazgos sugieren que las bio-nanocajas híbridas podrían catalizar eficazmente reacciones para producir productos industrialmente importantes.
Los polímeros biológicos pueden autoensamblarse espontáneamente en estructuras complejas que se asemejan a recipientes o jaulas, pero son mucho más pequeñas y se denominan "nanojaulas". Estas estructuras pueden acomodar una amplia gama de moléculas en su interior que se comportan como "huéspedes". Un ejemplo popular es la "nanojaula de ferritina", que está formada por el autoensamblaje de 24 subunidades en la proteína ferritina y puede contener iones metálicos que son catalizadores importantes. Con la ayuda de estos iones metálicos, una reacción catalítica convierte cualquier sustrato en un producto. Aunque son ampliamente conocidas, las aplicaciones potenciales de la jaula de ferritina en la industria aún no se han explorado por completo.
Hasta el momento, la mayoría de los esfuerzos para aumentar la absorción de iones metálicos en la ferritina han resultado en jaulas con baja estabilidad. Para que el "invitado" se sienta bien dentro de la jaula, la clave es un diseño eficaz. Teniendo eso en cuenta, un equipo de científicos dirigido por el profesor Takafumi Ueno, del Instituto de Tecnología de Tokio, Japón (Tokyo Tech), introdujo mutaciones específicas del sitio en el núcleo de la nanojaula de ferritina y aumentó su absorción del complejo de iridio (IrCp* ). Sus hallazgos se publican en Angewandte Chemie . El iridio es un catalizador vital en la vía de producción de alcohol y se utiliza comercialmente en las industrias farmacéutica, alimentaria y química.
El profesor Ueno explica:"Según la literatura anterior, sabíamos que la presencia de aminoácidos de coordinación en la jaula mejora la actividad del iridio y que sustituir estos aminoácidos con residuos apropiados podría aliviar el problema. Dado que el complejo de iridio se comporta como un catalizador, la coordinación los residuos harían el trabajo". Los autores utilizaron el aminoácido histidina para reemplazar dos residuos, la arginina y el ácido aspártico de las jaulas de ferritina regulares (de tipo salvaje) y crear los mutantes R52H y D38H. Sorprendentemente, la estructura de ensamblaje o el tamaño de la jaula no se vieron afectados por estos cambios.
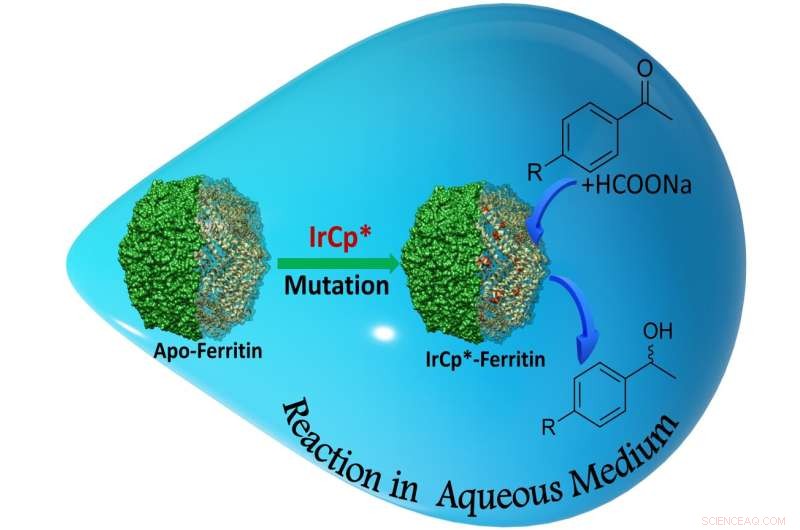
Figura 2. La nanojaula actúa como biocatalizador híbrido durante la conversión de sustratos a alcoholes con alta especificidad. Crédito:Takafumi Ueno del Instituto de Tecnología de Tokio
A continuación, agregaron IrCp* a los mutantes y descubrieron que R52H podía incrustar 1,5 veces más átomos de iridio que la jaula de tipo salvaje (Figura 1). Pero, lo que les llamó la atención fue el mutante D38H, que se comportó exactamente como el tipo salvaje. Entonces, ¿por qué ambas mutaciones no tuvieron el mismo efecto? Según el profesor Ueno, "esto implica que no es solo la presencia del residuo de histidina sino también su posición lo que es crucial para determinar la eficiencia de absorción en la jaula".
Usando las nuevas jaulas catalíticas, los investigadores pudieron lograr tasas de producción de alcohol de hasta el 88%. Evidentemente, las mutaciones favorecieron un reordenamiento estructural de los componentes de la reacción, lo que mejoró la tasa de conversión (Figura 2).
Para comprender cómo se comportaba el sustrato dentro de la jaula, los investigadores utilizaron simulaciones en las que las moléculas del sustrato podían moverse libremente dentro de la nanojaula. Observaron algunas interacciones entre el sustrato y la histidina en el mutante R52H, que no estaban presentes en la jaula de tipo salvaje, es decir, el sustrato mostró una unión preferencial dentro de la nanojaula.
"También se descubrió que estas bionanocajas híbridas eran muy estables, lo que sugiere que podrían usarse como catalizadores viables en aplicaciones industriales", concluye el profesor Ueno. El diseño actual basado en la estructura de la investigación del sitio de unión de iones metálicos podría avanzar para crear nuevos mutantes de ferritina con absorción selectiva de moléculas huésped específicas, para diversas aplicaciones catalíticas en la industria química y farmacéutica. Jaulas de proteínas para el diseño de diversas reacciones catalíticas