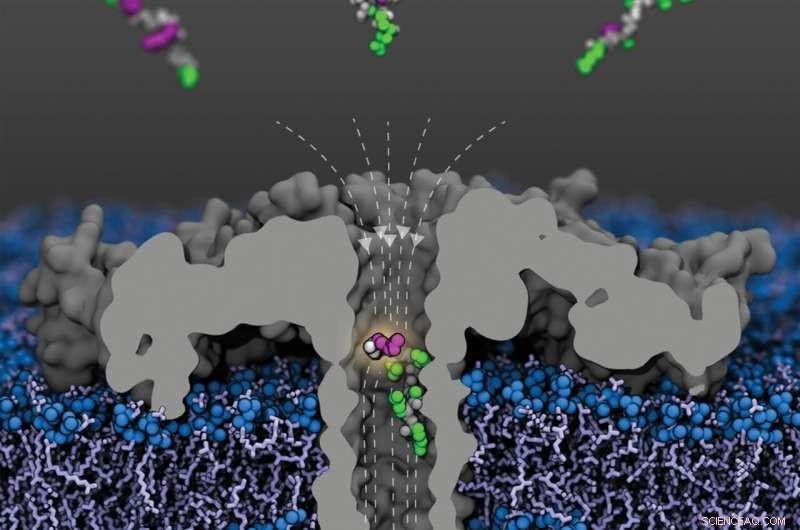
Vista recortada del poro de aerolisina modificado (R220S) (gris) con líneas de campo (discontinuas) en una membrana lipídica. Del compartimento superior llegan fragmentos de proteína histona 4 humana acetilados en varios residuos de lisina; se muestra un fragmento acetilado en lisina-8 dentro del poro. Los esqueletos peptídicos se muestran en gris, las cadenas laterales no modificadas en verde y las lisinas acetiladas en púrpura. Crédito:Sarthak Kumar, Universidad de Illinois en Urbana-Champaign
Los cambios conocidos como modificaciones epigenéticas juegan un papel importante en el desarrollo del cáncer. Ser capaz de analizarlos de manera rápida y confiable podría contribuir significativamente al desarrollo posterior de la terapia personalizada. Un equipo de investigación del Instituto de Fisiología de la Universidad de Freiburg ha logrado caracterizar los cambios químicos en las proteínas que son típicos de las modificaciones epigenéticas mediante el análisis de nanoporos. Los investigadores han publicado los resultados de su investigación en el Journal of the American Chemical Society (JACS ).
En los últimos años, los nanoporos se han convertido en una herramienta ampliamente aplicable para el análisis de moléculas. Debido a sus propiedades especiales, permiten analizar la estructura de las moléculas en fracciones de segundo:como proteínas dispuestas cilíndricamente, los nanoporos forman pequeños canales de solo unas pocas millonésimas de milímetro (nanómetro) de diámetro que pueden incrustarse en biomembranas.
"Para los experimentos, aplicamos un voltaje constante a través de la membrana para que los iones del medio circundante fluyan a través del poro. Esto crea una corriente eléctrica constante y medible con precisión", explica el Prof. Dr. Jan C. Behrends de la Facultad de Medicina. en la Universidad de Friburgo, en cuyo laboratorio tuvieron lugar los experimentos ahora publicados. Sin embargo, cuando una molécula migra al poro, la corriente se bloquea:cuanto más grande es la molécula, más fuertemente se bloquea también.
Una proteína en el punto de mira de la investigación:H4
En el contexto de los experimentos ahora publicados, los científicos de Friburgo se dedicaron a la investigación de la llamada proteína histona H4. Esta proteína está firmemente asociada con el ADN en todas las células con núcleo y es uno de los objetivos mejor investigados de las modificaciones epigenéticas. Una región en el extremo N-terminal de la proteína se ve particularmente afectada por estas modificaciones.
"La secuencia de proteínas allí contiene el aminoácido lisina varias veces", explica Behrends. Los grupos acetilo o metilo, por ejemplo, se pueden unir a estas lisinas, que se denominan K8, K12 y K16 según su posición en la cadena proteica, como parte de modificaciones epigenéticas. Qué modificación química tiene lugar en qué posición de lisina es definitivamente de importancia médica, como señala el fisiólogo de Friburgo. "La acetilación en K16, por ejemplo, es importante para el desarrollo humano, mientras que la metilación en K12 juega un papel en el desarrollo de algunos tumores de próstata y pulmón, según los últimos resultados del Centro Médico de la Universidad de Freiburg".
Detectar cambios con la ayuda de un nanoporo
En sus experimentos, Behrends y su equipo ahora pudieron distinguir claramente fragmentos H4 con o sin acetilación, así como fragmentos con una, dos o tres acetilaciones. Además, consiguieron demostrar que el nanoporo que utilizaron también era sensible al sitio de acetilación:los fragmentos de histonas con un grupo acetilo en K8 bloqueaban la corriente a través del poro con más fuerza que los acetilados en K12, y estos a su vez con más fuerza que aquellos con una acetilación K16.
"Este tipo de sensibilidad es sorprendente porque estos fragmentos son idénticos en términos de masa y volumen total", dice Behrends. Por lo tanto, la corriente de poro parece ser sensible no solo al tamaño, sino también a la forma de la molécula. Era igualmente fácil distinguir entre las diferentes variantes de fragmentos de histonas doblemente acetilados (K8 y K12, K8 y K16, y K12 y K16) nuevamente, a pesar de la masa idéntica. Los fragmentos de H4 metilados en diferentes grados y en diferentes posiciones también bloquearon la corriente a través del poro en diferentes grados, aunque no tan claramente como las variantes acetiladas.
"Hemos podido mostrar por primera vez a través de nuestros experimentos que el análisis de nanoporos nos permite distinguir moléculas no solo por su tamaño, sino también por su forma", dice el líder del estudio Behrends. Las simulaciones de dinámica molecular realizadas por el grupo de investigación dirigido por Aleksei Aksimentiev de la Universidad de Illinois en los EE. UU., también involucrado en el estudio, muestran que un campo eléctrico altamente heterogéneo dentro del poro juega un papel clave en este efecto.
Visión de futuro:diagnóstico médico optimizado
Si bien la secuenciación de ADN utilizando nanoporos ya está establecida y comercializada, el desarrollo del análisis de proteínas basado en nanoporos apenas comienza, dice Behrends. "La dificultad con la secuenciación de proteínas es que estas son moléculas con patrones de carga muy no uniformes". Mientras que el ADN, que tiene carga negativa, migra direccionalmente en el campo eléctrico y, por lo tanto, puede ser arrastrado a través del poro base por base, las proteínas consisten en bloques de construcción hechos de aminoácidos con diferentes cargas. Como resultado, no es posible el movimiento dirigido en el campo eléctrico y el "barrido" de aminoácido por aminoácido. Por lo tanto, los científicos de Friburgo se basaron en un enfoque diferente para sus experimentos. En lugar de un poro con una constricción corta, como se usa en la secuenciación del ADN, usaron un poro hecho a medida con una especie de trampa molecular. "Esto permitió capturar todo el fragmento de proteína a la vez", dice Behrends.
Todavía no está claro hasta qué tamaño de fragmento se puede utilizar este tipo de análisis. Sin embargo, experimentos adicionales muestran que el método también será adecuado para el análisis de los fragmentos H4 utilizados anteriormente en la investigación epigenética. Estos contienen 14 aminoácidos en lugar de los diez utilizados aquí, y actualmente se investigan modificaciones epigenéticas con espectrometría de masas en tándem, una técnica muy elaborada. Los investigadores esperan que los nanoporos hagan que el análisis sea mucho más simple, rápido y rentable, y que se pueda realizar cerca del paciente.
El desarrollo adicional del análisis de nanoporos de proteínas para el diagnóstico médico y su implementación en productos y servicios concretos también es uno de los proyectos centrales del recientemente aprobado BMBF Cluster4Future nanodiagBW, que Behrends dirige junto con el Prof. Dr. Felix von Stetten de Hahn- Schickard-Gesellschaft, que es el líder de este proyecto. Los nanoporos pueden identificar los aminoácidos en las proteínas, el primer paso para la secuenciación