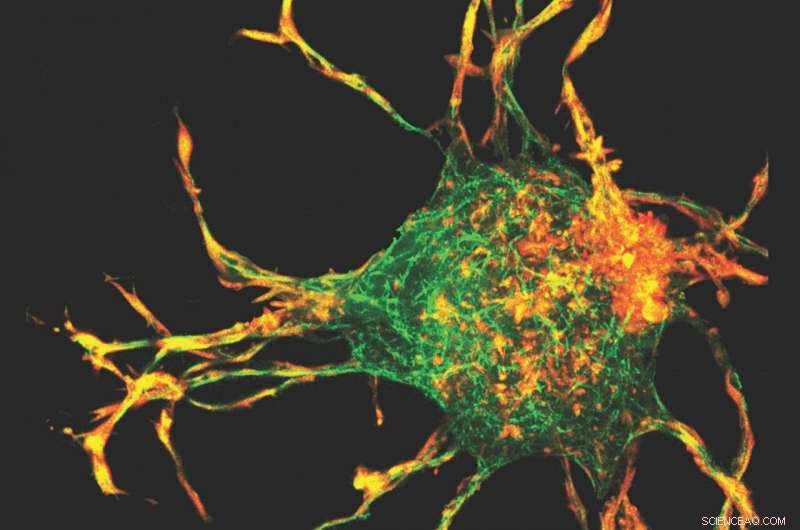
Los investigadores utilizaron una técnica de mapeo 3D, la primera vez que se aplicó al colágeno, junto con un modelo computacional para calcular los campos de tensión y tensión 3D creados por las protuberancias de las células. Crédito:Imagen de cortesía
Cuando tenemos una herida en la piel las células de nuestro cuerpo se movilizan rápidamente para repararlo. Si bien se sabe cómo las células curan las heridas y cómo se forman las cicatrices, un equipo dirigido por investigadores de la Universidad de Washington en St. Louis ha determinado por primera vez cómo comienza el proceso, que puede proporcionar una nueva perspectiva sobre la cicatrización de heridas, fibrosis y metástasis del cáncer.
El equipo, dirigido por Delaram Shakiba, un becario postdoctoral del Centro de Ciencia y Tecnología de NSF para Mecanobiología de Ingeniería (CEMB) en la Escuela de Ingeniería McKelvey, descubrió la forma en que los fibroblastos, o células comunes en el tejido conectivo, interactuar con la matriz extracelular, que proporciona soporte estructural, así como señales bioquímicas y biomecánicas a las células. El equipo descubrió un proceso recursivo que ocurre entre las células y su entorno, así como estructuras en las células que antes se desconocían.
Los resultados de la investigación se publicaron en ACS Nano el 28 de julio. Los autores principales del artículo son Guy Genin, el Profesor Harold y Kathleen Faught de Ingeniería Mecánica en la Escuela de Ingeniería McKelvey, y Elliot Elson, profesor emérito de bioquímica y biofísica molecular de la Facultad de Medicina.
"Esfuerzos clínicos para prevenir la progresión de enfermedades fibrocontráctiles, como cicatrices y fibrosis, han fracasado en gran medida, en parte porque los mecanismos que utilizan las células para interactuar con las fibras proteicas que las rodean no están claros, ", Dijo Shakiba." Descubrimos que los fibroblastos utilizan mecanismos completamente diferentes en las etapas tempranas, y creo que las más tratables, de estas interacciones, y que, por lo tanto, sus respuestas a las drogas pueden ser opuestas a las que serían en las etapas posteriores ".
Genin, quien es el codirector del CEMB, dijo que el proceso ha obstaculizado a los investigadores de mecanobiología durante algún tiempo.
"Los investigadores en el campo de la mecanobiología pensaron que las células extraían el colágeno de la matriz extracelular extendiéndose con protuberancias largas, agarrándolo y tirando de él hacia atrás, "Dijo Genin." Descubrimos que este no era el caso. Una célula tiene que abrirse paso a través del colágeno primero, luego, en lugar de agarrar, esencialmente dispara pelos diminutos, o filopodia, fuera de los lados de sus brazos, extrae colágeno de esa manera, luego se retrae ".
Ahora que entienden este proceso, Genin dijo, pueden controlar la forma que toma una celda.
"Con nuestros colegas de CEMB en la Universidad de Pennsylvania, pudimos validar algunos modelos matemáticos para pasar por el proceso de ingeniería, y ahora tenemos las reglas básicas que siguen las celdas, ", dijo." Ahora podemos comenzar a diseñar estímulos específicos para hacer que una célula se comporte de cierta manera en la construcción de una estructura de tejido ".
Los investigadores descubrieron que podían controlar la forma celular de dos formas:primero, controlando los límites a su alrededor, y segundo, inhibiendo o regulando al alza proteínas particulares implicadas en la remodelación del colágeno.
Los fibroblastos juntan los bordes de una herida, haciendo que se contraiga o se cierre. El colágeno en las células luego remodela la matriz extracelular para cerrar completamente la herida. Aquí es donde entra en juego la mecanobiología.
"Existe un equilibrio entre la tensión y la compresión dentro de una célula que está recién expuesta a proteínas fibrosas, "Genin dijo." Hay tensión en los cables de actina, y jugando con ese equilibrio, podemos hacer que estas protuberancias crezcan extremadamente largas, ", Dijo Genin." Podemos detener la remodelación o podemos aumentarla ".
El equipo utilizó una técnica de mapeo en 3-D, la primera vez que se aplicó al colágeno, junto con un modelo computacional para calcular los campos de tensión y tensión en 3D creados por las protuberancias de las células. A medida que las células acumulaban colágeno, La remodelación impulsada por la tensión y la alineación de las fibras de colágeno condujeron a la formación de tractos de colágeno. Esto requiere interacciones cooperativas entre células, a través del cual las células pueden interactuar mecánicamente.
"Nuevos métodos de microscopía, La ingeniería de tejidos y el modelado biomecánico mejoran en gran medida nuestra comprensión de los mecanismos mediante los cuales las células modifican y reparan los tejidos que pueblan. "Dijo Elson." Las estructuras celulares fibrosas generan y guían fuerzas que comprimen y reorientan su entorno fibroso extracelular. Esto plantea nuevas preguntas sobre los mecanismos moleculares de estas funciones y cómo las células regulan las fuerzas que ejercen y cómo gobiernan el grado de deformación de la matriz ".
"La cicatrización de heridas es un gran ejemplo de cómo estos procesos son importantes desde el punto de vista fisiológico, ", Dijo Genin." Podremos obtener información sobre cómo entrenar a las células para que no compacten excesivamente el colágeno a su alrededor ".