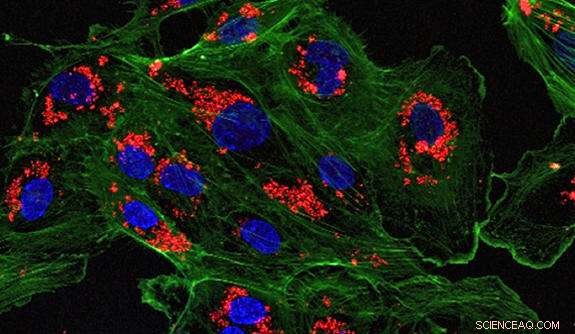
Una imagen microscópica de células endoteliales tratadas con nanopartículas cargadas de fármaco. Crédito:Laboratorio Saltzman
Usando nanopartículas, Los investigadores de Yale han desarrollado un sistema de administración de fármacos que podría reducir las complicaciones del trasplante de órganos al ocultar el tejido donado al sistema inmunológico del receptor.
Alrededor de 25, Cada año se realizan 000 trasplantes de órganos en los EE. UU. A pesar de los importantes avances en el campo, El rechazo de órganos a corto y largo plazo todavía representa un riesgo (las tasas de rechazo varían según el tipo de órgano). El riesgo de rechazo es aún mayor cuando el donante ha fallecido, debido al daño de órganos.
Células T, los glóbulos blancos que identifican y atacan cuerpos extraños, son uno de los principales culpables del rechazo de órganos. El más potente de estos, conocidas como células T de memoria efectora, son activados por un grupo de proteínas conocidas como antígenos leucocitarios humanos (HLA) en la superficie de las células endoteliales que recubren los vasos sanguíneos del órgano donado. Los investigadores pueden silenciar las proteínas con pequeños ARN interferentes (ARNip), un ARN bicatenario que dificulta la expresión de genes diana. Cuando se entrega de forma convencional, sin embargo, los efectos del ARNip duran solo unos días. Un órgano trasplantado de un donante fallecido generalmente necesita semanas para "sanar" y reducir el riesgo de rechazo. El ARNip también puede causar efectos secundarios en las células endoteliales de otros órganos, que no necesitan tratamiento, cuando se administra a todo el cuerpo.
Para dar al ARNip más poder de permanencia, Los investigadores desarrollaron un sistema de administración de fármacos en el que las nanopartículas a base de polímeros transportan ARNip al sitio del injerto y liberan lentamente el fármaco. También desarrollaron métodos para introducir las nanopartículas en el órgano del donante antes de trasplantarlo. para que solo se trate el órgano, no todo el cuerpo. Los resultados de su trabajo se publican en la revista Comunicaciones de la naturaleza .
Las partículas, fabricadas en el laboratorio de Yale de Mark Saltzman, el Profesor de Ingeniería Química y Biomédica de la Fundación Goizueta — se puede ajustar para propiedades específicas. Saltzman, quien también es miembro del Yale Cancer Center, dijo que estas nanopartículas fueron diseñadas para tener una ligera carga positiva para interactuar con la carga negativa del ácido nucleico del siRNA. Esta afinidad entre los dos materiales hace que la partícula sea un portador natural del fármaco, a diferencia de las nanopartículas disponibles comercialmente que pueden contener solo una cantidad limitada del fármaco.
Para el estudio, los investigadores trataron parte de una arteria humana, de unos pocos milímetros de diámetro, con nanopartículas cargadas de ARNip y lo trasplantaron a la aorta abdominal de un ratón inmunodeficiente inoculado con células T humanas. Los investigadores encontraron que las nanopartículas todavía estaban presentes en el tejido donado y silenciaron significativamente la expresión de las proteínas hasta seis semanas después del trasplante. Adicionalmente, no hubo daño a las células endoteliales de los órganos no seleccionados.
Las primeras semanas después del trasplante son críticas, especialmente cuando el donante de órganos ha fallecido, dijo Jordan Pober, el profesor Bayer de Medicina Traslacional y profesor de inmunobiología, patología, y dermatología en Yale.
"Si retrasamos el inicio de la respuesta de rechazo, debe ser más suave y más fácil de controlar y conducir a un rechazo menos tardío, "dijo Pober, quien es coautor del estudio y también director del programa de inmunología traslacional y humana de Yale.
Centrándose en los trasplantes de riñón (con mucho, el tipo de trasplante de órganos más común que se realiza), Saltzman y Pober están buscando aplicar el sistema de administración a un proceso conocido como perfusión de máquina normotérmica ex vivo. Desarrollado para riñones por colegas de la Universidad de Cambridge, el proceso implica bombear tibio, Glóbulos rojos oxigenados a través de un órgano extraído de un donante fallecido para reparar cualquier daño al órgano antes de implantarlo en el receptor. Los investigadores de Yale planean agregar las nanopartículas a los glóbulos rojos para proporcionar una entrega controlada del ARNip a las células endoteliales del riñón.