
Una nano lámina que puede adoptar varias funciones:un equipo de investigadores del Instituto Max Planck de Coloides e Interfaces y el Instituto Federal Suizo de Tecnología en Lausana (EPFL) generó una nanocapa de carbono a partir de moléculas que se acumulan en paralelo de forma autoorganizada. sobre una superficie de agua y formar una alfombra densa en el proceso. La lámina puede equiparse con funciones para diferentes aplicaciones en ambos lados uniendo los correspondientes apéndices químicos a los extremos de la molécula de partida. La nanocapa se puede ver en un portaobjetos perforado en la imagen del microscopio electrónico de barrido. Crédito:EPFL
(Phys.org) —Los científicos han desarrollado un nanomaterial prometedor que puede adaptarse para su uso en una amplia gama de aplicaciones. Un equipo internacional encabezado por científicos del Instituto Federal Suizo de Tecnología de Lausana (EPFL) y el Instituto Max Planck de Coloides e Interfaces en Potsdam-Golm ha desarrollado un método elegante para producir nanocapas de carbono autoorganizadas y equiparlas químicamente con una gama de funciones. Se cree que tales nanocapas de carbono funcionalizadas son adecuadas para diversas aplicaciones. Por ejemplo, podrían actuar como recubrimientos que hacen que las superficies sean resistentes a los arañazos y repelentes a la suciedad, o como sensores para la detección de cantidades extremadamente pequeñas de sustancias. La conductividad eléctrica de las capas de carbono también las hace adecuadas para su uso como componentes electrónicos en diversas aplicaciones.
En la tecnología del mañana algo inconcebiblemente pequeño bien podría convertirse en un gigante. Los científicos están investigando muchas variantes de nanomateriales, a saber, sustancias con dimensiones en el rango de 100 nanómetros. El prefijo nano proviene de la palabra griega para enano, y se refiere a la mil millonésima parte. Por lo tanto, un nanómetro es una mil millonésima parte de un metro. Los científicos están muy entusiasmados con un material en particular que se presenta en estas dimensiones:las nanocapas de carbono. Estas son capas de átomos de carbono en forma de panal que tienen unos pocos nanómetros de espesor, o incluso menos. Las nanocapas de carbono más delgadas imaginables de este tipo son los grafenos, que constan de una sola capa de carbono.
Para muchas aplicaciones, Sería importante poder equipar estas láminas de carbono ultrafinas con determinados residuos de moléculas químicas, conocidos como grupos funcionales. "Esto solo ha sido posible hasta ahora de manera limitada porque las nanohojas de carbono generalmente solo se pueden preparar a temperaturas extremadamente altas, y, por lo tanto, en condiciones que destruirían inmediatamente tales grupos funcionales, "explica Gerald Brezesinski del Instituto Max Planck de Coloides e Interfaces en Golm cerca de Potsdam. Junto con colegas de su Instituto, Brezesinski ha brindado apoyo a investigadores del Instituto Federal Suizo de Tecnología de Lausana (EPFL) en el desarrollo de un enfoque de síntesis que podría ser de interés en este contexto. Usando este método, nanocapas de carbono, incluidos los grupos funcionales, podría ser accesible a temperaturas considerablemente más bajas que las que se aplican habitualmente en la producción de tales materiales.
Sumergirse profundamente en la bolsa de trucos químicos
Para formar una estructura plana a partir de átomos de carbono, los investigadores suizos desplegaron una serie de trucos. Uno de los principales se refería al compuesto de partida seleccionado, una molécula cuya sección central tiene seis enlaces simples y triples carbono-carbono alternos. Estas secciones consisten exclusivamente en átomos de carbono y son altamente reactivas, ya que también pueden sufrir reacciones químicas a temperaturas más bajas. A diferencia de otros procesos, esto significa que se pueden producir capas delgadas de carbono a partir de estas moléculas a temperatura ambiente.
Usando una configuración de prueba especial, los científicos hicieron que muchas de estas moléculas se alinearan perfectamente en paralelo entre sí en una sola capa autoorganizada, como las cerdas de un cepillo. Sin embargo, había una pequeña diferencia en las cerdas del cepillo:cada una de las cadenas paralelas de moléculas tenía una ligera curva. Como resultado de este arreglo, las secciones ricas en carbono de todas las moléculas se ubicaron al mismo nivel. Cuando los investigadores aplicaron luz ultravioleta a esta configuración, algunos de los triples enlaces se rompieron y, en cambio, se formaron enlaces entre los átomos de carbono de las moléculas vecinas. Debido a que casi todas las cerdas finalmente se unieron con sus cerdas vecinas, Surgió una capa consistente de átomos de carbono:una nanocapa de carbono.
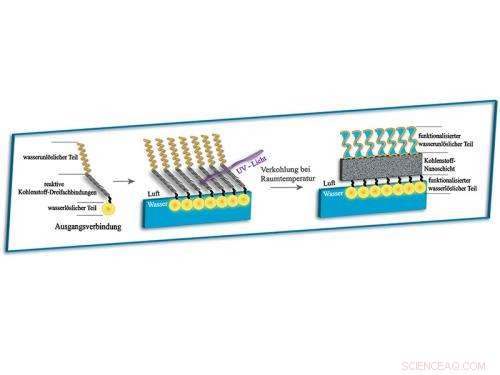
Una nanocapa de carbono autoorganizada:moléculas de cadena con un extremo soluble en agua y otro insoluble se autoorganizan en una superficie de agua como las cerdas de un cepillo. La luz ultravioleta desencadena la reacción química, en el que los triples enlaces de carbono reactivo en la sección media del compuesto de partida se combinan para formar una capa consistente, se carbonizan. Tanto el lado soluble en agua como el insoluble de la nanocapa pueden equiparse químicamente con funciones para diversas aplicaciones. Crédito:EPFL / MPI de coloides e interfaces
Para permitir que todo esto suceda, Los científicos de Lausana claramente tuvieron que profundizar en la caja de los trucos químicos para el diseño del precursor molecular. Para asegurar la disposición paralela de sus moléculas, idearon moléculas similares a los tensioactivos, similares a los que se encuentran en el líquido para lavar platos. Mientras que un extremo de tales moléculas se disuelve bien en agua, el otro no se disuelve en absoluto. Entre estos dos extremos, los científicos colocaron los triples enlaces reactivos.
Cuando pusieron su compuesto en contacto con el agua en este punto, solo un extremo de la molécula se disolvió. Todo el residuo restante era tan insoluble que sobresalía de la superficie al aire. Los investigadores lograron establecer deliberadamente una distancia uniforme entre las cerdas moleculares individuales. En el nivel de los triples enlaces, tenía que ser inferior a 0,4 nanómetros, ya que los átomos de carbono vecinos solo están lo suficientemente cerca entre sí en este caso como para formar nuevos enlaces entre sí bajo la luz ultravioleta.
Éxito del proceso de síntesis confirmado por análisis altamente especializados
Para los científicos era importante comprender cómo se veía realmente la capa molecular a lo largo del límite agua-aire, y cómo cambió en el curso de la reacción. Aquí entraron en juego métodos especiales, que forman parte del repertorio de Gerald Brezesinski y su Grupo de Investigación en el Instituto Max Planck de Coloides e Interfaces en Potsdam. Por ejemplo, Para detectar la posición de los átomos relevantes en la capa límite y, por lo tanto, también la disposición exacta de las moléculas iniciales, los investigadores utilizaron haces de rayos X de alta energía del sincrotrón DESY en Hamburgo. Las formas en que estos rayos se dispersaron o se reflejaron en la capa de muestra delgada como una oblea finalmente proporcionaron a Gerald Brezesinski y su colega Cristina Stefaniu, que ahora trabaja en la Universidad de Potsdam, con información sobre la disposición exacta de las moléculas iniciales.
Con la ayuda de la espectroscopia de reflexión-absorción infrarroja, Posteriormente, los científicos lograron rastrear la reacción real durante la irradiación ultravioleta. Para hacer esto, midieron cómo la señal característica de los triples enlaces declinaba continuamente durante el transcurso de la reacción. Aquí fue útil una técnica muy especial utilizada por los investigadores en Potsdam. Las perturbadoras influencias de las moléculas de agua presentes solo podrían enmascararse con la ayuda de esta técnica. "Hay sólo unos pocos grupos de investigación en el mundo que pueden hacer visible este tipo de espectroscopía infrarroja en tales capas, "subraya Gerald Brezesinski.
Las técnicas especiales utilizadas por los investigadores de Max Planck con sede en Potsdam también resultaron útiles para caracterizar el producto resultante. Estos incluyeron, por ejemplo, la microscopía de ángulo de Brewster, que se desarrolló hace unos 20 años en el Instituto Max Planck de Química Biofísica en Göttingen. Con la ayuda de este microscopio, los investigadores pudieron demostrar que el producto era una capa lisa muy homogénea, que es un total de dos nanómetros de espesor - y, por lo tanto, en realidad, una nanocapa de carbono.
Gerald Brezesinski del Instituto Max Planck de Coloides e Interfaces en Potsdam también se mostró satisfecho con este éxito:"Esto significa que en realidad es posible diseñar moléculas similares a los surfactantes de una manera que permita su uso en la síntesis de una capa de carbono en un superficie del agua. Pudimos probar esto con la ayuda de nuestros métodos ".
Punto de partida de las "nanocapas de carbono funcionales"
Al final del proceso de síntesis, los extremos de las moléculas de partida aún sobresalían de la nanocapa:el extremo soluble en agua en un lado y el extremo insoluble en el otro. Este factor en particular es extremadamente importante para los investigadores, ya que crea la posibilidad de unir grupos químicos en el extremo antes de la síntesis que darán a la nanocapa de carbono subsiguiente una función especial. Los apéndices químicos resistirían el proceso de producción suave sin daños, y también se conservaría en la nanocapa de carbono resultante.
De este modo, por ejemplo, sería posible anclar grupos químicos en un lado que luego soportarían la conexión a determinadas superficies de vidrio o metal. También se podrían unir grupos al otro lado que harían que la capa repele la suciedad. La propia capa de carbono también haría que la superficie fuera muy resistente a los arañazos. Los nanosensores químicos también podrían construirse a partir de capas tan delgadas como una oblea. Para tal fin, Los grupos químicos podrían integrarse en las moléculas de partida que luego aseguran la interacción con la sustancia o grupo de sustancias a medir. La alta conductividad eléctrica de las nanocapas de carbono podría utilizarse entonces para la transmisión de las señales de medición. Por lo tanto, los investigadores de Lausana y Potsdam esperan que su proceso innovador para la producción de nanocapas de carbono autoorganizadas y funcionales allane el camino para un gran número de nuevas aplicaciones interesantes.