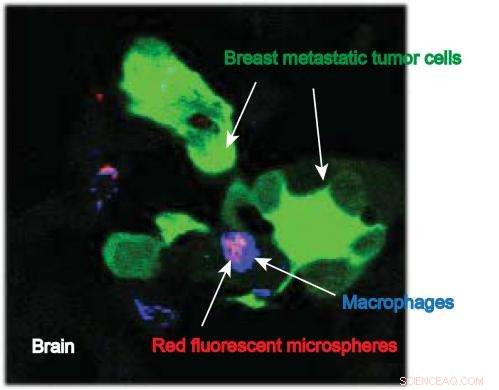
Esta imagen de Susan Clare, investigadora de la Facultad de Medicina de IU, muestra macrófagos que llevan nanopartículas (con un tinte fluorescente adherido) en el sitio de las células metastásicas del tumor de mama en el cerebro. Crédito:Susan Clare, MARYLAND., Doctor.
Un cirujano de cáncer de mama de la Facultad de Medicina de la Universidad de Indiana está realizando una investigación que utilizará vidrio, oro, nanotecnología y mitología griega con la esperanza de vencer el cáncer de mama que ha hecho metástasis en el cerebro.
Susan E. Clare, MARYLAND., Doctor., profesor asociado de cirugía en la Facultad de Medicina de IU, es el investigador principal iniciador por $ 573, 000 subvención del Departamento de Defensa que le permitirá explorar un nuevo enfoque para administrar la terapia a las metástasis cerebrales del cáncer de mama primario.
Como hicieron los griegos de antaño, El Dr. Clare espera entregar secretamente "guerreros" a la fortaleza enemiga, en este caso un tumor cerebral metastásico. Su investigación explorará el uso de una célula del sistema inmunológico del cuerpo para administrar quimioterapia directamente a las metástasis cerebrales. El fármaco u otro terapéutico está unido a las nanoesferas, que se llevan dentro de la célula inmunitaria, tanto como los soldados fueron llevados dentro del Caballo de Troya. Las células inmunitarias viajan por el torrente sanguíneo y liberan el fármaco cuando llega al sitio del tumor.
Los dos tipos de cáncer de mama que más comúnmente hacen metástasis en el cerebro son HER2 positivo y triple negativo. No existe un tratamiento dirigido específicamente para tratar los tumores metastásicos triple negativos. pero el lapatinib es un tratamiento estándar para el cáncer HER2 positivo que se ha diseminado a otras partes del cuerpo.
"El problema de casi todas las drogas, y los medicamentos dirigidos a HER2 no son una excepción, es que la barrera hematoencefálica es un impedimento significativo para administrar terapias en concentraciones que puedan ser efectivas, "Dijo el Dr. Clare. Ese problema biológico hizo que el Dr. Clare explorara otros métodos para administrar medicamentos a los tumores cerebrales metastásicos.
Usando nanopartículas llamadas "nanocapas, "desarrollado por Naomi J. Halas, Doctor., D.Sc., director del Laboratorio de Nanofotónica de la Universidad de Rice, El Dr. Clare espera apuntar a los tumores cerebrales con lapatinib en una dosis suficiente para cerrar la vía de señalización necesaria para que las células cancerosas proliferen.
En un artículo de julio en la revista Nanotecnología del cáncer , Drs. Clare, Halas y sus colegas demostraron que las células inmunes que transportan las nanopartículas pudieron cruzar la barrera hematoencefálica y dirigirse a metástasis cerebrales en un modelo experimental de ratón.
Primero, Se recolecta un componente de los glóbulos blancos llamados macrófagos, células versátiles que inician una respuesta inmune después de infiltrarse en células anormales (cancerosas). Las nanopartículas son ingeridas por los macrófagos, que luego se liberan en el torrente sanguíneo. El Dr. Clare dijo que los macrófagos se sienten atraídos por las metástasis por los quimioatrayentes, que son sustancias químicas producidas por el tumor.
Estas nanopartículas se encuentran en estudios clínicos de fase I para el tratamiento del cáncer de cabeza y cuello, cáncer de próstata avanzado y cáncer de pulmón a través de Nanospectra Biosciences, con sede en Houston, Texas. Debido a que se pensaba que la barrera hematoencefálica era un impedimento significativo para el parto, la efectividad del tratamiento para las metástasis cerebrales no se incluyó en las pruebas iniciales. La subvención del Departamento de Defensa del Dr. Clare permitirá la investigación en tres áreas clave.
El primer objetivo es mostrar que los medicamentos de quimioterapia pueden atarse a las nanopartículas y liberarse a voluntad en el lugar apropiado del cerebro. Dijo el Dr. Clare. Liberar "a voluntad" es fundamental en el proceso.
"La droga se libera de la partícula al hacer brillar un láser sobre la partícula, ", dijo." La droga se transporta entre dos piezas de ADN que están cargadas negativamente. Cuando se expone a la luz láser, los electrones pasan de la nanopartícula al ADN, lo que le permite liberar la droga ".
Los macrófagos llevan la nanopartícula directamente a las células cancerosas, así que cuando se libera la droga, es exactamente donde debe estar para difundirse al tumor e interrumpir la actividad celular de las células metastásicas.
Tan simple como suena, No lo es.
La nanopartícula es una bola de sílice cubierta de oro, que ha demostrado ser no tóxico en extensos, estudios científicos a largo plazo. El grosor de la capa de oro determina en qué parte del espectro de luz se absorbe la luz láser. Para una máxima penetración en los tejidos, las nanopartículas deberían absorber luz en el infrarrojo cercano. Las nanopartículas desarrolladas por el Dr. Halas hacen precisamente eso.
Sin embargo, el hueso del cráneo presenta un desafío adicional para entregar suficiente potencia láser a la nanopartícula. Aumentar la potencia del láser no es la respuesta porque quemará la piel. Hay muchas variables en el enigma, pero el Dr. Clare ha contratado a Keith Stantz, Doctor., profesor asistente adjunto de radiología en el Instituto de Ciencias de Imágenes Biomédicas de Indiana, y Jacqueline A. Johnson, Doctor., profesor asociado en el Instituto Espacial de la Universidad de Tennessee, ambos son expertos en láseres de nanosegundos y femtosegundos. El equipo cree que tiene una solución al desafío de la energía y la probará en modelos de ratón.
"Esa es una gran pieza del rompecabezas, "Dijo el Dr. Clare." El oro se usa como caparazón para la partícula debido a sus propiedades físicas. Cálculos precisos para el espesor del oro, la profundidad ideal de penetración y la potencia del láser eran desafíos que debían resolverse antes de poder estudiar la eficacia del sistema de administración del fármaco ".