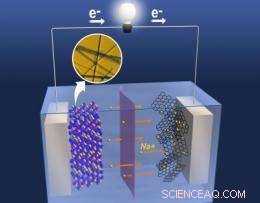
La nanoestructura uniforme del óxido de manganeso tratado térmicamente proporciona túneles para que fluyan los iones de sodio, mejorando el rendimiento de los electrodos. Crédito:PNNL
(PhysOrg.com) - Al agregar la cantidad correcta de calor, Los investigadores han desarrollado un método que mejora la capacidad eléctrica y la vida útil de recarga de las baterías recargables de iones de sodio. lo que podría ser una alternativa más económica para usos a gran escala, como almacenar energía en la red eléctrica.
Para conectar fuentes de energía solar y eólica a la red eléctrica, Los administradores de la red requieren baterías que puedan almacenar grandes cantidades de energía creada en la fuente. Las baterías recargables de iones de litio, comunes en la electrónica de consumo y los vehículos eléctricos, funcionan bien, pero son demasiado caras para un uso generalizado en la red porque se necesitarán muchas baterías, y probablemente necesitarán ser grandes. El sodio es la siguiente mejor opción, pero las baterías de sodio-azufre actualmente en uso funcionan a temperaturas superiores a 300 grados Celsius, o tres veces la temperatura del agua hirviendo, haciéndolos menos eficientes energéticamente y seguros que las baterías que funcionan a temperatura ambiente.
Los desarrolladores de baterías quieren lo mejor de ambos mundos:usar sodio económico y usar el tipo de electrodos que se encuentran en las recargables de litio. Un equipo de científicos del Laboratorio Nacional del Noroeste del Pacífico del Departamento de Energía e investigadores visitantes de la Universidad de Wuhan en Wuhan, China usó nanomateriales para fabricar electrodos que pueden funcionar con sodio, informaron el 3 de junio en línea en la revista Materiales avanzados .
"La batería de iones de sodio funciona a temperatura ambiente y utiliza iones de sodio, un ingrediente en la sal para cocinar. Entonces será mucho más barato y seguro, "dijo el químico de PNNL Jun Liu, quien codirigió el estudio con el químico de la Universidad de Wuhan, Yuliang Cao.
Los electrodos de los recargables de litio que interesan a los investigadores están hechos de óxido de manganeso. Los átomos de este óxido metálico forman muchos agujeros y túneles por los que viajan los iones de litio cuando las baterías se cargan o se utilizan. El libre movimiento de los iones de litio permite que la batería retenga electricidad o la libere en una corriente. Pero simplemente reemplazar los iones de litio con iones de sodio es problemático:los iones de sodio son un 70 por ciento más grandes que los iones de litio y tampoco caben en las grietas.
Para encontrar una manera de hacer agujeros más grandes en el óxido de manganeso, Los investigadores de PNNL fueron mucho más pequeños. Recurrieron a los nanomateriales, materiales fabricados en la escala del tamaño de un nanómetro, o aproximadamente un millón de veces más delgado que una moneda de diez centavos, que tienen propiedades sorprendentes debido a su pequeñez. Por ejemplo, las distancias cortas que los iones de sodio tienen que viajar en los nanocables podrían hacer que el óxido de manganeso sea un mejor electrodo en formas no relacionadas con el tamaño de los túneles.
Para explorar, el equipo mezcló dos tipos diferentes de bloques de construcción atómicos de óxido de manganeso:uno cuyos átomos se organizan en pirámides, y otro cuyos átomos forman un octaedro, una estructura en forma de diamante de dos pirámides pegadas en sus bases. Esperaban que el material final tuviera grandes túneles en forma de S y túneles más pequeños de cinco lados a través de los cuales pudieran fluir los iones.
Después de mezclar, el equipo trató los materiales con temperaturas que oscilan entre 450 y 900 grados Celsius, luego examinó los materiales y probó qué tratamiento funcionaba mejor. Usando un microscopio electrónico de barrido, el equipo descubrió que las diferentes temperaturas creaban material de diferente calidad. El tratamiento del óxido de manganeso a 750 grados Celsius creó los mejores cristales:demasiado bajo y los cristales parecían escamosos, demasiado alto y los cristales se convirtieron en placas planas más grandes.
Acercándonos aún más con un microscopio electrónico de transmisión en EMSL, Laboratorio de Ciencias Moleculares Ambientales del DOE en el campus de PNNL, el equipo vio que el óxido de manganeso calentado a 600 grados tenía marcas de viruela en los nanocables que podían impedir los iones de sodio, pero los alambres tratados a 750 grados parecían uniformes y muy cristalinos.
Pero incluso el material más atractivo es solo una fachada si no funciona bien. Para saber si estuvo a la altura de su buen aspecto, el equipo de PNNL-Wuhan sumergió el material del electrodo en electrolito, el líquido que contiene iones de sodio que ayudará a que los electrodos de óxido de manganeso formen una corriente. Luego cargaron y descargaron las celdas de la batería experimental repetidamente.
El equipo midió la capacidad máxima a 128 miliamperios hora por gramo de material de electrodo a medida que se descargaba la celda de la batería experimental. Este resultado superó los anteriores tomados por otros investigadores, uno de los cuales alcanzó una capacidad máxima de 80 miliamperios hora por gramo para electrodos hechos de óxido de manganeso pero con un método de producción diferente. Los investigadores creen que la menor capacidad se debe a que los iones de sodio causan cambios estructurales en ese óxido de manganeso que no ocurren o ocurren con menos frecuencia en el material de tamaño nanométrico tratado térmicamente.
Además de alta capacidad, el material resistió bien los ciclos de carga y descarga, como ocurriría en el uso del consumidor. De nuevo, el material tratado a 750 grados Celsius funcionó mejor:después de 100 ciclos de carga-descarga, perdió sólo el 7 por ciento de su capacidad. El material tratado a 600 Celsius o 900 Celsius perdió alrededor del 37 por ciento y el 25 por ciento, respectivamente.
Incluso después de la 1, 000 ciclos, la capacidad de los electrodos tratados con 750 grados Celsius solo se redujo alrededor del 23 por ciento. Los investigadores pensaron que el material funcionó muy bien, reteniendo el 77 por ciento de su capacidad inicial.
Último, el equipo cargó la celda experimental a diferentes velocidades para determinar qué tan rápido podría absorber electricidad. El equipo descubrió que cuanto más rápido lo cargaban, menos electricidad podría contener. Esto sugirió al equipo que la velocidad con la que los iones de sodio podrían difundirse en el óxido de manganeso limitaba la capacidad de la celda de la batería, cuando se cargaba rápido, los iones de sodio no podían entrar en los túneles lo suficientemente rápido como para llenarlos.
Para compensar los lentos iones de sodio, los investigadores sugieren que en el futuro fabricarán nanocables aún más pequeños para acelerar la carga y descarga. Las baterías de la red necesitan una carga rápida para que puedan recolectar la mayor cantidad posible de energía procedente de fuentes renovables. Y necesitan descargar rápidamente cuando la demanda se dispara cuando los consumidores encienden sus aires acondicionados y televisores, y enchufar sus vehículos eléctricos en casa.
Este tipo de baterías de alto rendimiento podrían eliminar el calor de una red de energía eléctrica ya gravada.