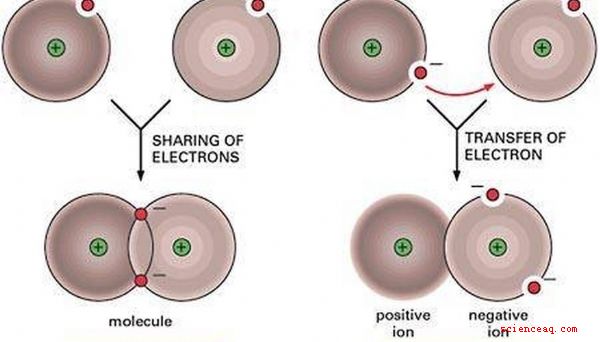
Un enlace molecular o covalente se forma cuando los átomos se unen al compartir pares de electrones. Este intercambio puede ocurrir de átomo a átomo, o de un átomo a otro enlace molecular.
Tipos
Hay dos tipos de enlaces moleculares: enlaces polares y enlaces no polares. En los enlaces polares, el enlace molecular se comparte de manera desigual entre los átomos; en los enlaces no polares, los electrones se comparten de manera uniforme entre los dos átomos.
Características
Los enlaces moleculares se clasifican como enlaces singulares o enlaces múltiples. Los enlaces moleculares forman enlaces simples, donde dos átomos solo comparten un par de electrones.
Enlaces moleculares múltiples
El enlace doble consta de dos pares de electrones, un enlace triple consta de tres pares y los enlaces cuádruples comparten cuatro pares de electrones; también hay enlaces quíntuples y sextuples.
Enlace covalente coordinado
En un enlace covalente coordinado, se forma un enlace covalente o molecular cuando solo uno de los dos átomos es responsable de proporcionar ambos electrones. Enlace disulfuro
Un enlace disulfuro es un enlace molecular que se forma cuando dos átomos de sulfuro se unen para formar cadenas de polipéptidos en las proteínas.
Enlaces de alta energía
Liberación de enlaces de alta energía altos niveles de energía cuando el enlace sufre hidrólisis.
Enlaces iónicos
Los enlaces iónicos provocan la transferencia de electrones de un átomo a otro, dejándolo con una carga negativa.