En la mayoría de las reacciones químicas industriales, los catalizadores se combinan con los materiales de partida y los acompañan a través de etapas intermedias hasta llegar al producto. En química, esta vía se conoce como mecanismo de reacción, y es una especie de caja negra:nadie sabe lo que sucede a nivel molecular al principio.
Si el resultado de la reacción en el laboratorio no cumple con las expectativas, los químicos primero recurren al ensayo y error. En pocas palabras, modifican la reacción hasta que funciona. A veces, sin embargo, vale la pena observar más de cerca el mecanismo de reacción, como lo demuestra la Dra. Nora Jannsen del Instituto Leibniz de Catálisis en Rostock utilizando un modelo de reacción.
Recientemente publicó sus hallazgos, que obtuvo como parte de su doctorado, en el Journal of the American Chemical Society. .
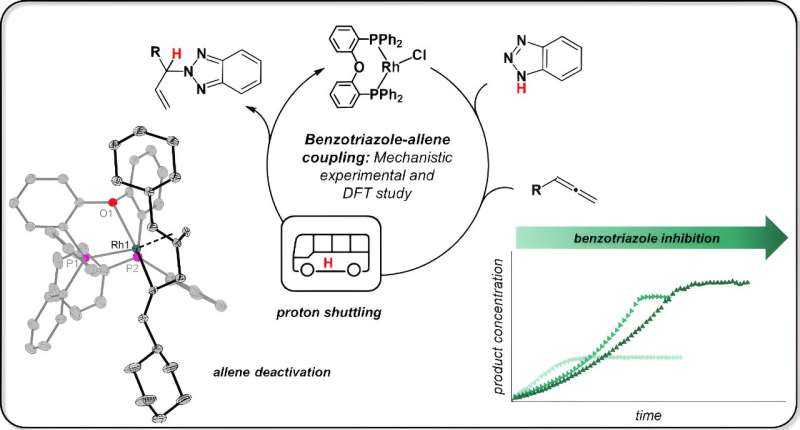
La reacción del modelo no suena espectacular y, sobre todo, extraña al oído del profano, explica Jannsen. "El benzotriazol, normalmente un inhibidor de la corrosión, se convierte en una nueva sustancia con un aleno (aquí el énfasis está en la segunda sílaba) utilizando un catalizador de rodio". Luego se llama alilbenzotriazol y puede usarse en una variedad de síntesis. La reacción fue desarrollada por un grupo de investigación dirigido por el Prof. Breit de la Universidad de Friburgo.
Los colegas de Friburgo lograron vincular con precisión un "grupo funcional" a una posición muy específica en el benzotrialzol. Aquí es donde se encuentra el enlace nitrógeno-hidrógeno (N-H), como explica Jannsen.
Los "grupos funcionales" son importantes como segmentos moleculares porque son responsables del efecto específico, por ejemplo, farmacéutico.
"El equipo de Friburgo quería colocar un grupo de este tipo en el benzotriazol exactamente donde se encuentra el enlace N-H, y para ello el enlace N-H tiene que ceder", continúa Jannsen. Los colegas lograron hacer esto. "Pero no entendieron sobre qué base lo habían logrado".
Eso es desafortunado. Porque sólo con una comprensión de los eventos moleculares se podrá aplicar y optimizar la reacción específicamente en el futuro. Este era el objetivo de la tesis de Jannsen, que defendió con éxito en 2023 en Rostock.
Entonces, ¿cómo funciona tal reacción? Se conocen el comienzo y el final. Lo que también se sabe acerca de esta reacción es que cada átomo de los materiales de partida se encuentra posteriormente en el producto; Los químicos llaman a esto una reacción "atómico-económica". Esto significa que en el transcurso de la reacción, el hidrógeno del enlace N-H debe pasar del benzotriazol al segundo material de partida, el aleno.
Jannsen afirma:"Los científicos de Friburgo pensaban que el catalizador rompe el enlace nitrógeno-hidrógeno, es decir, se produce la llamada adición oxidativa del benzotriazol. Los catalizadores de rodio son conocidos por este tipo de reacción".
Jannsen probó la idea haciendo reaccionar primero el catalizador de rodio con un solo material de partida, el benzotriazol. Aisló muestras de esta reacción para espectroscopia de resonancia magnética nuclear (RMN) y análisis de la estructura cristalina de rayos X. El resultado:"El enlace N-H no se rompe en absoluto. El benzotriazol permanece completamente intacto, sólo se adhiere al catalizador."
El químico descubrió entonces que la segunda sustancia de partida, allen, también se une al catalizador. Y aquí ocurre lo siguiente:"Los dos materiales de partida entran en contacto directo entre sí y el benzotriazol transfiere el átomo de hidrógeno, también conocido como protón, al aleno. El catalizador simplemente mantiene los materiales de partida en su lugar, pero no interviene directamente en este paso."
Posteriormente, Jannsen fundamentó detalladamente esta propuesta utilizando la mecánica cuántica, es decir, modelando teóricamente la vía de reacción.
A Jannsen le sorprendió que el catalizador gestionara todo con tanta sencillez. Para los profanos, puede sonar un poco como un truco químico con una cuerda. En términos técnicos, este proceso es bien conocido y se llama protonación.
Este proceso tenía una ventaja. Jannsen dice:"Curiosamente, las condiciones de reacción para la protonación pueden mejorarse significativamente añadiendo otra fuente de protones". Por ejemplo, logró reducir la temperatura de reacción de 80 °C a temperatura ambiente añadiendo un tipo de cocatalizador.
Jannsen también descubrió que el benzotriazol también puede bloquear el catalizador en determinadas circunstancias. Este es el caso cuando esta sustancia de partida ocupa el catalizador dos veces, de modo que su compañero de reacción, el allen, no puede encontrar un espacio libre en el catalizador.
Esto paraliza la actividad catalítica y conduce a que el catalizador se "consuma". "Probablemente sea útil añadir el material de partida a la reacción de forma sucesiva para que el catalizador entre en menor contacto con él", afirma Jannsen.
Más información: Nora Jannsen et al, Revisión del mecanismo de acoplamiento catalizado por Rh (I) de benzotriazoles y alenos:inhibición de sustrato, transporte de protones y el papel de las especies catiónicas frente a las neutras, Revista de la Sociedad Química Estadounidense (2024). DOI:10.1021/jacs.4c02679
Información de la revista: Revista de la Sociedad Química Estadounidense
Proporcionado por el Instituto Leibniz de Catálisis