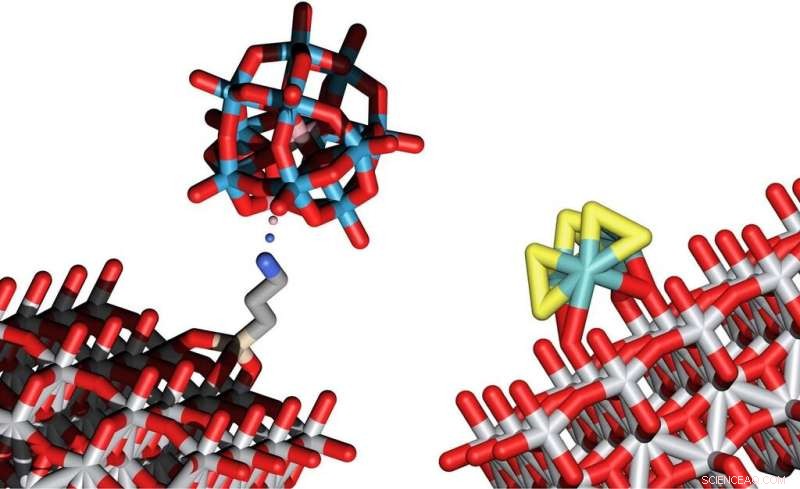
Modelos estructurales de dos cúmulos que permiten la descomposición del agua en O2 y H2 mediante energía lumínica. Crédito:Universidad Tecnológica de Viena
El hidrógeno podría ser una parte importante de nuestro suministro de energía en el futuro:puede almacenarse, transportarse y quemarse según sea necesario. Sin embargo, la mayor parte del hidrógeno disponible en la actualidad es un subproducto de la producción de gas natural, y esto tiene que cambiar por razones de protección climática. La mejor estrategia hasta ahora para producir "hidrógeno verde" respetuoso con el medio ambiente es dividir el agua en hidrógeno y oxígeno utilizando electricidad procedente de fuentes de energía renovables, por ejemplo, células fotovoltaicas.
Sin embargo, sería mucho más fácil si la luz del sol pudiera usarse directamente para dividir el agua. Esto es exactamente lo que ahora están haciendo posibles los nuevos catalizadores, en un proceso llamado "división fotocatalítica del agua". El concepto aún no se utiliza industrialmente. En TU Wien, ahora se han dado pasos importantes en esta dirección:a escala atómica, los científicos han realizado una nueva combinación de catalizadores moleculares y de estado sólido que pueden hacer el trabajo utilizando materiales relativamente económicos.
Interacción de los átomos
"En realidad, para poder dividir el agua con luz, debes resolver dos tareas al mismo tiempo", dice Alexey Cherevan del Instituto de Química de Materiales de TU Wien. "Tenemos que pensar en el oxígeno y en el hidrógeno. Los átomos de oxígeno del agua deben transformarse en O2 moléculas y los iones de hidrógeno restantes, que son solo protones, deben convertirse en moléculas de H2".
Ahora se han encontrado soluciones para ambas tareas. Pequeños grupos inorgánicos que consisten en solo una pequeña cantidad de átomos están anclados en una superficie de estructuras de soporte que absorben la luz, como el óxido de titanio. La combinación de clústeres y soportes de semiconductores cuidadosamente elegidos conducen al comportamiento deseado.
Los clusters responsables de oxidar el oxígeno están formados por cobalto, tungsteno y oxígeno, mientras que los clusters de azufre y molibdeno son especialmente adecuados para crear moléculas de hidrógeno. Los investigadores de TU Wien fueron los primeros en depositar estos grupos en una superficie hecha de óxido de titanio, donde pueden actuar como catalizadores para la división del agua.
"El óxido de titanio es sensible a la luz, eso ya se sabía", dice Alexey Cherevan. "La energía de la luz absorbida conduce a la creación de electrones de movimiento libre y cargas positivas de movimiento libre en el óxido de titanio. Estas cargas permiten que los grupos de átomos que se encuentran en esta superficie faciliten la división del agua en oxígeno e hidrógeno. "
Control preciso, átomo a átomo
"Otros grupos de investigación que trabajan en la división del agua con luz se basan en nanopartículas que pueden adoptar formas y propiedades superficiales muy diferentes", explica Alexey Cherevan. "Los tamaños son difíciles de controlar, los átomos no están dispuestos de la misma manera. Por lo tanto, en este caso, no es posible explicar exactamente cómo se lleva a cabo el proceso de catálisis en detalle". En TU Wien, por otro lado, la estructura exacta de los cúmulos se determina con precisión atómica, lo que permite una comprensión completa del ciclo catalítico.
"Esta es la única forma de obtener retroalimentación sobre de qué depende realmente la eficiencia del proceso", dice Alexey Cherevan. "No queremos confiar simplemente en un enfoque de prueba y error y probar diferentes nanopartículas hasta que encontremos la mejor; queremos descubrir a nivel atómico cuál es realmente el catalizador óptimo".
Ahora que se ha demostrado que los materiales seleccionados son adecuados para dividir el agua, el siguiente paso es ajustar aún más su estructura exacta para lograr eficiencias aún mayores.
Simple y prometedor
"La ventaja decisiva de nuestro método sobre la división del agua por electrólisis es su simplicidad", enfatiza Alexey Cherevan. La producción de hidrógeno eléctrico primero necesita una fuente de energía sostenible, como células fotovoltaicas, posiblemente un dispositivo de almacenamiento de energía eléctrica y una célula de electrólisis. Con todo, esto da como resultado un sistema relativamente complejo que consta de una multitud de materias primas. Para la división fotocatalítica del agua, por otro lado, todo lo que se necesita es una superficie adecuadamente recubierta que esté cubierta por agua e irradiada por el sol.
A largo plazo, este método también podría usarse para producir moléculas más complicadas utilizando el concepto de fotosíntesis artificial. Incluso podría ser posible utilizar la energía de la radiación solar para producir hidrocarburos con dióxido de carbono de la atmósfera y el agua, que luego pueden utilizarse para otras aplicaciones.
Los estudios asociados aparecen en ACS Catalysis y Materiales ACS Au . Superficie del catalizador analizada a resolución atómica