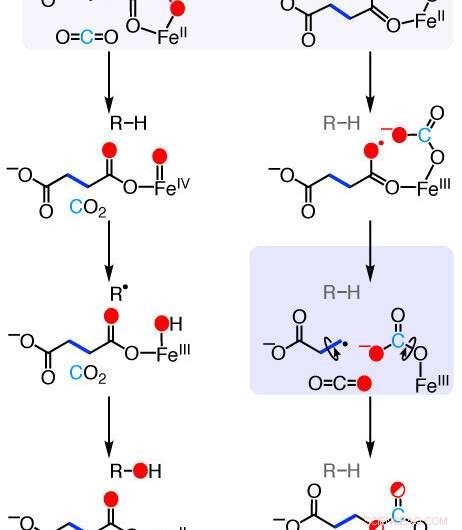
Mecanismos de las reacciones de la enzima formadora de etileno (EFE). Una nueva investigación describe los pasos químicos utilizados por esta enzima natural para convertir un compuesto químico común en etileno, una hormona vegetal importante para la maduración de la fruta y un químico industrial utilizado en la producción de plásticos y textiles. Crédito:Rachelle Copeland, Penn State
Una nueva investigación describe los pasos químicos utilizados por una enzima natural para convertir un compuesto químico común en etileno, una hormona vegetal importante para la maduración de la fruta y un químico industrial utilizado en la producción de plásticos y textiles. Un artículo que describe la investigación de científicos de Penn State aparece en línea el 12 de agosto en la revista. Ciencias .
"Debido a que el etileno es tan importante en la industria manufacturera para fabricar plásticos, disolventes y textiles, es uno de los compuestos más abundantemente producidos en la Tierra, "dijo Rachelle Copeland, un doctorado reciente de Penn State y primer y co-autor correspondiente del artículo. "En la actualidad, el petróleo es nuestra principal fuente de etileno para estos usos. Sin embargo, las plantas y algunos microbios producen etileno de forma natural. Comprender el proceso químico paso a paso utilizado por estas plantas y microbios podría ayudarnos a alejarnos de la producción de etileno a base de petróleo ".
La denominada "enzima formadora de etileno (EFE)" es capaz de transformar un compuesto químico común:2-oxoglutarato, que se encuentra en casi todos los organismos donde juega un papel en el metabolismo, en etileno, pero los investigadores no habían podido caracterizar con precisión el mecanismo empleado por la enzima. La reacción requerida para esta transformación es fundamentalmente diferente de las reacciones impulsadas por enzimas estrechamente relacionadas con EFE.
Las enzimas son proteínas que inician o aceleran las reacciones químicas necesarias para mantener la vida. la mayoría de los cuales requieren átomos, grupos de átomos, o moléculas pequeñas —conocidas colectivamente como cofactores— para hacer que ocurran estas reacciones. EFE pertenece a una clase de enzimas que promueven reacciones de varios tipos de moléculas con oxígeno, habilitado por un cofactor de hierro y cosustrato de 2-oxoglutarato.
"Nuestro grupo de laboratorio ha estado estudiando enzimas relacionadas con EFE durante casi 20 años, "dijo Carsten Krebs, profesor de química y de bioquímica y biología molecular en Penn State y autor del artículo. "EFE es único entre esta familia de enzimas porque descompone el 2-oxoglutarato de dos formas diferentes. La primera está bien caracterizada, pero el segundo, el que produce etileno, ha sido un misterio hasta ahora ".
El equipo de investigación diseccionó la vía química para la formación de etileno por EFE insertando isótopos (átomos que difieren en peso atómico y pueden rastrearse a medida que la reacción está en progreso) en los diversos productos. De esta manera, el equipo podría rastrear átomos individuales para ver adónde van en el transcurso de la reacción. Por separado, también hicieron modificaciones químicas tanto a la enzima como al 2-oxoglutarato para ver cómo se alteraron la reacción y los productos.
"Con estas técnicas, pudimos ver que EFE inicia la reacción entre el 2-oxoglutarato y el oxígeno de una forma muy diferente a otras enzimas relacionadas, ", dijo Copeland." Inserta el oxígeno entre dos átomos de carbono de 2-oxoglutarato, que produce un compuesto intermedio único que la enzima luego descompone en etileno ".
La ubicación del átomo de oxígeno insertado se había predicho computacionalmente, pero no se había mostrado experimentalmente hasta ahora.
"Se han propuesto varios mecanismos a lo largo de los años para explicar cómo EFE convierte el 2-oxoglutarato en etileno, pero no ha habido datos experimentales para distinguir entre ellos, "dijo J. Martin Bollinger Jr., profesor de química y de bioquímica y biología molecular en Penn State y autor del artículo. "Rachelle diseñó estos experimentos para observar los aspectos más fundamentales de la reacción. ¿Dónde van los átomos individuales? Y traza un mecanismo inequívocamente claro".