Crédito:Instituto de Tecnología de Massachusetts
Las reacciones electroquímicas que se aceleran mediante el uso de catalizadores se encuentran en el centro de muchos procesos de fabricación y uso de combustibles. productos químicos, y materiales, incluido el almacenamiento de electricidad de fuentes de energía renovables en enlaces químicos, una capacidad importante para descarbonizar los combustibles para el transporte. Ahora, La investigación en el MIT podría abrir la puerta a formas de hacer que ciertos catalizadores sean más activos, y mejorando así la eficiencia de tales procesos.
Un nuevo proceso de producción produjo catalizadores que aumentaron cinco veces la eficiencia de las reacciones químicas, permitiendo potencialmente nuevos procesos útiles en bioquímica, química Orgánica, química ambiental, y electroquímica. Los hallazgos se describen hoy en la revista. Catálisis de la naturaleza , en un artículo de Yang Shao-Horn, un profesor del MIT de ingeniería mecánica y de ciencia e ingeniería de materiales, y miembro del Laboratorio de Investigación de Electrónica (RLE); Tao Wang, un postdoctorado en RLE; Yirui Zhang, estudiante de posgrado en el Departamento de Ingeniería Mecánica; y otros cinco.
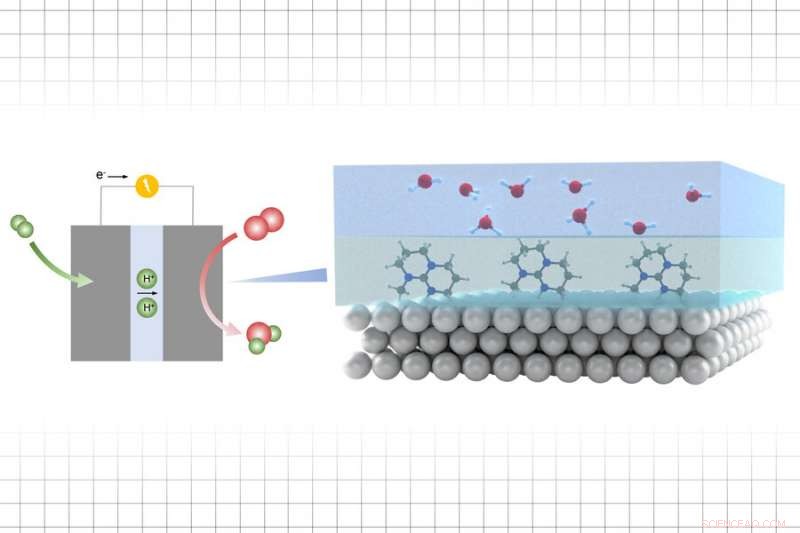
El proceso implica agregar una capa de lo que se llama un líquido iónico entre un catalizador de oro o platino y una materia prima química. Los catalizadores producidos con este método podrían potencialmente permitir una conversión mucho más eficiente de combustible de hidrógeno en dispositivos de energía como las pilas de combustible, o conversión más eficiente de dióxido de carbono en combustibles.
"Existe una necesidad urgente de descarbonizar la forma en que impulsamos el transporte más allá de los vehículos ligeros, cómo hacemos combustibles, y cómo fabricamos materiales y productos químicos, "dice Shao-Horn, haciendo hincapié en el llamamiento urgente para reducir las emisiones de carbono destacado en el último informe del IPCC sobre cambio climático. Este nuevo enfoque para mejorar la actividad catalítica podría proporcionar un paso importante en esa dirección, ella dice.
El uso de hidrógeno en dispositivos electroquímicos como las pilas de combustible es un enfoque prometedor para descarbonizar campos como la aviación y los vehículos pesados. y el nuevo proceso puede ayudar a que esos usos sean prácticos. En el presente, la reacción de reducción de oxígeno que impulsa a estas pilas de combustible está limitada por su ineficacia. Los intentos anteriores de mejorar esa eficiencia se han centrado en elegir diferentes materiales catalizadores o modificar sus composiciones superficiales y estructura.
En esta investigación, sin embargo, en lugar de modificar las superficies sólidas, el equipo agregó una capa delgada entre el catalizador y el electrolito, el material activo que participa en la reacción química. La capa de líquido iónico, ellos encontraron, regula la actividad de los protones que ayudan a aumentar la velocidad de las reacciones químicas que tienen lugar en la interfaz.
Debido a que existe una gran variedad de tales líquidos iónicos para elegir, es posible "sintonizar" la actividad de los protones y las velocidades de reacción para que coincidan con la energía necesaria para los procesos que involucran la transferencia de protones, que se puede utilizar para fabricar combustibles y productos químicos a través de reacciones con oxígeno.
"La actividad de los protones y la barrera para la transferencia de protones está gobernada por la capa de líquido iónico, y, por lo tanto, hay una gran capacidad de sintonización en términos de actividad catalítica para reacciones que involucran transferencia de protones y electrones, ", Dice Shao-Horn. Y el efecto es producido por una capa extremadamente delgada del líquido, solo unos pocos nanómetros de espesor, por encima de la cual hay una capa mucho más gruesa del líquido que va a sufrir la reacción.
"Creo que este concepto es novedoso e importante, "dice Wang, el primer autor del artículo, "porque la gente sabe que la actividad de los protones es importante en muchas reacciones electroquímicas, pero es muy difícil de estudiar ". Eso se debe a que en un entorno acuático, hay tantas interacciones entre las moléculas de agua vecinas involucradas que es muy difícil separar qué reacciones están teniendo lugar. Al usar un líquido iónico, cuyos iones solo pueden formar un enlace sencillo con el material intermedio, se hizo posible estudiar las reacciones en detalle, utilizando espectroscopia de infrarrojos.
Como resultado, Wang dice:"Nuestro hallazgo destaca el papel fundamental que desempeñan los electrolitos interfaciales, en particular, el enlace de hidrógeno intermolecular, puede contribuir a mejorar la actividad del proceso electrocatalítico. También proporciona información fundamental sobre los mecanismos de transferencia de protones a nivel mecánico cuántico, que puede empujar las fronteras del conocimiento de cómo los protones y los electrones interactúan en las interfaces catalíticas ".
"El trabajo también es emocionante porque brinda a las personas un principio de diseño sobre cómo pueden ajustar los catalizadores, ", dice Zhang." Necesitamos algunas especies justo en un 'punto óptimo', ni demasiado activas ni demasiado inertes, para mejorar la velocidad de reacción ".
Con algunas de estas técnicas, dice Reshma Rao, un doctorado reciente del MIT y ahora un postdoctorado en el Imperial College, Londres, quien también es coautor del artículo, "Vemos un aumento de hasta cinco veces en la actividad. Creo que la parte más emocionante de esta investigación es la forma en que abre una dimensión completamente nueva en la forma en que pensamos sobre la catálisis". El campo se había topado con "una especie de barricada, " ella dice, en la búsqueda de formas de diseñar mejores materiales. Al enfocarse en la capa líquida en lugar de la superficie del material, "Esa es una forma completamente diferente de ver este problema, y abre una dimensión completamente nueva, un eje completamente nuevo a lo largo del cual podemos cambiar las cosas y optimizar algunas de estas velocidades de reacción ".