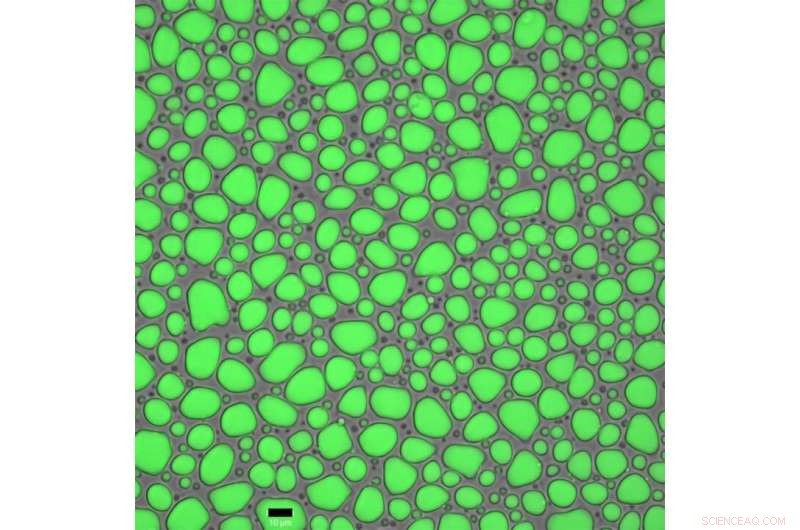
La adición de fosfato de potasio hace que las proteínas artificiales MaSp2 se condensen en gotas grandes de alta densidad. Crédito:Universidad de Kioto / Laboratorio Numata
De todos los temas interesantes en el campo de la investigación bioquímica y de materiales, uno de los más calientes, con mucho, es el de desentrañar los misterios de la seda de araña.
A menudo se dice que es 'más fuerte que el acero', las fibras a base de proteínas tienen el potencial de cambiar el mundo material tal como lo conocemos. Sin embargo, a pesar de décadas de investigación, nadie ha podido producir en masa seda de araña, principalmente porque el método exacto de cómo se hace todavía está envuelto en un misterio.
En un paso hacia la comprensión de su funcionamiento interno, investigadores de la Escuela de Graduados de Ingeniería de la Universidad de Kioto informan sobre un nuevo modelo para el ensamblaje de seda de araña, informando que la clave para el 'hilado' de la seda de araña es una combinación de acidificación y un proceso conocido como separación de fase líquido-líquido, o LLPS.
"La seda de araña está hecha de proteínas llamadas espidroína. La araña tiene una glándula que está densamente llena de espidroína en su estado líquido llamada droga, "explica Ali D Malay, primer autor del estudio, publicado en Avances de la ciencia .
"Este líquido se convierte rápidamente en seda resistente y estructuralmente compleja. Para investigar cómo se hace exactamente esto, decidimos volver a la mesa de dibujo y observar las espidroínas en sí. Así que desarrollamos espidroínas artificiales que imitan de cerca las que se encuentran en la naturaleza. "
Desarrollar la proteína no fue tarea fácil, pero llegaron al uso de una espidroína específica llamada MaSp2, una de las proteínas de seda de araña más comunes, y que sean solubles en agua.
Después de aislar su proteína de seda de araña artificial, el equipo comenzó a observar su actividad en diferentes condiciones químicas, con la intención de comprender qué cambios químicos clave son necesarios para que la fase líquida se vuelva sólida.
"Primero vimos la proteína reuniéndose en pequeños grupos. Pero cuando agregamos fosfato de potasio, instantáneamente comenzó a condensarse en grandes gotas de alta densidad, ", explica Malay." Este es un fenómeno conocido como separación de fase líquido-líquido, ocurre con bastante frecuencia en las células, y es cuando las gotas de líquido cambian su tamaño y densidad de acuerdo con el entorno circundante ".
Pero esta era solo una parte del rompecabezas. ¿Qué se necesita para convertir esta fase líquida en las fibras de seda que conocemos tan bien? La clave fue el pH. A medida que el equipo bajó el pH de la solución, los globos comenzaron a fusionarse, formando una fina red de fibras.
Tanto la formación de LLPS como de la red de fibra se produjo de forma tan espontánea que fue visible en tiempo real. Es más, cuando la red de fibras se sometió a tensión mecánica, comenzó a organizarse en una estructura jerárquica como la seda de araña.
"La seda de araña a menudo supera a los materiales artificiales más avanzados de la actualidad, y la fabricación de estas fibras sintéticas a menudo se basa en disolventes orgánicos nocivos y altas temperaturas. Lo increíble aquí es que pudimos formar seda de araña usando agua como solvente, y a temperatura ambiente, ", concluye Keiji Numata, quien dirigió el estudio.
"Si podemos aprender a emular los mecanismos del hilado de la seda de araña, podría tener un impacto profundo en el futuro de la fabricación ".