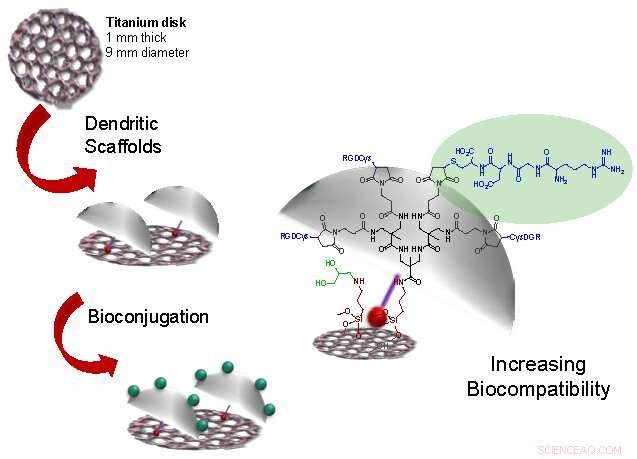
El implante de titanio está recubierto con una nanoestructura ramificada tridimensional que transporta sustancias que facilitan la formación de tejido nuevo. Crédito:Fundación Descubre
Un equipo de investigación de la Universidad de Málaga, el Centro Andaluz de Nanomedicina y Biotecnología-BIONAND, el Instituto Tecnológico de Canarias, la empresa Osteobionix, y el CIBER (Networking Center for Biomedical Research) ha desarrollado un recubrimiento para prótesis de titanio basado en polímeros ramificados 3-D que pueden incorporar sustancias que faciliten la unión con el hueso. Este mecanismo facilita el reconocimiento de células óseas del implante, mejorando así la osteointegración y evitando tanto el rechazo como el desgaste de la masa ósea y del propio implante.
El resultado es un implante de titanio recubierto con una nanoestructura ramificada tridimensional, llamado dendrímero, que actúa como puente entre el titanio y el hueso y que también transporta sustancias que facilitan la formación de tejido nuevo sobre la superficie de la prótesis. Esto asegura que el componente sano se adhiera a la prótesis haciendo que la fijación se produzca de forma natural, más estable y más duradero que los actuales.
El método propuesto por los investigadores en el artículo "Andamio dendrítico sobre implantes de titanio. Una estrategia versátil que aumenta la biocompatibilidad, "publicado en la revista Polímeros , confiere características específicas a los implantes, ya que tienen una estructura más homogénea con mayor integridad, que causa menos desgaste. También ofrece la posibilidad de controlar su composición para la administración de fármacos específicos con el fin de evitar rechazos e infecciones.
Específicamente, los expertos incluyeron fragmentos de proteínas que el cuerpo produce de forma natural, conocidas como fibronectinas, que fomentan la unión de las células óseas al implante. Estas moléculas hacen que las células crezcan y proliferen. resultando en una mayor aceptación del elemento externo. Leonor Santos-Ruiz, investigador de la Universidad de Málaga y uno de los autores del artículo, declaró a Fundación Descubre:"Las integrinas de las células funcionan como ganchos perfectos que se adhieren a los fragmentos de fibronectina introducidos en la estructura dendrímero, logrando una sólida integración entre el implante y el organismo ".
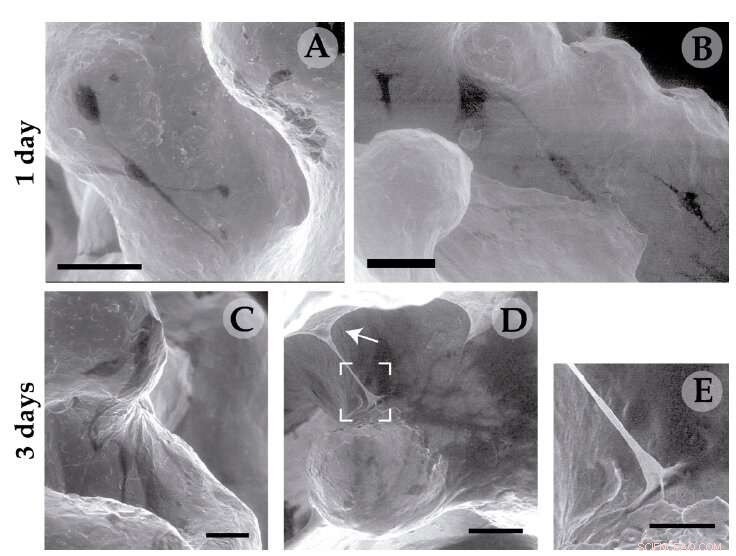
Microscopía electrónica de células osteoblásticas humanas con discos de titanio y recubiertas por la estructura 1 y 3 días después del implante. Crédito:Fundación Descubre
De este modo, cada rama del andamio se une al hueso con estos ganchos, anclando así el implante y ayudando a que las conexiones se produzcan de forma natural gracias a la integración del metal con el tejido vivo. "Estas propiedades únicas hacen que los sistemas dendriméricos sean adecuados para una amplia variedad de aplicaciones en la medicina regenerativa, "agregó el investigador.
Por lo tanto, además de fibronectinas, se podrían incorporar otras sustancias, como sustancias antiinflamatorias, que favorecen la recuperación de los tejidos tras la instalación de la prótesis, o antibióticos, para evitar problemas frecuentes en los implantes actuales, como infecciones bacterianas.
Implantes convertidos en hueso
Los problemas derivados de las sustituciones por material metálico suelen deberse a sobrecargas, que puede conducir a la pérdida de hueso sano, desgaste del propio implante, o una mala interacción hueso-implante que resulta en rechazo o infección.
Crédito:Fundación Descubre
Los expertos ya están trabajando para confirmar la idoneidad de su uso en pacientes como se ha demostrado en el laboratorio. Además, lo consideran una opción viable y aplicable para los implantes dentales, y para la mandíbula completa, prótesis de cadera o rodilla. Estos últimos tienen actualmente una vida útil de unos 10 años. Con esta nueva estructura la duración sería mayor, "concluyó el investigador.
El trabajo de estos expertos modificó las superficies de los dendrímeros con el fragmento de fibronectina conocido como "dominio RGD, "que consta de solo tres aminoácidos (arginina, glicina y aspartato) que sirven como ancla para los receptores de la membrana celular llamados integrinas. Estos receptores transmiten a las células numerosas señales cruciales sobre el entorno circundante y determinan si la célula puede adherirse o no a un material en particular.
Los metales, Los polímeros y productos sintéticos utilizados para fabricar las prótesis actuales carecen del dominio RGD, ya que no son materiales biológicos, y por lo tanto es difícil para las células reconocerlos. Cuando el metal se recubre con un dendrímero que lleva el dominio RGD, la célula encuentra un punto de anclaje en ese metal y se une a él de forma natural. Por tanto, esta composición ha favorecido y mejorado la adhesión celular a las superficies de titanio, lo que aumenta su biocompatibilidad, es decir, su capacidad de ser aceptado por el organismo. Al hacerlo, el dendrímero se fija al hueso, que lo interpreta como parte de sí mismo y no como algo ajeno, y tanto el implante como el lugar donde está instalado pueden hablar el mismo 'lenguaje biológico' y no hay rechazo.