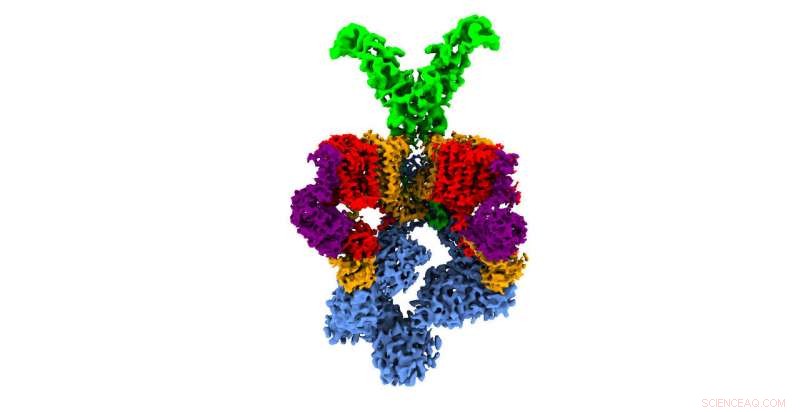
Estructura 3D del sistema de secreción T7SS de la bacteria 'Mycobacterium smegmatis', similar al utilizado por la bacteria de la tuberculosis durante la infección. Las diferentes proteínas que componen esta nanomáquina se muestran en diferentes colores. En azul, Los elementos del sistema ubicados en el interior de la bacteria son los encargados de atrapar los factores de virulencia producidos por la bacteria y proporcionar la energía necesaria para su secreción. En verde, parte del sistema ubicado fuera de la membrana de la bacteria, y que constituye parte del poro por el que se secretan los factores de virulencia. Crédito:CNIO
Un equipo internacional encabezado por Óscar Llorca en el Centro Nacional de Investigaciones Oncológicas (CNIO), y el grupo dirigido por Sebastian Geibel en la Universidad de Würzburg (Alemania), informan de un modelo tridimensional preciso del mecanismo utilizado por la bacteria Mycobacterium tuberculosis para bloquear la respuesta inmune al infectar un organismo.
Este hallazgo tan esperado se publica en Naturaleza . En una época en la que las bacterias desarrollan cada vez más resistencia a los antibióticos, Poner fin a la epidemia de tuberculosis es uno de los problemas de salud más urgentes de los Objetivos de Desarrollo Sostenible establecidos por la Organización de las Naciones Unidas (ONU) para el año 2030.
La tuberculosis es una enfermedad infecciosa con una alta tasa de mortalidad:es una de las 10 principales causas de muerte en todo el mundo. y afecta especialmente a personas con SIDA y otras inmunodeficiencias. Según datos de la OMS, 10 millones de personas contrajeron tuberculosis en 2017 en todo el mundo, y 1,6 millones murieron. Dado que el tratamiento actual se ha utilizado durante 40 años y están surgiendo nuevas cepas de la enfermedad resistentes a los antibióticos, la necesidad de nuevas estrategias terapéuticas es urgente.
Bacterias contra el sistema inmunológico.
Cuando un organismo está infectado por M. tuberculosis, el sistema inmunológico lanza una respuesta compleja para destruirlo. La bacteria ha desarrollado varios mecanismos sofisticados para debilitar el sistema inmunológico. La bacteria usa un sistema de secreción, un complejo de proteínas ubicado en su membrana, para inyectar ciertos factores de virulencia en las células del sistema inmunológico. Estos factores son moléculas que paralizan la respuesta defensiva de las células inmunes para que las bacterias tengan rienda suelta para seguir infectando el organismo.
La estructura y el mecanismo de funcionamiento del sistema de secreción de M. tuberculosis, llamado T7SS (sistema de secreción de tipo VII), no se había estudiado en detalle. Hasta ahora, sólo se había obtenido información estructural de muy baja resolución, el cual presentaba una estructura en forma de hexámero (estrella de seis puntas) cuyo centro sirve de canal a través del cual la bacteria expulsa los factores de virulencia. La falta de información sobre T7SS y sobre su funcionamiento a nivel atómico ha impedido avanzar en el logro de nuevas estrategias terapéuticas contra la tuberculosis basadas en atacar el sistema de secreción.
Ahora, los investigadores Óscar Llorca y Ángel Rivera-Calzada del CNIO, que contribuyeron con su experiencia en microscopía crioelectrónica (crio-EM) y procesamiento de imágenes digitales, y Sebastian Geibel y Nikolaos Famelis de la Universidad de Würzburg, expertos en sistemas de secreción bacteriana, Fuerzas combinadas para desentrañar este rompecabezas. Ahora han descrito T7SS a nivel atómico. Los investigadores trabajaron con una bacteria muy similar, M. smegmatis, que se utiliza en la investigación como modelo para estudiar M. tuberculosis y que comparte el mismo sistema de secreción con ella. El trabajo ha demostrado que T7SS es una nanomáquina sofisticada en la que varias proteínas cooperan para inyectar los factores de virulencia producidos por la bacteria en las células del sistema inmunológico.
Hacia una nueva generación de drogas
Los desarrollos recientes han transformado cryo-EM en una tecnología extremadamente poderosa que permite la obtención de imágenes de alta resolución de estructuras moleculares. Esta técnica acelera la obtención de información estructural que de otro modo requeriría grandes volúmenes de muestra o su cristalización. Con esta técnica, la biología molecular y la biomedicina están dando un gran salto cualitativo que se espera que revolucione el desarrollo de tratamientos de enfermedades.
En este papel, los investigadores han identificado todos los componentes de T7SS, y esclareció la función de algunos de ellos que permaneció desconocida. También han modelado su estructura tridimensional y han propuesto un mecanismo operativo.
“Pudimos ver que los componentes que hasta ahora aparecían borrosos con otras técnicas son, De hecho, elementos que están en constante movimiento, "explica Llorca". vimos que el hexámero de T7SS está compuesto por un subcomplejo de 4 proteínas y que se necesitan 6 copias idénticas de este subcomplejo para dar forma a la estrella de seis puntas alrededor de un poro central, a través del cual se expulsan los factores de virulencia que bloquean la respuesta defensiva del organismo infectado ”. Posteriormente, el mecanismo propuesto fue probado por el grupo de la Universidad de Würzburg utilizando versiones mutadas del sistema.
El sistema utilizado por el grupo alemán para probar el mecanismo también es de gran interés para la comunidad investigadora. "Será muy útil probar el efecto de nuevas moléculas dirigidas contra este mecanismo de secreción, que las bacterias del género Mycobacterium necesitan para llevar a cabo con éxito la infección, "explica Rivera-Calzada.
Este estudio multidisciplinario abre un nuevo campo para explorar las enfermedades causadas por infecciones bacterianas, ya que conocer las estructuras tridimensionales de los sistemas de secreción bacteriana permitirá explorar nuevos compuestos que bloquean la secreción. En los próximos pasos de esta investigación, El equipo del CNIO y la Universidad de Würzburg intentarán estudiar con mayor profundidad cómo se produce el proceso de secreción en Mycobacterium para abrir paso al diseño de moléculas que puedan bloquearlo.