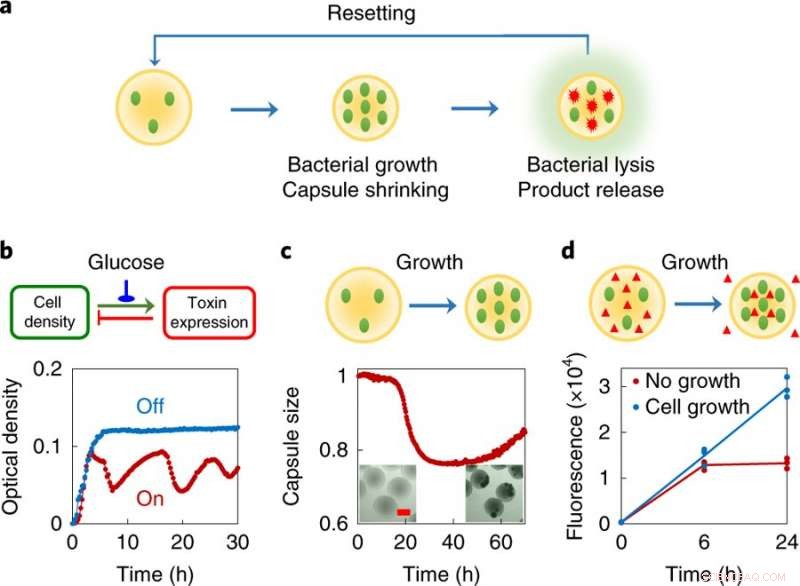
a, Concepto de diseño, cada swarmbot consiste en una pequeña población de bacterias manipuladas encapsuladas en microcápsulas poliméricas. Estas bacterias están diseñadas para someterse a una lisis parcial a una densidad local suficientemente alta. En cambio, el material de encapsulación se encogerá en respuesta al entorno químico cambiante causado por el crecimiento celular. A medida que las bacterias se someten a una autólisis programada, liberan proteínas intracelulares. Las cápsulas poliméricas reticuladas atrapan las células vivas y los desechos grandes en el interior, y la contracción correspondiente facilita la exportación de productos proteicos de las cápsulas. El sistema se reinicia rellenando con medio nuevo. B, Lisis autónoma programada por el circuito ePop (arriba, lógica de circuito; fondo, datos experimentales). Un aumento dependiente de la densidad en el número de copias de plásmido conduce a un aumento en la expresión de una toxina (la proteína E del fago φX174). A una concentración suficientemente alta, la proteína E causa lisis celular, conduciendo a una disminución de la densidad celular. Cuando se enciende (curva roja), el circuito condujo a una densidad de cultivo reducida de MC4100Z1 (ePop) equilibrada por el crecimiento y la destrucción regulada. A los efectos del diseño general del sistema, la generación de oscilaciones no es imprescindible. El circuito se puede apagar (curva azul) agregando glucosa al 1%. El experimento se repitió más de tres veces de forma independiente con resultados similares. C, Reducción de las cápsulas en respuesta al crecimiento de bacterias encapsuladas (arriba, esquemático; fondo, datos experimentales). Se encapsularon células MC4100Z1 (ePop / GFP) en cápsulas de quitosano y se cultivaron en M9. Todos los datos se normalizaron al valor en el momento cero. Recuadro, Imágenes de microscopía de MSB después de 0 h (izquierda) y 48 h (derecha). Barra de escala, 200 μm. El experimento se repitió más de tres veces de forma independiente con resultados similares. D, La contracción de la cápsula mediada por el crecimiento facilita la exportación de macromoléculas de las cápsulas (arriba, esquemático; fondo, datos experimentales). Células MG1655 y dextrano-rodamina (peso molecular ≈ 70, 000 g mol-1) se encapsularon en las cápsulas de quitosano y se cultivaron en M9. Las cápsulas se trataron con o sin ampicilina (100 μg ml-1). Cápsulas que se encogen, causado por el crecimiento bacteriano en ausencia de antibióticos, condujo a un aumento de ~ 2,25 veces en la fluorescencia de rodamina en comparación con las cápsulas que no encogen después de 24 h, que contenía bacterias que no crecían (suprimidas por antibióticos). El experimento se realizó por triplicado como réplicas biológicas independientes y los datos se muestran como puntos individuales, la línea indica la media. Crédito: Biología química de la naturaleza (2019). DOI:10.1038 / s41589-019-0357-8
Los ingenieros biomédicos de la Universidad de Duke han desarrollado una nueva plataforma para crear fármacos biológicos utilizando bacterias especialmente diseñadas que explotan y liberan proteínas útiles cuando sienten que su cápsula se está llenando demasiado.
La plataforma se basa en dos componentes principales:las bacterias diseñadas, llamado "swarmbots, "que están programados para detectar la densidad de sus pares dentro de su contenedor, y el biomaterial que confina a los swarmbots, una cápsula porosa que puede encogerse en respuesta a cambios en la población bacteriana. Cuando se encoge la cápsula exprime las proteínas específicas creadas por las bacterias cautivas.
Esta plataforma autónoma podría facilitar a los investigadores la creación, analizar y purificar diversos productos biológicos para su uso en la fabricación biológica a pequeña escala.
La investigación apareció en línea el 16 de septiembre en la revista Biología química de la naturaleza .
Las bacterias se utilizan comúnmente para producir productos biológicos, que son productos como vacunas, terapias génicas y proteínas que se crean o sintetizan a partir de fuentes biológicas. En la actualidad, este proceso implica una serie de pasos sofisticados que incluyen el cultivo de células, aislamiento de proteínas y purificación de proteínas, cada uno de los cuales requiere una infraestructura delicada para garantizar la eficiencia y la calidad. Para operaciones industriales, estos pasos se llevan a cabo a gran escala. Si bien esto ayuda a producir grandes cantidades de ciertas moléculas, esta configuración no es flexible ni económicamente viable cuando los investigadores necesitan producir pequeñas cantidades de diversos productos biológicos o trabajar en entornos con recursos limitados.
La nueva tecnología fue desarrollada por Lingchong You, profesor de Ingeniería Biomédica en la Universidad de Duke, y ex investigador postdoctoral de Duke, Zhuojun Dai, ahora es profesor asociado en el Instituto de Tecnologías Avanzadas de Shenzhen. En el nuevo estudio, muestran cómo su nueva plataforma utiliza la comunicación entre swarmbots y su cápsula para lograr una producción versátil, análisis y purificación de diversas proteínas y complejos proteicos.
En una prueba de concepto anterior, Usted y su equipo diseñaron una cepa no patógena de la bacteria E. coli para producir un antídoto contra los antibióticos cuando la bacteria alcanza una cierta densidad. Estos enjambres fueron luego confinados a una cápsula, que fue bañado en antibióticos. Si una bacteria salió de la cápsula, se destruyó, pero si permanecía dentro del contenedor donde la densidad de población era alta, sobrevivió.
"Nuestro primer estudio mostró esencialmente la comunicación unidireccional, donde las células podían sentir el ambiente dentro de la cápsula pero el ambiente no reaccionaba a las células, "dijo usted". Ahora, tenemos comunicación bidireccional:los swarmbots diseñados todavía pueden sentir su densidad y su confinamiento, pero hemos introducido un material que puede responder cuando cambia la población bacteriana en su interior. Es como si los dos componentes estuvieran hablando entre sí, y colectivamente te dan un comportamiento muy dinámico ".
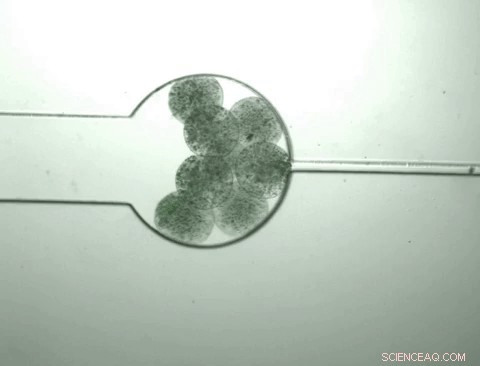
Las cápsulas que contienen bacterias adaptadas llamadas "swarmbots" crecen y se encogen en respuesta al entorno químico que contienen. Los swarmbots sienten que su propia densidad de población ha alcanzado un cierto nivel y se abren para liberar su contenido. incluida una proteína para la que han sido diseñados. Luego, la cápsula se encoge y el proceso se reanuda cuando se introducen los nutrientes. Crédito:Zhuojun Dai
Una vez que la población dentro de la cápsula alcanza una cierta densidad, las bacterias comienzan a estallar, 'liberando todo su contenido celular, incluido el producto proteico de interés. Al mismo tiempo, este crecimiento bacteriano cambia el entorno químico dentro de la cápsula, haciendo que se encoja. A medida que se encoge, exprime la proteína liberada de las células que estallan mientras las bacterias y los restos celulares se mantienen dentro de la cápsula.
Una vez que se recolectan las proteínas, los investigadores pueden agregar una reposición de nutrientes al plato como una señal para que las cápsulas se agranden. Esto restablece el ambiente interior y permite que las bacterias comiencen a crecer nuevamente. reiniciando el proceso. De acuerdo a ti, este ciclo se puede repetir hasta por una semana.
Para que el enfoque sea útil para la biofabricación, el equipo agregó las cápsulas a un chip de microfluidos, que incluía una cámara para que detectaran y cuantificaran qué proteínas se liberaban. Esto podría reemplazarse con una cámara de purificación para preparar las proteínas para su uso en biológicos.
"Es un proceso muy compacto. No necesitas electricidad, y no necesita una centrífuga para producir y aislar estas proteínas, "dijo usted." Hace que esta sea una buena plataforma para la biofabricación. Tiene la capacidad de producir un determinado tipo de medicamento en un formato muy compacto a bajo costo, y es fácil de entregar. Además de eso, esta plataforma ofrece una manera fácil de producir múltiples proteínas simultáneamente ".
De acuerdo a ti, esta facilidad de uso ha permitido al equipo producir, cuantificar y purificar más de 50 proteínas diferentes en colaboración con el laboratorio de Ashutoshi Chilkoti, Alan L. Kaganov Profesor y presidente del Departamento de Ingeniería Biomédica de Duke. También han explorado cómo su plataforma puede simplificar la creación de complejos de proteínas, que son estructuras hechas de múltiples proteínas.
En un experimento de prueba de concepto para producir una vía de síntesis de ácidos grasos a partir de múltiples enzimas, "pudimos utilizar siete versiones de nuestros swarmbots microbianos, cada uno de los cuales estaba programado para producir una enzima diferente, "dijo usted." Por lo general, para producir una vía metabólica, necesitaría equilibrar la cadena de suministro, lo que podría implicar regular al alza la expresión de una enzima y regular a la baja la expresión de otra. Con nuestra plataforma no necesita hacer eso, solo necesitas establecer la proporción correcta de swarmbots ".
"Esta tecnología es increíblemente versátil, ", dijo." Esa es una capacidad que queremos aprovechar ".