
Imágenes de resolución atómica de dosis baja de K2PtCl4. (A) El modelo atómico de la celda unitaria K2PtCl4, con K en cian, Pt en morado, y Cl en rosa. (B) Imagen TEM de campo brillante de un gran cristalito de K2PtCl4. (C) Patrón de difracción del cristalito de K2PtCl4 en (B) después de que se inclina a lo largo del eje de la zona (001). (D) Imagen TEM de baja dosis de resolución atómica de K2PtCl4. El fraccionamiento de la dosis se realizó utilizando una dosis de electrones de 1 e / Å2 · s, con 0,1 s para cada imagen. Se adquirieron sesenta y cuatro imágenes, alineado, y promediado. La dosis de electrones se convierte entonces en 6,4 e / Å2. El modelo atómico se superpone en el recuadro. (E) Imagen HREM simulada de K2PtCl4 con un espesor de 12,3 nm. (F) Una imagen ampliada de K2PtCl4 de una subárea en (D), y el perfil de la línea de intensidad en unidades arbitrarias (a.u.) del cuadro rojo, se muestra en (G), donde la intensidad de los átomos de Pt se encuentra entre dos átomos de Cl. Crédito:Science Advances, doi:10.1126 / sciadv.aau9590.
Una clave para la síntesis de materiales es la capacidad de controlar el proceso de cinética de reducción y nucleación (transición de fase) en los materiales. La comprensión de la dinámica de reducción durante la etapa inicial de síntesis de materiales es limitada debido a la dificultad de investigar reacciones químicas a escala atómica. Esto se debe principalmente a que los precursores químicos utilizados para sintetizar materiales pueden degradarse cuando se exponen a haces de electrones que se utilizan normalmente para obtener imágenes de compuestos a resolución atómica.
En un estudio reciente, ahora publicado en Avances de la ciencia , científicos de materiales interdisciplinarios Wenpei Gao y colaboradores en los EE. UU. y China, estudió la cinética de reacción de un compuesto precursor de platino (Pt) en estado sólido. En el estudio, utilizaron un microscopio electrónico de transmisión con corrección de aberraciones (TEM) combinado con electrones de baja dosis e imágenes in situ. Los científicos tomaron imágenes del precursor de Pt sensible al haz; tetracloroplatinato de potasio (II) (K 2 PtCl 4 ), a la resolución atómica para determinar los átomos individuales (K, Pt y Cl) implicados en la síntesis de nanoclusters de platino. Gao y col. capturó la transformación del material a nanoagrupamientos de Pt en tiempo real para mostrar la cinética de reacción de tres etapas, incluyendo (1) ruptura del enlace iónico, (2) formación de PtCl 2 y (3) reducción del Pt divalente a nanoagrupamientos metálicos de Pt.
En el nuevo método, los científicos combinaron técnicas para comprender la transformación de sustancias químicas a escala atómica en tiempo real sin dañar los sustratos y proporcionaron una nueva plataforma para estudiar la cinética de reacción. Gao y col. capturado identificó y reveló la dinámica en diferentes etapas de descomposición, reducción y nucleación del material. El trabajo les permitió comprender la cinética de transformación del platino de precursor a nanocluster como una vía prometedora para estudiar la dinámica de reacción a escala atómica.
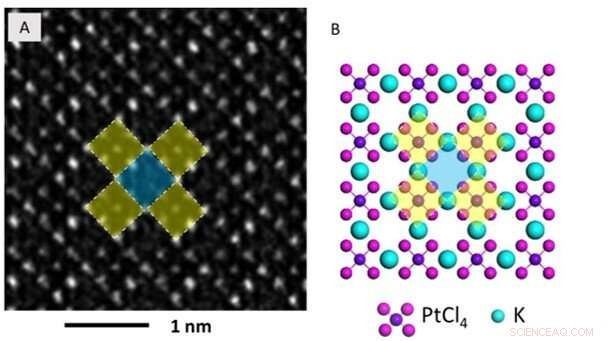
Imagen ampliada y modelo atómico de K2PtCl4. (A) y (B) son la imagen TEM correspondiente y el modelo de estructura atómica de K2PtCl4. Los cuadrados de color amarillo tienen un átomo de Pt en el centro, con átomos de Cl en los centros de los bordes y átomos de K en las esquinas. El cuadrado en azul no tiene un átomo de Pt en el centro. Crédito:Science Advances, doi:10.1126 / sciadv.aau9590
En química coloidal y sintética, Los científicos de materiales tienen como objetivo controlar la forma y el tamaño de las nanopartículas para lograr las propiedades deseadas de componentes electrónicos, materiales ópticos y catalíticos. La nucleación de nanocluster es un proceso clave de la cinética de crecimiento en el estado sólido de la síntesis de materiales. La manipulación de la cinética ha permitido la síntesis de un grupo de nanopartículas con forma de nanovarillas, nanocubos, octaedros, nanopartículas en forma de octópodo, icosaedros y otras características de la superficie.
Si bien la nucleación es el paso inicial en la síntesis de materiales, Es difícil controlar la cinética de nucleación sin comprender cómo interactúan los átomos. Las nanopartículas de platino generalmente se sintetizan en una reacción en fase líquida con C-H o Cl - como precursor. Durante el crecimiento en tal sistema, el precursor es reducido por el agente reductor para formar monómeros metálicos con disposiciones atómicas basadas en interacciones metal-metal. Sin embargo, un mecanismo microscópico que detalla los pasos de reacción intermedios aún no está disponible.
Como alternativa a la síntesis de materiales en fase líquida, Las nanoestructuras también se pueden cultivar en fase sólida. El estudio del proceso de reducción en estado sólido puede descifrar la transformación de materiales para un control preciso de la síntesis de materiales. Comprender la cinética de la transformación de materiales de precursores a nanoestructuras a escala atómica basada en la ruptura de enlaces iónicos es, por lo tanto, de considerable importancia.
Los científicos optaron por estudiar el proceso de nucleación en la fase sólida sin el entorno líquido utilizando herramientas de caracterización de nanodifracción de rayos X y TEM, que ofrecía una resolución ultra alta. El método resolvió las estructuras en evolución en el espacio real y recíproco, aunque la sensibilidad de la mayoría de los precursores químicos al haz de electrones debido a la fotoiluminación había hecho anteriormente casi imposible observar la estructura atómica inicial del precursor.
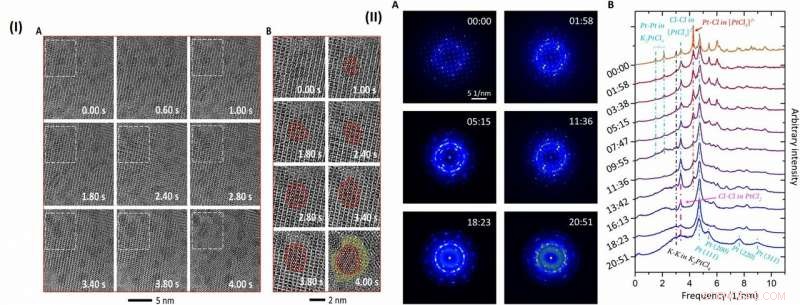
(I) Evolución de K2PtCl4 en nanopartículas de Pt. (A) Las imágenes secuenciales de TEM muestran la evolución de K2PtCl4 en nanopartículas de Pt. Un proceso de nucleación de nanopartículas de Pt se muestra en las imágenes ampliadas en (B), de la subárea marcada dentro de los recuadros de trazos blancos en (A). Las líneas de contorno rojas indican el borde de los grupos de Pt recién formados. La región en amarillo resalta el área vacía sin celosía después de la formación de un grupo de Pt. (II) Función de distribución radial secuencial (RDF) durante la transformación. (A) Difractograma de series de tiempo usando FFT de imágenes secuenciales de baja dosis. (B) RDF derivado del difractograma secuencial. Crédito:Science Advances, doi:10.1126 / sciadv.aau9590
Para la observación TEM, K 2 PtCl 4 se disolvió por primera vez en agua desionizada como preparación para obtener una imagen de su estructura cristalina. En la imagen TEM de campo brillante, el cristalito tenía un tamaño de 50 nm x 60 nm. Gao y col. debilitó la dosis del haz de electrones a la escala angstrom por menos de 1 e / A 2 ∙ s para limitar la reducción de la muestra inducida por el haz durante el proceso de obtención de imágenes. Los científicos realizaron microscopía electrónica de alta resolución (HREM) a 300, Ampliación de 000 x para obtener 64 imágenes de la misma zona. Al promediar las imágenes, las columnas atómicas se resolvieron claramente en el estudio.
La imagen TEM de alta resolución mostró cuadrados de celosía periódica con un átomo (amarillo) rodeando aquellos sin contraste atómico brillante (azul) en el centro. Gao y col. comparó las imágenes de resolución atómica con la estructura atómica existente de K 2 PtCl 4 para identificar cada elemento individual. Los científicos identificaron los átomos en las esquinas como potasio (K), átomos en el medio de los bordes de los cuadrados como cloro (Cl) y los del centro del cuadrado en amarillo como platino (Pt). Cuando Gao et al. aumentó la dosis del haz de electrones a 30 e / A 2 ∙ s, la celosía de K 2 PtCl 4, que originalmente se veía en toda el área se convirtió en grupos de Pt individuales. A tiempo, los nanoclusters se hicieron más pronunciados bajo el microscopio.

Análisis de composición del producto final. (A a D) Imagen HAADF y mapas EDS del producto final del experimento in situ y (E) EELS del producto final del experimento in situ que muestran la existencia de Cl y K. Crédito:Science Advances, doi:10.1126 / sciadv.aau9590
Luego observaron una mayor formación de los nanoclusters de Pt a lo largo de períodos de tiempo prolongados en condiciones de imágenes de baja dosis. Los científicos seleccionaron una subárea de las imágenes secuenciales y aplicaron una transformada rápida de Fourier (FFT) para discernir la estructura y los componentes. Gao y col. fueron capaces de obtener una serie de tiempo de patrones FFT en el K 2 PtCl 4 enrejado, que también refleja la función de distribución radial (RDF) (para encontrar partículas adyacentes). Luego, los científicos investigaron la orientación superficial adicional de los átomos en el material, además de los nanoclusters de Pt, para comprender la ubicación de las especies de K y Cl.
En el trabajo, utilizaron una serie de métodos analíticos y de imágenes de la ciencia de los materiales, comenzando con microscopía electrónica de transmisión de barrido (STEM) de campo oscuro anular de alto ángulo (HAADF) y el mapa 2-D de espectros de dispersión de energía (EDS) para caracterizar el material. Los resultados mostraron que las señales de K y Cl en el fondo estaban distribuidas uniformemente por el área. Cuando los científicos utilizaron la espectroscopia de pérdida de energía de electrones (EELS), observaron además la existencia de K y Cl a partir de KCl, después de la formación de nanopartículas de Pt.
Gao y col. recopiló suficiente información de la dinámica de reacción capturada en el espacio real a través de técnicas de espectroscopía y caracterización en la ciencia de los materiales. Propusieron un proceso microscópico de cinética de reducción para K 2 PtCl 4. Respectivamente, el precursor K 2 PtCl 4 primero descompuesto en K + y PtCl 4 2- rompiendo el enlace iónico débil.
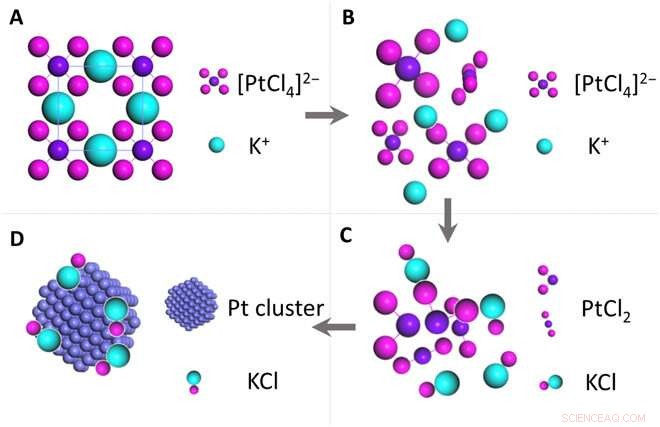
Un esquema que muestra la evolución de K2PtCl4 en nanopartículas de Pt. (A) K2PtCl4, (B) disociación de K + y [PtCl4] 2−, (C) disociación adicional en PtCl2 y KCl, y (D) nucleación de nanopartículas de Pt. Crédito:Science Advances, doi:10.1126 / sciadv.aau9590.
Entonces PtCl 4 2- descompuesto en PtCl 2 y Cl - , una reacción que no se había informado previamente en estudios experimentales. Gao y col. revelaron este proceso usando FFT de la imagen de alta resolución bajo una baja dosis de electrones y alta eficiencia de adquisición.
Al eliminar la especie K del precursor, la red se volvió inestable y los compuestos que incluían PtCl 2 , KCl y Cl 2 podría moverse libremente. Cuando PtCl 2 se redujo a Pt, las moléculas de Cl 2 pasó a la fase gaseosa para su eliminación de la columna TEM. La especie de Pt de valencia cero formó pequeños núcleos o migró y creció en grandes nanopartículas de Pt.
De este modo, los científicos demostraron elegantemente la cinética de reducción en el estudio e ilustraron el concepto utilizando modelos atómicos. Los hallazgos observados de nucleación y reducción de Pt coincidieron con los de la energía libre calculada previamente en la reacción química. Este método se puede aplicar para estudiar en profundidad transformaciones de materiales adicionales. Los resultados beneficiarán las aplicaciones de nanoestructuras en nanofísica para el desarrollo de nuevos materiales, nuevos procesos energéticos en remediación ambiental y en nanomedicina.
© 2019 Science X Network