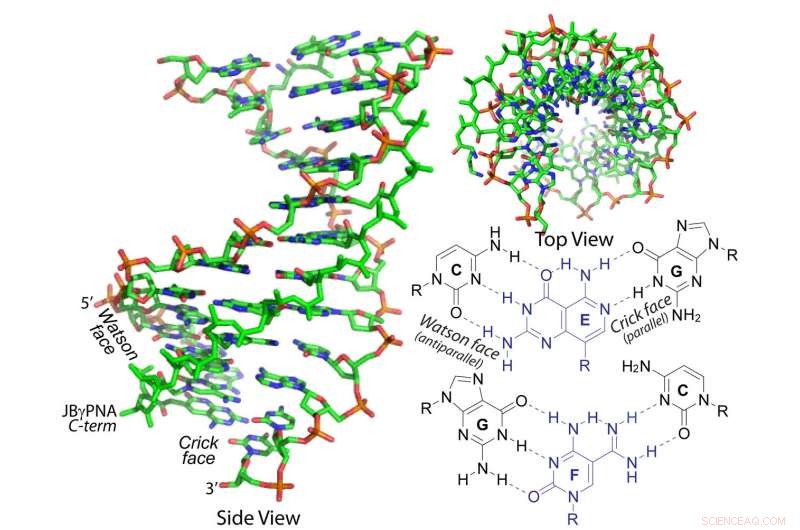
Desarrollado por investigadores de la Universidad Carnegie Mellon, este ácido nucleico peptídico janus gamma (PNA) puede invadir la doble hélice de ADN y ARN. Crédito:Universidad Carnegie Mellon
Los investigadores de la Universidad Carnegie Mellon han desarrollado una molécula sintética que puede reconocer y unirse al ADN o ARN de doble hebra en condiciones fisiológicas normales. La molécula podría proporcionar una nueva plataforma para desarrollar métodos para el diagnóstico y tratamiento de enfermedades genéticas. Sus hallazgos se publican en Química de las comunicaciones .
El trabajo fue realizado por un equipo internacional de expertos, incluyendo a la profesora Carnegie Mellon de Química Danith Ly, un experto en diseño de péptidos nucleicos, el postdoctorado en química Shivaji Thadke y la estudiante graduada de química Dinithi Perera, Profesor de Química y experto en resonancia magnética nuclear Roberto Gil, y Arnab Mukherjee, científico informático del Instituto Indio de Educación e Investigación Científica de Pune.
"Dado que Watson y Crick aclararon por primera vez la estructura de doble hélice del ADN, Los científicos han estado tratando de diseñar moléculas que puedan unirse al ADN y permitir que uno controle el flujo de información genética. ", dijo Ly." Esta es la primera molécula bifacial que puede invadir el ADN o ARN de doble hebra en condiciones biológicamente relevantes ".
ADN que contiene toda la información genética de un organismo, está formado por dos cadenas de nucleótidos. Los nucleótidos se conectan entre sí mediante enlaces de hidrógeno, formando una cadena helicoidal de pares de bases Watson-Crick. Si bien estos pares de bases proporcionan un código relativamente simple para nuestra información genética, Entrar en la doble hélice para cambiar el código es difícil debido a los fuertes vínculos entre los pares de bases.
Ly y sus colegas del Instituto de Diseño y Descubrimiento Biomolecular (IBD) de la Universidad Carnegie Mellon y del Centro de Ciencia y Tecnología de Ácidos Nucleicos (CNAST) son líderes en el diseño y desarrollo de ácidos nucleicos péptidos gamma (PNA gamma). Análogos sintéticos de ADN y ARN, Los PNA gamma se pueden programar para unirse al material genético (ADN o ARN) que causa la enfermedad, permitiéndoles buscar secuencias perjudiciales y unirse a ellas para evitar que un gen funcione mal.
El grupo ha creado PNA gamma de doble cara llamados PNA gamma Janus. Nombrado en honor al dios romano de dos caras, Los PNA de Janus son capaces de reconocer y unirse a ambas cadenas de una molécula de ADN o ARN.
El concepto de reconocimiento bifacial, que es la base de los PNA Janus gamma, fue concebido por primera vez hace más de dos décadas por Jean-Marie Lehn, un premio Nobel conocido por su trabajo en el campo de la química supramolecular, y expuesto por otros investigadores en el campo.
El avance de esta investigación se ha visto frenado por dos obstáculos. Primero, Los investigadores solo habían podido hacer una pequeña cantidad de bases de Janus, y esas bases variaban considerablemente en forma y tamaño. Estas limitaciones significaban que las diferentes bases de Janus solo podían reconocer repeticiones del mismo conjunto de pares de bases y no podían usarse juntas como bloques de construcción para reconocer secuencias más complejas en ADN o ARN.
En segundo lugar, fue difícil sintetizar bases de Janus para pares de bases canónicos. La naturaleza complementaria de los dos lados de las bases de Janus hizo que las moléculas se hibridaran y se unieran entre sí, impidiendo que se incorporen al ADN y al ARN.
En el estudio actual, Ly y sus colegas superan estos obstáculos. Crearon un conjunto completamente nuevo de elementos de reconocimiento de ácidos nucleicos bifaciales, 16 en total, que explicaba todas las combinaciones posibles de nucleobases que se podían encontrar en el código genético. Los PNA de Janus gamma se pueden usar para reconocer cualquier combinación de pares de bases y se pueden mezclar y combinar para detectar y unirse a secuencias genéticas complejas.
Thadke resolvió el problema de la síntesis química mediante el diseño de un nuevo método sintético en solución y en fase sólida para desarrollar los PNA Janus gamma. También implementó un truco inherente a la preorganización helicoidal en la columna vertebral del gamma PNA para evitar que las bases de Janus autocomplementarias se hibridaran entre sí.
Estos nuevos PNA Janus gamma tienen una energía de unión extraordinariamente alta y son los primeros en ser capaces de invadir una doble hélice de ADN o ARN de pares de bases canónicos a una temperatura y fuerza iónica fisiológicamente relevantes.
Lo hacen aprovechando el momento en que las moléculas de ADN y ARN de doble hebra "respiran" y los enlaces entre los pares de bases se abren durante fracciones de segundo. Cuando esto pasa, el Janus PNA se inserta entre los hilos separados. Si los pares de bases no coinciden, el Janus PNA se expulsa de la molécula de ADN. Pero si coinciden, el Janus PNA se une a ambas cadenas de la molécula.
Los PNA Janus gamma tienen una amplia gama de usos biológicos y biomédicos. Pueden diseñarse para apuntar al ADN genómico para la edición de genes y la regulación transcripcional. También podrían diseñarse para unirse de forma específica y selectiva a las estructuras secundarias y terciarias del ARN, algo que los agentes antisentido tradicionales y los ligandos de moléculas pequeñas no pueden hacer. Por ejemplo, los PNA gamma de Janus podrían programarse para unirse a expansiones repetidas de ARN, que podría conducir a nuevos tratamientos para una serie de trastornos neuromusculares y neurodegenerativos, incluyendo distrofia miotónica tipo 1 y enfermedad de Huntington, oa ARN no codificantes, incluido el ARN ribosómico y de telomerasa del patógeno, para combatir enfermedades genéticas e infecciosas.
La tecnología está siendo explorada tanto por empresas emergentes como por compañías farmacéuticas para desarrollos terapéuticos.