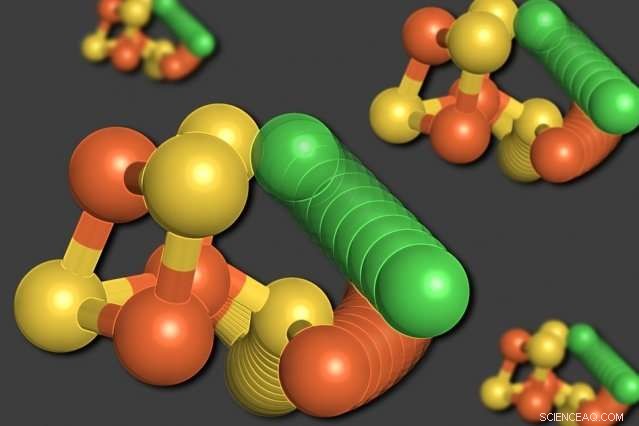
Los investigadores del MIT han demostrado que algunos de los átomos de una enzima llamada monóxido de carbono deshidrogenasa pueden reorganizarse cuando los niveles de oxígeno son bajos. Un átomo de níquel (verde) sale de la estructura en forma de cubo, desplazando un átomo de hierro (naranja). Un átomo de azufre (amarillo) también sale del cubo. Crédito:Elizabeth Wittenborn
Muchos microbios tienen una enzima que puede convertir el dióxido de carbono en monóxido de carbono. Esta reacción es fundamental para la construcción de compuestos de carbono y la generación de energía. particularmente para las bacterias que viven en ambientes libres de oxígeno.
Esta enzima también es de gran interés para los investigadores que desean encontrar nuevas formas de eliminar los gases de efecto invernadero de la atmósfera y convertirlos en compuestos útiles que contienen carbono. Los métodos industriales actuales para transformar el dióxido de carbono consumen mucha energía.
"Hay procesos industriales que hacen estas reacciones a altas temperaturas y altas presiones, y luego está esta enzima que puede hacer lo mismo a temperatura ambiente, "dice Catherine Drennan, profesor de química y biología del MIT e investigador del Instituto Médico Howard Hughes. "Por mucho tiempo, la gente ha estado interesada en comprender cómo la naturaleza realiza esta química desafiante con este ensamblaje de metales ".
Drennan y sus colegas del MIT, Universidad de Brandeis, y la Universidad de Aix-Marsella en Francia han descubierto ahora un aspecto único de la estructura del "grupo C":la colección de átomos de metal y azufre que forma el corazón de la enzima monóxido de carbono deshidrogenasa (CODH). En lugar de formar un andamio rígido, como se esperaba, el clúster realmente puede cambiar su configuración.
"No era lo que esperábamos ver, "dice Elizabeth Wittenborn, un reciente doctorado del MIT. destinatario y autor principal del estudio, que aparece en la edición del 2 de octubre de la revista eLife .
Una rueda de carro molecular
Los grupos que contienen metales, como el grupo C, realizan muchas otras reacciones críticas en los microbios, incluida la división del gas nitrógeno, que son difíciles de replicar industrialmente.
Drennan comenzó a estudiar la estructura de la monóxido de carbono deshidrogenasa y el grupo C hace unos 20 años. poco después de que ella comenzara su laboratorio en el MIT. Ella y otro grupo de investigación idearon una estructura para la enzima utilizando cristalografía de rayos X, pero las estructuras no eran exactamente iguales. Las diferencias finalmente se resolvieron y se pensó que la estructura de CODH estaba bien establecida.
Wittenborn asumió el proyecto hace unos años, con la esperanza de precisar por qué la enzima es tan sensible a la inactivación por el oxígeno y determinar cómo se forma el grupo C.
Para sorpresa de los investigadores, su análisis reveló dos estructuras distintas para el C-cluster. El primero era un arreglo que esperaban ver:un cubo que constaba de cuatro átomos de azufre, tres átomos de hierro, y un átomo de níquel, con un cuarto átomo de hierro conectado al cubo.
En la segunda estructura, sin embargo, el átomo de níquel se elimina de la estructura en forma de cubo y ocupa el lugar del cuarto átomo de hierro. El átomo de hierro desplazado se une a un aminoácido cercano, cisteína que lo mantiene en su nueva ubicación. Uno de los átomos de azufre también sale del cubo. Todos estos movimientos parecen ocurrir al unísono, en un movimiento que los investigadores describen como una "rueda de carro molecular".
"El azufre, el hierro, y el níquel todos se mudan a nuevas ubicaciones, "Drennan dice." Estábamos realmente conmocionados. Pensamos que entendíamos esta enzima, pero descubrimos que está haciendo este movimiento increíblemente dramático que nunca anticipamos. Luego obtuvimos más evidencia de que esto es realmente algo que es relevante e importante; no es solo una casualidad, sino que es parte del diseño de este grupo ".
Los investigadores creen que este movimiento, que ocurre con la exposición al oxígeno, ayuda a proteger el racimo de desmoronarse completa e irreversiblemente en respuesta al oxígeno.
"Parece que esto es una red de seguridad, permitir que los metales se muevan a lugares donde están más seguros en la proteína, "Drennan dice.
Douglas Rees, profesor de química en Caltech, describió el artículo como "un hermoso estudio de un fascinante proceso de conversión de grupos".
"Estos cúmulos tienen características similares a los minerales y podría pensarse que serían 'tan estables como una roca, '"dice Rees, que no participó en la investigación. "En lugar de, los clústeres pueden ser dinámicos, lo que les confiere propiedades que son críticas para su función en un entorno biológico ".
No es un andamio rígido
Este es el cambio de metal más grande que se haya visto en cualquier grupo de enzimas, pero se han visto reordenamientos a menor escala en algunos otros, incluyendo un grupo de metales que se encuentra en la enzima nitrogenasa, que convierte el gas nitrógeno en amoniaco.
"En el pasado, la gente pensaba en estos grupos como si fueran andamios rígidos, pero solo en los últimos años hay cada vez más evidencia de que no son realmente rígidos, "Drennan dice.
Los investigadores ahora están tratando de averiguar cómo las células ensamblan estos grupos. Aprender más sobre cómo funcionan estos clústeres, cómo se ensamblan, y cómo se ven afectados por el oxígeno podría ayudar a los científicos que intentan copiar su acción para uso industrial, Drennan dice. Existe un gran interés en encontrar formas de combatir la acumulación de gases de efecto invernadero mediante, por ejemplo, convertir el dióxido de carbono en monóxido de carbono y luego en acetato, que se puede utilizar como bloque de construcción para muchos tipos de compuestos útiles que contienen carbono.
"Es más complicado de lo que la gente pensaba. Si lo entendemos, entonces tenemos muchas más posibilidades de imitar realmente el sistema biológico, "Drennan dice.
Esta historia se vuelve a publicar por cortesía de MIT News (web.mit.edu/newsoffice/), un sitio popular que cubre noticias sobre la investigación del MIT, innovación y docencia.