Crédito:Wiley
Algunas pequeñas células que son diferentes del resto pueden tener un gran efecto. Por ejemplo, las células cancerosas individuales pueden ser resistentes a una quimioterapia específica, lo que provoca una recaída en un paciente que de otro modo se curaría. En el diario Angewandte Chemie , Los científicos ahora han introducido un chip basado en microfluídicos para la manipulación y posterior análisis de ácido nucleico de células individuales. La técnica utiliza campos eléctricos locales para "atrapar" las células de manera altamente eficiente (dielectroforesis).
Los análisis moleculares de células individuales son necesarios para comprender mejor el papel de las poblaciones celulares heterogéneas en el desarrollo de enfermedades y para desarrollar terapias efectivas para la medicina personalizada. La identificación de células individuales en una masa de otras células es un desafío enorme en la medicina diagnóstica. Las celdas deben estar ordenadas, retenida, transferido a otro recipiente con un volumen extremadamente pequeño ( <1 μL) y luego deben someterse a un análisis molecular. Los métodos convencionales suelen consumir mucho tiempo y son complejos, así como poco confiable e ineficiente. También pueden comprometer la viabilidad de las células, requieren grandes volúmenes de muestra, tienen un alto riesgo de contaminación, y / o requieren instrumentos costosos.
Científicos de la Universidad de Washington (Seattle, ESTADOS UNIDOS), Universidad Estatal de Iowa (Ames, ESTADOS UNIDOS), y el Centro de Investigación del Cáncer Fred Hutchinson (Seattle, EE. UU.) Han utilizado tecnología de microfluidos para superar estos problemas. Todos los pasos necesarios ocurren de manera confiable en un microchip especialmente desarrollado usando cantidades mínimas de solvente y sin requerir que las celdas estén marcadas. A diferencia de los chips de microfluidos convencionales, éste no requiere tecnología de fabricación compleja ni componentes como válvulas o agitadores.
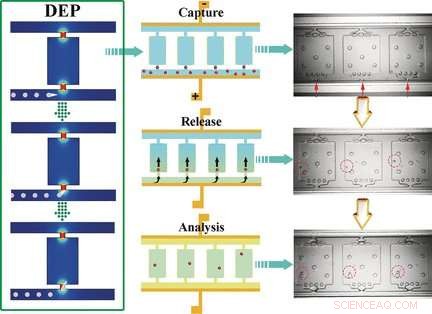
El chip de autodigitalización dielectroforético (SD-DEP) tiene aproximadamente el tamaño de una moneda y tiene dos microcanales paralelos (50 μm de profundidad x 35 μm de ancho x 3,2 cm de largo) conectados por numerosas pequeñas cámaras diminutas. Las aberturas de los microcanales tienen solo 15 μm de ancho. Se estira un electrodo delgado a lo largo de los canales. Los canales y cámaras se llenan con un búfer, se aplica una tensión alterna, y la muestra se agrega a uno de los microcanales. El equipo encabezado por Robbyn K. Anand y Daniel T. Chiu utilizó células leucémicas en sus experimentos.
Los máximos locales del campo eléctrico se producen en las estrechas entradas a las cámaras. Las células que entran en las cámaras quedan "atrapadas". Dado que las dimensiones de la entrada son similares al tamaño medio de una celda, solo una celda puede quedar atrapada por cada entrada de la cámara. Cuando se apaga la corriente alterna y se aumenta el caudal mediante la inyección de los reactivos necesarios para el análisis posterior, las células se lavan en las cámaras. Luego se agrega un aceite para sellar las cámaras. Luego, las células se disuelven, y los ácidos nucleicos se liberan y multiplican y pueden identificarse como células leucémicas mediante un gen marcador.
En estudios futuros, los investigadores esperan usar el chip para determinar la distribución de mutaciones genéticas que están relacionadas con la resistencia en las células leucémicas y, por lo tanto, pueden causar recaídas.