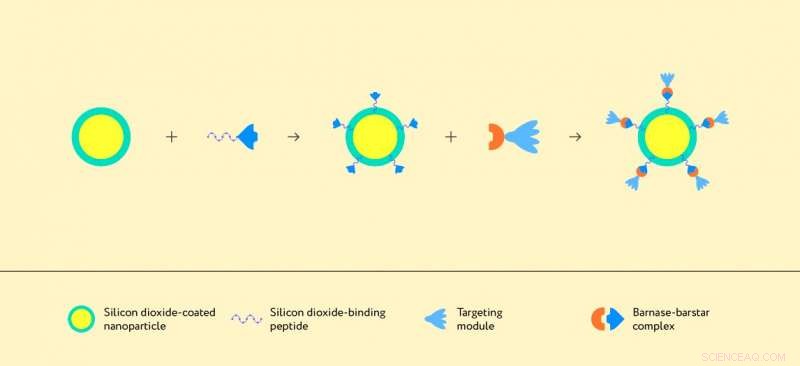
Ilustración del ensamblaje de la estructura basada en una nanopartícula y el complejo proteico barnasa-barstar. Crédito:Autores del artículo y Lion_on_helium, MIPT
Los biofísicos han desarrollado un método para modificar la superficie de micro y nanopartículas, estructuras diminutas que miden entre una milésima y una millonésima de milímetro, cubriéndolas con moléculas biológicas. Diseñado de esta manera, las partículas pueden servir como agentes terapéuticos y de diagnóstico, administrar medicamentos a las células cancerosas.
El artículo fue publicado en la revista Interfaces y materiales aplicados ACS . Sus autores son investigadores del Instituto de Física y Tecnología de Moscú (MIPT), el Instituto de Química Bioorgánica de la Academia de Ciencias de Rusia (IBCh RAS), MEPhI de la Universidad Nacional de Investigación Nuclear, Universidad Sechenov, y Universidad Macquarie (Australia).
Alrededor de 1900, Paul Ehrlich, el ganador del Premio Nobel de Fisiología o Medicina de 1908, medicamentos previstos que tendrían un componente que reconozca los patógenos en el cuerpo y otro componente que actúe sobre el objetivo. Generalmente, tales medicamentos se dirigen a los receptores en la superficie de las células dañadas. Estos receptores también permiten que el agente reconozca la célula. Un sistema universal de este tipo se puede utilizar para el diagnóstico, terapia, o ambos. Cuando se combinan la terapia y el diagnóstico, esto se conoce como teranósticos.
Hacer un sistema que incorpore un componente terapéutico y de diagnóstico, se necesita un "pegamento molecular" para unir las dos partes. Este pegamento se puede realizar como proteínas capaces de formar un complejo estable uniéndose entre sí. Uno de los complejos más estables de este tipo es el par de proteínas barnasa-barstar. Existe un valor conocido como constante de unión que caracteriza la fuerza con la que se acoplan las moléculas de un complejo. La constante de unión del complejo barnasa-barstar es 1, 000 a 1 millón de veces mayor que los de los complejos antígeno-anticuerpo, que son la base de nuestra respuesta inmunológica.
Barnase y barstar se pueden utilizar para diseñar varios módulos funcionales para teranóstica. Por ejemplo, barnasa se puede unir a agentes terapéuticos:anticuerpos, drogas moléculas fluorescentes, etc., mientras que barstar se puede fusionar con un agente de focalización. Este concepto fue sugerido por Sergey Deyev, el jefe del Laboratorio de Inmunología Molecular de IBCh RAS. A continuación, se combinan los dos módulos, formando un compuesto bifuncional, que tiene propiedades terapéuticas y de diagnóstico, y permite la administración de fármacos dirigida. Al fusionar barnasa y barstar con varias moléculas terapéuticas y de diagnóstico, los investigadores pueden desarrollar una gama de agentes teranósticos basados en el mismo principio. Estas estructuras moleculares pueden transportarse en la superficie de nanopartículas o micropartículas. Las propias partículas pueden tener propiedades auxiliares, incluida la fluorescencia o la capacidad de ser destruida cuando se expone a la radiación, matando las células dañinas circundantes, como las células cancerosas. Se pueden depositar docenas de estructuras moleculares de diferentes tipos en una partícula diminuta, potencialmente aumentando sus efectos terapéuticos.

Ilustración del principio operativo de la estructura teranóstica. Crédito:Autores del artículo y Lion_on_helium, MIPT
Kit de montaje molecular
La noción de utilizar nanopartículas y micropartículas para administrar medicamentos se está investigando activamente en muchos laboratorios. Los investigadores rusos y australianos desarrollaron un agente teranóstico basado en nanopartículas utilizando el complejo proteico barnasa-barstar y estudiaron sus propiedades.
"La mayoría de los métodos que se utilizan actualmente para acoplar químicamente biomoléculas a nanopartículas tienen graves defectos, "dice la autora principal Victoria Shipunova, investigador del Laboratorio de Nanobiotecnología del MIPT e investigador principal del Laboratorio de Inmunología Molecular del Instituto de Química Bioorgánica. "La orientación espacial de las biomoléculas está mal controlada, y encuentran problemas cuando se unen a sus objetivos. La densidad de las moléculas acopladas es bastante baja, y el procedimiento lleva mucho tiempo ".
"Desarrollamos un método basado en el par de proteínas barnasa-barstar que no altera la estructura espacial de las moléculas diana. Dos ventajas más son su alta especificidad y su rápido acoplamiento:solo se necesitan varios minutos para que todos los módulos se unan, " ella explica.
Los investigadores utilizaron partículas recubiertas de dióxido de silicio como portadores de su complejo molecular. Los objetivos principales de las bioestructuras descritas en el documento son las células cancerosas, identificables por el oncomarker HER2 / neu en su superficie, se muestra como una excrecencia roja en la figura 2. HER2 / neu es una proteína responsable del crecimiento y división celular y está presente en las células sanas. En las células cancerosas, sin embargo, esta proteína está en exceso, o sobreexpresada, lo que les permite crecer y dividirse sin control.
Los investigadores utilizaron una molécula de la clase de proteínas de repetición de anquirina diseñadas, o DARPins, como agente de direccionamiento que reconoce la proteína HER2 / neu. Mostrado como estructuras en forma de campana de color azul claro en las figuras 1 y 2, Las DARPins son proteínas pequeñas y altamente estables capaces de unirse selectivamente a la molécula diana. Además de una molécula de DARPin, que reconoce las células cancerosas, la estructura debe incorporar una molécula capaz de unirse a la superficie de la partícula portadora, es decir, al dióxido de silicio. Para esto, los investigadores utilizaron un péptido de unión a dióxido de silicio obtenido por diseño racional en la Universidad de Macquarie. Como resultado, crearon la siguiente estructura:una nanopartícula o micropartícula está recubierta con dióxido de silicio, al que se une el módulo barnasa-DARPin a través del péptido de unión a dióxido de silicio fusionado con barstar (figura 1). En tono rimbombante, cada uno de los elementos involucrados puede ser alterado o incluso reemplazado, modificar las propiedades de la estructura general. En cierto sentido, es similar a un kit molecular de bloques de construcción, que se puede ensamblar de muchas formas, produciendo diferentes agentes terapéuticos.
En efecto, los investigadores han creado un método de ensamblaje universal, que permite combinar fácilmente una serie de moléculas con potencial terapéutico y diagnóstico, preservando su estructura espacial y propiedades.