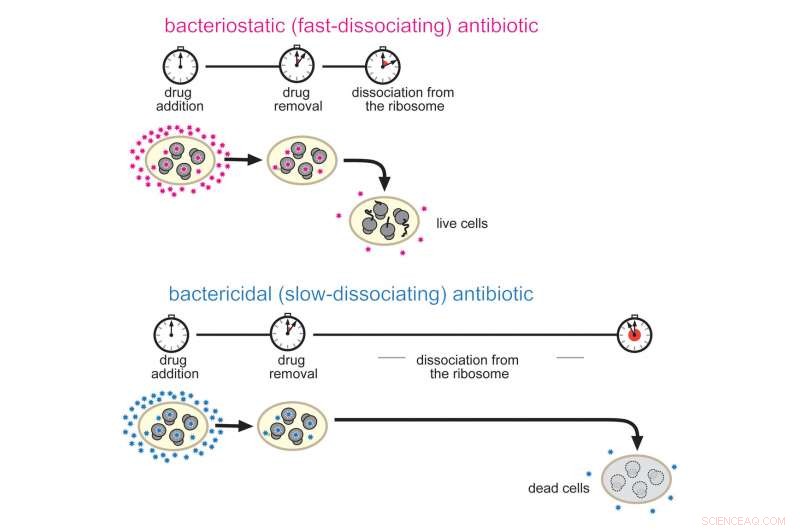
La investigación muestra que la inhibición prolongada de la síntesis de proteínas conduce a la muerte celular. Crédito:Actas de la Academia Nacional de Ciencias.
La investigación de la Universidad de Illinois en Chicago sugiere la duración del bono, no unión tirante, puede ser el diferenciador más importante entre los antibióticos que matan las bacterias y los antibióticos que solo detienen el crecimiento bacteriano.
Si bien ambos tipos de antibióticos se usan para tratar una variedad de infecciones bacterianas, Los antibióticos bactericidas, los que matan las bacterias, se pueden tomar durante períodos más cortos. se asocian con un menor riesgo de recurrencia de la infección y, a menudo, curan la infección mucho mejor que los antibióticos bacteriostáticos.
"Los antibióticos bacteriostáticos actúan retardando el crecimiento de las células bacterianas mientras el sistema inmunológico del individuo combate la infección, "dijo Alexander Mankin, autor principal del estudio y director del Centro de Ciencias Biomoleculares de la Facultad de Farmacia de la UIC. "A menudo, esto es suficiente para tratar una infección; pero si el sistema inmunológico no es lo suficientemente fuerte, la infección puede persistir ".
Desafortunadamente, no se sabe mucho acerca de por qué las moléculas de antibióticos a veces similares interactúan de manera diferente con las bacterias en el cuerpo.
Mankin y sus colegas analizaron una clase de antibióticos llamados macrólidos, que funcionan uniéndose al ribosoma de las bacterias para detener la síntesis de proteínas. Sin embargo, mientras que los antibióticos macrólidos son todos estructuralmente similares y actúan sobre el mismo objetivo molecular (el ribosoma), algunos son bactericidas y otros bacteriostáticos.
Usando una nueva técnica desarrollada por Maxim Svetlov, investigadora postdoctoral en el laboratorio de Mankin y Nora Vázquez-Laslop, un profesor asociado en el centro, los investigadores estudiaron las diferencias entre los macrólidos bacteriostáticos y bactericidas. La técnica permite analizar qué tan estrechamente interactúan los medicamentos con el ribosoma y medir la velocidad con la que los antibióticos pueden desconectarse del objetivo.
"Los investigadores suelen pensar que es la rigidez de la unión del fármaco al ribosoma lo que marca la diferencia entre un antibiótico que mata las bacterias y uno que solo ralentiza el crecimiento bacteriano. "Dijo Mankin." Por lo tanto, nos sorprendió descubrir que la rigidez de la unión del fármaco no define la capacidad del fármaco para matar bacterias.
"En cambio, entendimos que los fármacos bactericidas se disocian del ribosoma a un ritmo significativamente más lento, "Dijo Mankin.
La presencia de una cadena lateral extendida en la estructura del antibiótico funciona "como una mano extra para sujetar el ribosoma; permite que el fármaco se una por un período más largo, "dice Mankin.
Los resultados, publicado en el procedimientos de la Academia Nacional de Ciencias , ofrecen una posibilidad nueva y previamente inexplorada.
"Los resultados de este estudio sugieren que cuando hablamos del mecanismo de acción de los antibióticos, Necesitamos hablar sobre más que 'qué tan fuerte' se une una droga, "Dijo Mankin." También tenemos que hablar sobre la cinética y la tasa de disociación de un fármaco del ribosoma ".
Además de mejorar los resultados para las personas que necesitan tratamiento con antibióticos, particularmente para pacientes inmunodeprimidos, Comprender la diferencia entre antibióticos bacteriostáticos y bactericidas también puede ayudar a abordar el problema del aumento de la resistencia a los antibióticos en la sociedad.
"Si podemos comprender estos mecanismos, es posible que podamos reducir la velocidad a la que se desarrolla la resistencia a los antibióticos y se repiten las infecciones, "Dijo Mankin.