
Un LED azul se ilumina en un vial que contiene agua pesada, un compuesto farmacéutico, y un catalizador activado por luz. El nuevo enfoque fotocatalítico de David MacMillan de Princeton convierte un proceso de varios meses en un paso de un día, acelerar la llegada de nuevos medicamentos al mercado. Crédito:David MacMillan / Universidad de Princeton
La radiactividad puede tener mala reputación, pero juega un papel fundamental en la investigación médica. Una nueva técnica revolucionaria para crear moléculas radiactivas, pionera en el laboratorio del profesor de química de Princeton David MacMillan, tiene el potencial de llevar nuevos medicamentos a los pacientes mucho más rápido que antes.
"Un medicamento promedio tarda entre 12 y 14 años en llegar al mercado, "dijo MacMillan, el Profesor Distinguido de Química de la Universidad James S. McDonnell. "Entonces, todo lo que podamos hacer para tomar ese período de 14 o 12 años y comprimirlo beneficiará a la sociedad, porque lleva los medicamentos a las personas, a la sociedad, mucho más rápido ".
Cada medicamento nuevo potencial tiene que pasar por pruebas para confirmar que afecta la parte del cuerpo que se pretende que afecte. "¿Va al lugar correcto? ¿Al lugar equivocado? ¿Al lugar correcto y al lugar equivocado?" Preguntó MacMillan.
Trazar el camino de una sustancia química que se disuelve en el torrente sanguíneo presentó un serio desafío, pero uno que los radioquímicos resolvieron hace años intercambiando átomos individuales con sustitutos radiactivos. Una vez hecho esto, "las propiedades de la molécula, del fármaco, son exactamente las mismas, excepto que son radiactivas, y eso significa que puedes rastrearlos realmente, Realmente bien, "Dijo MacMillan.
Pero eso introdujo un nuevo problema.
"Introducir estos átomos radiactivos en la droga no es algo trivial, ", dijo." La gente se ha desarrollado durante mucho tiempo, a veces durante un mes, dos meses, secuencias de tres meses de duración sólo para obtener una pequeña cantidad de una sustancia con unos pocos átomos radiactivos ".
Pero ahora, él y sus colegas han encontrado una forma mejor, basándose en su trabajo utilizando luces LED azules y catalizadores que responden a la luz, conocidos como fotocatalizadores. Su investigación se publicó en línea en la revista. Ciencias el 9 de noviembre.
"¡Fue una idea loca! Afortunadamente, funcionó, ", Dijo MacMillan." Lo que se nos ocurrió fue, si les iluminas, ¿Podrían estos fotocatalizadores eliminar el átomo no radiactivo y luego instalar el átomo radiactivo? "
Ellos podrían.
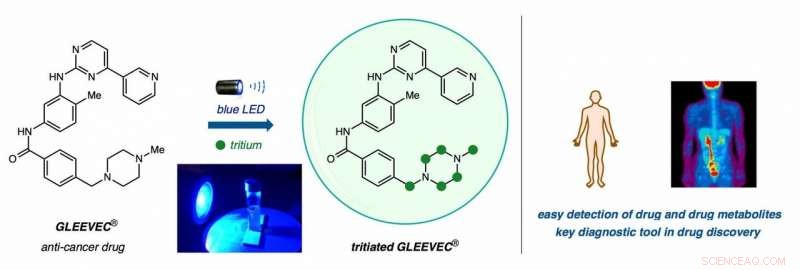
De izquierda a derecha:Gleevec, un medicamento contra el cáncer, se sumerge en agua pesada (T2O) y se baña en luz LED azul para reemplazar átomos de hidrógeno con átomos de tritio (círculos verdes) en un intercambio directo de isótopos de hidrógeno (HIE) de un solo paso. Los médicos pueden rastrear compuestos radiactivos en el cuerpo utilizando tecnologías de imagen sofisticadas con fines de investigación y diagnóstico. Crédito:Yong Yao Loh, Kazunori Nagao, y David MacMillan / Universidad de Princeton
La técnica de MacMillan utiliza "agua pesada, "que reemplaza el hidrógeno (H) en H2O con tritio, una versión radiactiva del hidrógeno que tiene dos neutrones extra por átomo.
"Si deja que su medicamento se asiente en el agua radiactiva y lo ilumine con un catalizador, el catalizador eliminará el átomo que no es radiactivo, en este caso es hidrógeno, y lo reemplazará con tritio, " él dijo.
Repentinamente, adjuntar una de estas etiquetas atómicas lleva horas en lugar de meses, y la técnica funciona con muchos tipos de compuestos de uso frecuente. Los investigadores ya lo han probado en 18 medicamentos disponibles comercialmente, así como candidatos en el proceso de descubrimiento de fármacos de Merck.
Para compuestos que no necesitan etiquetas radiactivas, el mismo proceso de un solo paso puede intercambiar en deuterio, una versión de hidrógeno con solo un neutrón extra. Estas "etiquetas estables" (con deuterio) y "etiquetas de radio" (con tritio) tienen innumerables aplicaciones, en el mundo académico y en el descubrimiento de fármacos.
La simplicidad de este nuevo enfoque tiene otra implicación, dijo Jennifer Lafontaine, el director senior de síntesis y química analítica de Pfizer en La Jolla, California, que no participó en la investigación.
Debido a que el proceso anterior requería tantos recursos, Las moléculas marcadas con deuterio o tritio a menudo solo se crearon para sustancias químicas que estaban "bastante avanzadas en el proceso de descubrimiento de fármacos, ", dijo." Por lo tanto, esta metodología podría abrir la puerta a un uso más temprano y ampliado del etiquetado isotópico en el descubrimiento de fármacos, mejorando significativamente nuestra capacidad para estudiar candidatos a fármacos en un nivel más profundo, y en una amplia gama de aplicaciones ".
Este nuevo método aprovecha el campo emergente de la fotocatálisis del que fue pionero en Princeton y lo aplicó a otro campo nuevo, Dijo MacMillan. También tiene un valor económico obvio, pero lo rechazó.
"Nadie está patentando nada de esto, porque queremos que esté disponible para que todos lo usen, "Dijo MacMillan.
Esta tecnología fue desarrollada en colaboración con Merck en el Merck Catalysis Center de Princeton, donde el estudiante graduado de Princeton Yong Yao Loh y el investigador postdoctoral Kazunori Nagao llevaron a cabo una investigación utilizando el material radiactivo, dijo Ian Davies, un coautor en el Ciencias paper que era el investigador principal en el laboratorio asociado de Merck mientras se realizaba la investigación.
"Este es un gran ejemplo de una colaboración entre Princeton e industria que beneficia a la ciencia y a toda la sociedad, "Dijo Davies.