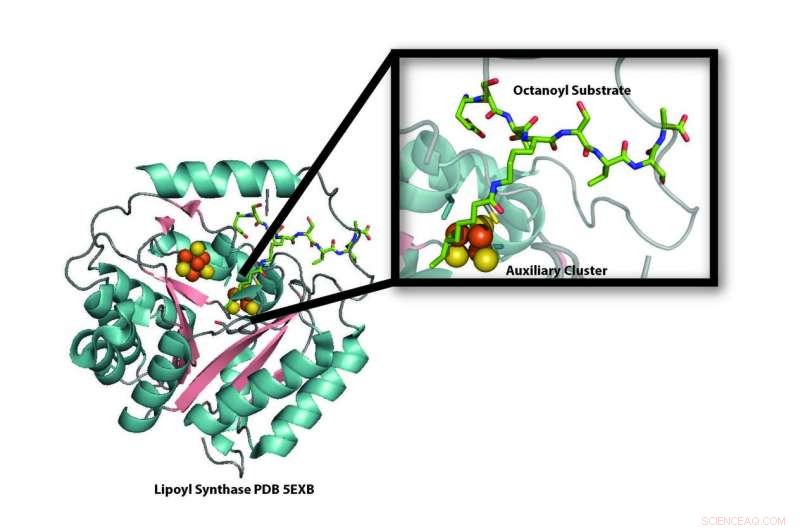
Modelo de la estructura cristalina de la enzima lipoil sintasa (LipA) de la bacteria Mycobacterium tuberculosis que revela la destrucción de uno de sus cúmulos de hierro-azufre (bolas naranjas y amarillas) para utilizarlo como fuente de azufre para la producción de ácido lipoico. Una nueva investigación demuestra que el grupo de hierro-azufre que se destruye durante la producción de ácido lipoico es reemplazado por una proteína transportadora de hierro-azufre, NfuA, para que LipA pueda seguir produciendo ácido lipoico. Crédito:laboratorio Booker, Universidad Penn State
Una nueva investigación muestra cómo se consume una proteína y luego se reconstituye durante la producción de ácido lipoico, un compuesto requerido por nuestros cuerpos para convertir la energía de los alimentos en una forma que pueda ser utilizada por nuestras células. La enzima lipoil sintasa (LipA) elimina dos átomos de hidrógeno de una cadena de carbono inerte y los reemplaza con átomos de azufre de uno de sus propios grupos de hierro-azufre para crear ácido lipoico. volviéndose inactivo en el proceso. La nueva investigación de Penn State University, que se publicará en la revista Ciencias el 20 de octubre 2017, muestra que otra proteína, un portador de racimo de hierro-azufre llamado NfuA, reemplaza el grupo de hierro-azufre destruido en LipA, lo que le permite seguir produciendo ácido lipoico. Los resultados también podrían ayudar a los científicos a comprender por qué los humanos con defectos en el gen portador de hierro-azufre, una condición fatal, tienen deficiencias de ácido lipoico.
"LipA se canibaliza para proporcionar los átomos de azufre necesarios para la producción de ácido lipoico, "dijo Squire Booker, profesor de química y de bioquímica y biología molecular en Penn State University, un investigador del Instituto Médico Howard Hughes, y el autor correspondiente del trabajo de investigación. "Cuando demostramos esto en 2011, era desconcertante porque si se destruye LipA, ¿Cómo podría la célula producir suficiente ácido lipoico? "
LipA es un miembro de la familia de enzimas de radicales SAM (S-adenosilmetionina). Como la mayoría de las enzimas SAM radicales, contiene un grupo de cuatro átomos de hierro y cuatro de azufre, que utiliza para convertir SAM en un radical de alta energía. Sucesivamente, ese radical puede eliminar átomos de hidrógeno de otras moléculas, un paso necesario para activar muchas reacciones metabólicas celulares importantes. Los átomos de hidrógeno se reemplazan con azufre para completar el proceso.
De dónde provienen los átomos de azufre que utiliza LipA para producir ácido lipoico y cómo se unen han sido cuestiones importantes en el campo. Se comprende bastante bien cómo otras enzimas unen átomos de oxígeno a los centros de carbono inerte. En esos casos, oxígeno, que está omnipresente en la atmósfera, se utiliza para crear radicales de alta energía y también es la fuente del átomo de oxígeno adjunto. Azufre, por otra parte, no está disponible de manera similar, pero a diferencia de la mayoría de las otras enzimas SAM radicales, LipA tiene un grupo adicional de hierro-azufre.
"Sabíamos por un trabajo anterior que LipA utilizaba su segundo grupo de hierro y azufre como fuente de átomos de azufre para crear ácido lipoico, "dijo Erin L. McCarthy, estudiante de posgrado en el laboratorio de Booker y primer autor del artículo. "Pero esto creó un problema. Si LipA robó átomos de azufre de su propio grupo de hierro-azufre, la enzima se destruiría y, por lo tanto, no podría crear más ácido lipoico. Cuando supimos que los humanos con genes NFU1 defectuosos, el equivalente humano del gen bacteriano NfuA utilizado en nuestros experimentos, tenía deficiencias en ácido lipoico, pensamos que este portador de hierro-azufre podría estar reemplazando el grupo de hierro-azufre consumido en LipA, lo que le permite seguir produciendo ácido lipoico ".
Para probar esta hipótesis, los investigadores realizaron dos experimentos clave. Primero, probaron si LipA y NfuA se asocian entre sí evaluando qué tan rápido migran las moléculas a través de un gel mediante una técnica llamada cromatografía de filtración en gel. En esta técnica, las moléculas grandes migran más rápido que las moléculas más pequeñas. Cuando se combinaron LipA y NfuA y luego se analizaron mediante esta técnica, migraron más rápido que cualquier molécula por sí sola, sugiriendo que las dos moléculas estaban unidas para formar una Molécula de migración más rápida. Luego, los investigadores crearon una versión de NfuA que contenía una forma ligeramente diferente de átomos de azufre (34S en lugar de 32S), una forma que podrían rastrear si se incorporara en LipA y luego en ácido lipoico. En este segundo experimento, los investigadores demostraron que después de que el 32S originalmente presente en LipA se consumiera en la reacción química para producir ácido lipoico, se produjo ácido lipoico que contiene 34S, que solo podría provenir de su NfuA diseñado.
"Hemos estado interesados durante bastante tiempo tanto en el proceso que agrega azufre a un compuesto de carbono inerte para producir ácido lipoico como en la fuente del azufre agregado, "dijo Booker." El ácido lipoico es un componente vital de los procesos metabólicos básicos que mantienen vivas nuestras células. Comprender la reacción que la crea no solo nos permite comprender mejor este proceso, también nos da una idea de las enfermedades humanas como la causada por mutaciones en NFU1 que resultan en deficiencia de ácido lipoico y muerte ".