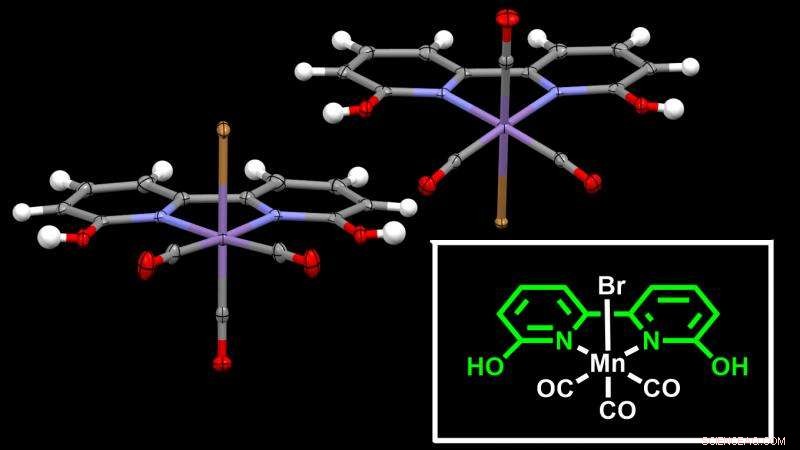
Estructura cristalina del catalizador a base de manganeso informado en el estudio. El átomo de manganeso (en púrpura) está en el centro del marco, el ligando, lo que facilita la hidrogenación del CO2. Crédito:Instituto de Ciencia y Tecnología de Okinawa
Los investigadores de OIST desarrollaron catalizadores simples basados en manganeso abundante en la Tierra para usar dióxido de carbono para el almacenamiento de energía o convertirlo en productos químicos útiles para la industria.
El dióxido de carbono (CO2) se conoce como gas de efecto invernadero y desempeña un papel fundamental en el cambio climático; No es de extrañar que los científicos hayan estado buscando soluciones para evitar su liberación en el medio ambiente. Sin embargo, como barato, fuente de carbono fácilmente disponible y no tóxica, En los últimos años se han realizado esfuerzos para convertir el dióxido de carbono en mercancías valiosas, o productos de "valor añadido".
Por ejemplo, El dióxido de carbono permite el almacenamiento de energía al reaccionar con hidrógeno gaseoso, llamado proceso de hidrogenación, transformando la mezcla en compuestos líquidos de mayor energía, como el metanol, que pueden transportarse y usarse fácilmente como combustible para automóviles. Similar, La hidrogenación de dióxido de carbono en presencia de otros productos químicos puede conducir a la formación de varios productos de valor agregado ampliamente utilizados en la industria, como el ácido fórmico. formamidas, o formaldehído. Estos productos químicos también se pueden usar potencialmente para el almacenamiento de energía como, por ejemplo, calentar ácido fórmico en determinadas condiciones permite la liberación de gas hidrógeno de forma controlada y reversible.
La conversión de dióxido de carbono en productos útiles se complica por el hecho de que el CO2 es la forma de carbono más oxidada y, como tal, una molécula muy estable y no reactiva. Por lo tanto, la reacción directa del CO2 con el hidrógeno requiere mucha energía, haciendo el proceso económicamente desfavorable. Este problema se puede solucionar utilizando catalizadores, que son compuestos que se utilizan en pequeñas cantidades para acelerar las reacciones químicas. Para fines de hidrogenación de CO2, Los catalizadores más conocidos se basan en metales preciosos como el iridio, rodio o rutenio. Si bien son excelentes catalizadores, la escasez de estos metales preciosos dificulta su uso a escala industrial. También son difíciles de reciclar y potencialmente tóxicos para el medio ambiente. Otros catalizadores utilizan metales más baratos como el hierro o el cobalto, pero requieren una molécula a base de fósforo, llamada fosfina, que rodea al metal. Las fosfinas no siempre son estables alrededor del oxígeno y, a veces, arden violentamente en una atmósfera de aire. lo que presenta otro problema para las aplicaciones prácticas.
Para superar estos problemas, la Unidad de Coordinación de Química y Catálisis de la OIST dirigida por la profesora Julia Khusnutdinova informó en Catálisis ACS Catalizadores novedosos y eficientes basados en un metal abundante y económico:el manganeso. El manganeso es el tercer metal más abundante en la corteza terrestre después del titanio y el hierro. y presenta una toxicidad mucho menor en comparación con muchos otros metales utilizados en la hidrogenación de CO2.
Los científicos inicialmente buscaron inspiración en el mundo natural:la hidrogenación es una reacción que ocurre en muchos organismos que no tendrían acceso a metales preciosos o fosfinas. Observaron la estructura de enzimas específicas, hidrogenasas, para comprender cómo podrían lograr la hidrogenación usando simples, Materiales abundantes en la tierra. Para facilitar la hidrogenación, Las enzimas utilizan una disposición "inteligente" en la que la estructura orgánica circundante coopera con un átomo de metal, como el hierro, para iniciar la reacción de manera eficiente.
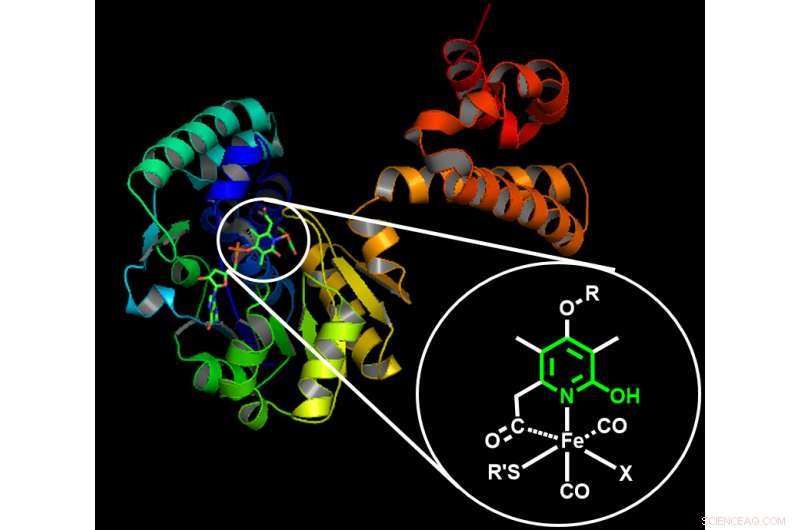
Estructura de una hidrogenasa a base de hierro natural. La estructura de las enzimas naturales inspiró a los científicos a diseñar un marco artificial eficiente para un catalizador a base de manganeso. El inserto muestra la estructura química propuesta responsable de la activación del hidrógeno. Estructura de una hidrogenasa a base de hierro natural. La estructura de las enzimas naturales inspiró a los científicos a diseñar un marco artificial eficiente para un catalizador a base de manganeso. El inserto muestra la estructura química propuesta responsable de la activación del hidrógeno. Crédito:Instituto de Ciencia y Tecnología de Okinawa
"Después de analizar las hidrogenasas, Queríamos comprobar si podíamos fabricar moléculas artificiales que imitaran estas enzimas utilizando el mismo tipo de materiales comunes. como el hierro y el manganeso, "explicó el Dr. Abhishek Dubey, el primer autor de este estudio.
El principal desafío de este estudio fue construir un marco adecuado, llamado ligando, alrededor del manganeso para inducir la hidrogenación. Los científicos encontraron una estructura de ligando sorprendentemente simple que se asemeja a las enzimas hidrogenasas naturales con un giro de los típicos catalizadores de fosfina.
"En la mayoría de los casos, los ligandos sostienen el metal sin participar directamente en la activación de un enlace químico. En nuestro caso, creemos que el ligando participa directamente en la reacción, "dijo el Dr. Dubey.
En el diseño de ligandos, la estructura de un ligando está estrechamente ligada a su eficacia. El nuevo catalizador, el ligando y el manganeso juntos, puede realizar más de 6, 000 pérdidas de balón en una reacción de hidrogenación, convertir más de 6, 000 veces las moléculas de CO2 antes de descomponerse. Y este nuevo ligando, el resultado de una colaboración con un equipo internacional que incluye al Prof.Carlo Nervi y al Sr. Luca Nencini de la Universidad de Turín en Italia y al Dr. Robert Fayzullin de Rusia, es fácil de fabricar y estable en el aire.
Por ahora, el catalizador es capaz de transformar el dióxido de carbono en ácido fórmico, un conservante de alimentos y un agente curtiente ampliamente utilizado, y formamida, que tiene aplicaciones industriales. Pero la versatilidad de este catalizador abre muchas otras posibilidades.
"Nuestro próximo objetivo es utilizar una estructura tan simple, catalizadores de manganeso económicos para apuntar a otros tipos de reacciones en las que el CO2 y el hidrógeno se pueden convertir en productos químicos orgánicos útiles ", concluyó la profesora Khusnutdinova.