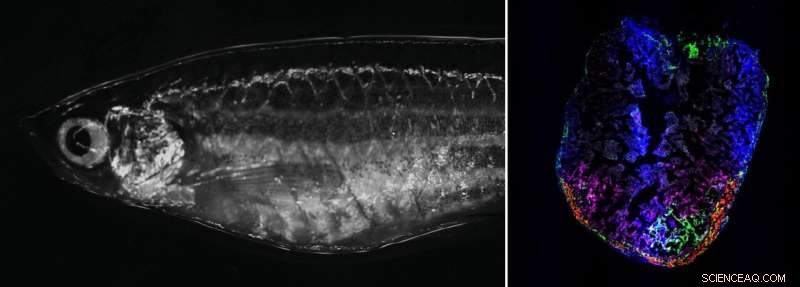
Derecha:pez cebra adulto en el microscopio de campo claro. Izquierda:corazón de pez cebra 7 días después de la criolesión. Los fibroblastos activados transitoriamente se localizan en el área de la lesión. Crédito:Laboratorio Panáková, MDC
Un equipo de investigación del MDC dirigido por Jan Philipp Junker y Daniela Panáková descubrió que el pez cebra puede regenerar el tejido cardíaco después de una lesión. Las células del tejido conectivo juegan un papel importante en el proceso al entrar temporalmente en un estado activado, como informa el equipo en Nature Genetics. .
Cuando una persona sufre un infarto y no recibe tratamiento con la suficiente rapidez, las células del músculo cardíaco (cardiomiocitos) se dañan por falta de oxígeno y comienzan a morir. Luego se forma tejido cicatricial y, debido a que no podemos producir nuevos cardiomiocitos, el corazón ya no puede bombear tan bien como debería. Las cosas son muy diferentes en los vertebrados inferiores como el pez cebra, que puede regenerar órganos, incluido su corazón.
"Queríamos saber cómo hace eso este pececito y si podíamos aprender de ello", dice el profesor Jan Philipp Junker, director del Laboratorio de Biología del Desarrollo Cuantitativo del Instituto de Biología de Sistemas Médicos de Berlín (BIMSB), parte del Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC) en Berlín. Trabajando con la Dra. Daniela Panáková, quien dirige el Laboratorio de Señalización Electroquímica en Desarrollo y Enfermedades en el MDC, los investigadores simularon lesiones de infarto de miocardio en los corazones de sus peces cebra. Usando análisis de células individuales y árboles de linaje celular, rastrearon la regeneración de los cardiomiocitos. Ahora han publicado sus observaciones en la revista Nature Genetics .
Los corazones humanos no llegan a regenerarse
Los investigadores comenzaron colocando una aguja fría en el corazón del tamaño de un milímetro del pez cebra durante unos segundos bajo un microscopio. La aguja mata cualquier tejido que toca. Al igual que en los pacientes humanos con ataques cardíacos, esto provoca una respuesta inflamatoria, seguida de una cicatrización de las células del tejido conectivo conocidas como fibroblastos. "Sorprendentemente, la respuesta inmediata a la lesión es muy similar. Pero mientras que el proceso en los humanos se detiene en ese punto, continúa en los peces. Forman nuevos cardiomiocitos, que son capaces de contraerse", dice Junker.
"Queríamos identificar las señales que provienen de otras células y ayudar a impulsar la regeneración", continúa. El equipo de Junker utilizó genómica unicelular para buscar en el corazón lesionado células que no existen en un corazón de pez cebra sano. Encontraron tres nuevos tipos de fibroblastos que entran temporalmente en un estado activado. Aunque son externamente idénticas a los otros fibroblastos, estas células activadas pueden leer toda una serie de genes adicionales que son responsables de formar proteínas, como factores de tejido conectivo como el colágeno 12.
Los fibroblastos dan la señal para la regeneración
En los humanos, la cicatrización (o fibrosis) se considera un obstáculo para la regeneración del corazón. Pero los fibroblastos parecen ser importantes para el proceso tan pronto como entran en su estado activado temporalmente. Su importancia quedó clara cuando Panáková usó un truco genético para desactivar los fibroblastos que expresan colágeno 12 en el pez cebra. El resultado:ninguna regeneración. Junker cree que tiene sentido que los fibroblastos sean responsables de dar las señales de reparación:"Después de todo, se forman justo en el sitio de la lesión", dice.
Para identificar la fuente de estos fibroblastos activados, el equipo de Junker produjo árboles de linaje celular utilizando una técnica llamada LINNAEUS, que su laboratorio desarrolló en 2018. LINNAEUS trabaja con cicatrices genéticas que actúan colectivamente como un código de barras para el origen de cada célula. "Creamos este código de barras usando tijeras genéticas CRISPR-Cas9. Si, después de la lesión, dos células tienen la misma secuencia de código de barras, significa que están relacionadas", explica Junker. Los investigadores identificaron dos fuentes de fibroblastos activados temporalmente:la capa externa del corazón (epicardio) y la capa interna (endocardio). Las células productoras de colágeno 12 se encontraron exclusivamente en el epicardio.
Distintas disciplinas colaboraron estrechamente en el estudio
Múltiples investigadores del MDC colaboraron a lo largo del estudio, desde los experimentos con los peces hasta los análisis genéticos y la interpretación bioinformática de los resultados. "Para mí, lo más emocionante fue ver qué tan bien se complementan nuestras disciplinas y cómo podíamos verificar los resultados de la bioinformática en un animal vivo", dice Sara Lelek, autora principal del estudio y responsable del animal. pruebas "Fue un gran proyecto que nos permitió a todos contribuir con nuestra experiencia. Creo que es por eso que el estudio es tan completo y tan útil para muchos investigadores".
El Dr. Bastiaan Spanjaard, también autor principal, está de acuerdo:"Debido a que teníamos áreas de experiencia tan diferentes, a menudo teníamos que explicarnos nuestros experimentos y análisis. La regeneración del corazón es un proceso complejo que está influenciado por muchas cosas diferentes. Los experimentos produjo enormes cantidades de datos. Filtrar las señales biológicas correctas de ellos fue un gran desafío".
Todavía no está claro si los corazones dañados en mamíferos como humanos y ratones carecen de las señales necesarias o de la capacidad de leer las señales. Si faltan las señales, eventualmente se podrían desarrollar medicamentos para simularlas. Pero, dice Junker, encontrar una manera de imitar la interpretación de señales sería mucho más difícil.
Los fibroblastos también ayudan a formar nuevos vasos sanguíneos
Los investigadores ahora quieren observar más de cerca los genes que los fibroblastos activados temporalmente leen con especial frecuencia. Saben que muchos de los genes en cuestión son importantes para liberar proteínas en el área circundante. Y estos podrían incluir factores que también influyen en los cardiomiocitos. Y la evidencia inicial sugiere que los fibroblastos activados no solo promueven la regeneración del corazón; también ayudan a formar nuevos vasos sanguíneos que suministran oxígeno al corazón.