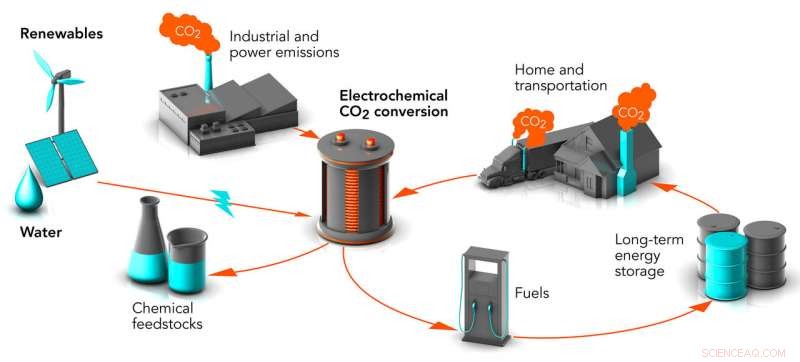
Los investigadores de Stanford y SLAC están trabajando en formas de convertir el dióxido de carbono (CO2) residual en materias primas químicas y combustibles. convertir un potente gas de efecto invernadero en productos valiosos. El proceso se llama conversión electroquímica. Cuando se alimenta con fuentes de energía renovables, podría reducir los niveles de dióxido de carbono en el aire y almacenar energía de estas fuentes intermitentes en una forma que se puede utilizar en cualquier momento. Crédito:Greg Stewart / SLAC National Accelerator Laboratory
Una forma de reducir el nivel de dióxido de carbono en la atmósfera, que ahora está en su punto más alto en 800, 000 años, sería capturar el potente gas de efecto invernadero de las chimeneas de las fábricas y plantas de energía y usar energía renovable para convertirlo en cosas que necesitamos, dice Thomas Jaramillo.
Como director del Centro SUNCAT de Ciencia y Catálisis de Interfaces, un instituto conjunto de la Universidad de Stanford y el Laboratorio Nacional Acelerador SLAC del Departamento de Energía, está en condiciones de ayudar a que eso suceda.
Un enfoque principal de la investigación de SUNCAT es encontrar formas de transformar el CO 2 en productos químicos, combustibles y otros productos, del metanol a los plásticos, detergentes y gas natural sintético. La producción de estos productos químicos y materiales a partir de ingredientes de combustibles fósiles ahora representa el 10% de las emisiones globales de carbono; la producción de gasolina, diesel, y el combustible para aviones representa mucho, mucho más.
"Ya hemos emitido demasiado CO 2 , y estamos en camino de seguir emitiéndolo durante años, Dado que el 80% de la energía consumida en todo el mundo en la actualidad proviene de combustibles fósiles, "dice Stephanie Nitopi, cuya investigación SUNCAT es la base de su recién adquirido doctorado en Stanford.
"Podrías capturar CO 2 de las chimeneas y almacenarlo bajo tierra, ", dice." Esa es una tecnología actualmente en juego. Una alternativa es usarlo como materia prima para fabricar combustibles, plástica, y productos químicos especiales, que cambia el paradigma financiero. Residuos de CO 2 las emisiones ahora se convierten en algo que puede reciclar en productos valiosos, proporcionando un nuevo incentivo para reducir la cantidad de CO 2 liberado a la atmósfera. Eso es beneficioso para todos ".
Le preguntamos a Nitopi, Jaramillo, El científico del personal de SUNCAT, Christopher Hahn, y la investigadora postdoctoral Lei Wang, para que nos digan en qué están trabajando y por qué es importante.
P. Primero lo básico:¿Cómo se convierte CO 2 en estos otros productos?
Tom:Es esencialmente una forma de fotosíntesis artificial, razón por la cual el Centro Conjunto de Fotosíntesis Artificial del DOE financia nuestro trabajo. Las plantas utilizan energía solar para convertir CO 2 del aire al carbono en sus tejidos. Similar, queremos desarrollar tecnologías que utilicen energías renovables, como el sol o el viento, convertir CO 2 de emisiones industriales a productos a base de carbono.
Chris:Una forma de hacer esto se llama CO electroquímico. 2 reducción, donde burbujeas CO 2 gas a través del agua y reacciona con el agua en la superficie de un electrodo a base de cobre. El cobre actúa como catalizador, juntar los ingredientes químicos de una manera que los anime a reaccionar. En pocas palabras, la reacción inicial quita un átomo de oxígeno del CO 2 para formar monóxido de carbono, o CO, que es una sustancia química industrial importante por derecho propio. Luego, otras reacciones electroquímicas convierten el CO en moléculas importantes como los alcoholes, combustibles y otras cosas.
Hoy en día, este proceso requiere un catalizador a base de cobre. Es el único conocido que hace el trabajo. Pero estas reacciones pueden producir numerosos productos, y separar el que quieres es costoso, por lo que necesitamos identificar nuevos catalizadores que sean capaces de guiar la reacción hacia la fabricación únicamente del producto deseado.
¿Cómo es eso?
Lei:cuando se trata de mejorar el rendimiento de un catalizador, uno de los aspectos clave que analizamos es cómo hacerlos más selectivos, por lo que generan un solo producto y nada más. Aproximadamente el 90 por ciento de la fabricación de combustibles y productos químicos depende de catalizadores, y deshacerse de los subproductos no deseados es una gran parte del costo.
También analizamos cómo hacer que los catalizadores sean más eficientes aumentando su área de superficie, por lo que hay muchos más lugares en un volumen dado de material donde las reacciones pueden ocurrir simultáneamente. Esto aumenta la tasa de producción.
Recently we discovered something surprising:When we increased the surface area of a copper-based catalyst by forming it into a flaky "nanoflower" shape, it made the reaction both more efficient and more selective. De hecho, it produced virtually no byproduct hydrogen gas that we could measure. So this could offer a way to tune reactions to make them more selective and cost-competitive.
Stephanie:This was so surprising that we decided to revisit all the research we could find on catalyzing electrochemical CO 2 conversion with copper, and the many ways people have tried to understand and fine-tune the process, using both theory and experiments, going back four decades. There's been an explosion of research on this—about 60 papers had been published as of 2006, versus more than 430 out there today—and analyzing all the studies with our collaborators at the Technical University of Denmark took two years.
We were trying to figure out what makes copper special, why it's the only catalyst that can make some of these interesting products, and how we can make it even more efficient and selective—what techniques have actually pushed the needle forward? We also offered our perspectives on promising research directions.
One of our conclusions confirms the results of the earlier study:The copper catalyst's surface area can be used to improve both the selectivity and overall efficiency of reactions. So this is well worth considering as a chemical production strategy.
Does this approach have other benefits?
Tom:Absolutely. If we use clean, renewable energy, like wind or solar, to power the controlled conversion of waste CO 2 to a wide range of other products, this could actually draw down levels of CO 2 in the atmosphere, which we will need to do to stave off the worst effects of global climate change.
Chris:And when we use renewable energy to convert CO 2 to fuels, we're storing the variable energy from those renewables in a form that can be used any time. Además, with the right catalyst, these reactions could take place at close to room temperature, instead of the high temperatures and pressures often needed today, making them much more energy efficient.
How close are we to making it happen?
Tom:Chris and I explored this question in a recent Perspective article in Ciencias , written with researchers from the University of Toronto and TOTAL American Services, which is an oil and gas exploration and production services firm.
We concluded that renewable energy prices would have to fall below 4 cents per kilowatt hour, and systems would need to convert incoming electricity to chemical products with at least 60% efficiency, to make the approach economically competitive with today's methods.
Chris:This switch couldn't happen all at once; the chemical industry is too big and complex for that. So one approach would be to start with making high-value, high-volume products like ethylene, which is used to make alcohols, polyester, antifreeze, plastics and synthetic rubber. It's a $230 billion global market today. Switching from fossil fuels to CO 2 as a starting ingredient for ethylene in a process powered by renewables could potentially save the equivalent of about 860 million metric tons of CO 2 emissions per year.
The same step-by-step approach applies to sources of CO 2 . Industry could initially use relatively pure CO 2 emissions from cement plants, breweries or distilleries, por ejemplo, and this would have the side benefit of decentralizing manufacturing. Every country could provide for itself, develop the technology it needs, and give its people a better quality of life.
Tom:Once you enter certain markets and start scaling up the technology, you can attack other products that are tougher to make competitively today. What this paper concludes is that these new processes have a chance to change the world.