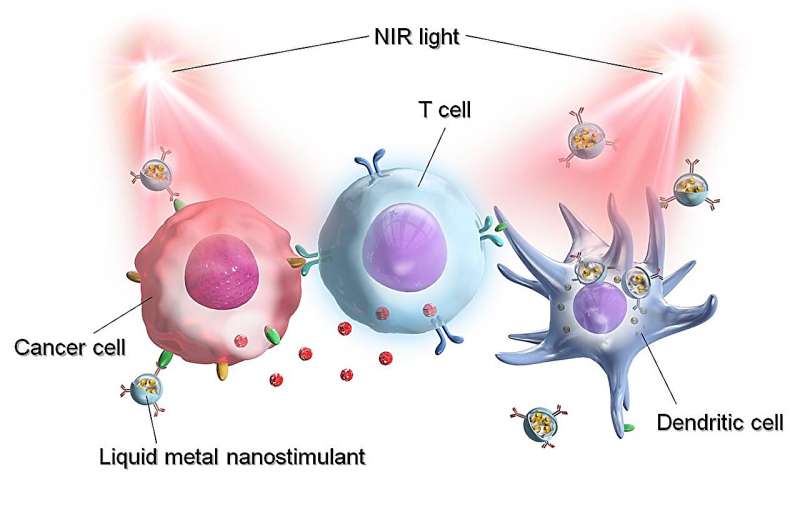
Los metales líquidos (LM), como el galio puro (Ga) y las aleaciones a base de Ga, son una nueva clase de materiales con propiedades fisicoquímicas únicas. Una de las aplicaciones más destacadas de los LM es la terapia fototérmica contra el cáncer, en la que las nanopartículas funcionales de LM convierten la energía luminosa en energía térmica, matando así las células cancerosas. La fototerapia basada en LM es superior a la terapia tradicional contra el cáncer debido a su alta especificidad, repetibilidad y bajos efectos secundarios.
En un nuevo estudio de vanguardia, el profesor asociado Eijiro Miyako y sus colegas del Instituto Avanzado de Ciencia y Tecnología de Japón (JAIST) sintetizaron nanopartículas multifuncionales basadas en Ga que combinan fototerapia contra el cáncer con inmunoterapia.
La nueva nanopartícula LM sintetizada (PEG-IMIQ-LM) contiene una aleación LM eutéctica de galio-indio (EGaIn) y un modulador inmunológico imiquimod (IMIQ), ambos integrados dentro de un tensioactivo biocompatible DSPE-PEG2000. -NH2 . Los hallazgos de su estudio se publicaron en Advanced Functional Materials. .
"Creemos que la convergencia de la nanoingeniería y la tecnología LM podría proporcionar una modalidad prometedora para desencadenar respuestas inmunes ideales para avanzar en la inmunoterapia contra el cáncer. En este estudio, informamos nanopartículas LM multifuncionales activables por luz con inmunoestimulantes para combinar la terapia fototérmica con la inmunoterapia. " dice el Dr. Miyako, mientras habla de la motivación del equipo para realizar este estudio.
En primer lugar, el equipo de investigación preparó nanopartículas LM dispersables en agua mediante un sencillo proceso de sonicación de un solo paso utilizando DSPE-PEG2000. -NH2 para introducir IMIQ. Esto se considera un gran avance, ya que EGaIn LM es inherentemente un material inmiscible en agua.
Investigaciones adicionales confirmaron que LM se desintegra para garantizar la entrega de IMIQ al objetivo. Además, la nanopartícula preparada mostró un aumento lineal en la absorbancia en la región del infrarrojo cercano (NIR) a 808 nm, lo que confirma su naturaleza ópticamente activable.
Cuando la solución acuosa de la nanopartícula LM fue irradiada por el láser NIR (808 nm), el equipo observó un aumento notable en la temperatura de la solución, que era proporcional al aumento en la concentración de la nanopartícula. Estos hallazgos confirmaron que la nanopartícula PEG-IMIQ-LM era un portador de fármaco fototérmico robusto y estable, adecuado para inmunoterapia.
Experimentos adicionales revelaron que las nanopartículas LM eran extremadamente seguras y no causaban citotoxicidad en fibroblastos humanos (MRC5) ni en células de cáncer de colon de ratón (Colon26).
Para evaluar el grado de internalización y distribución de las partículas, se introdujo en la partícula un tinte fluorescente conocido como verde de indocianina (ICG) mediante sonicación, lo que dio como resultado la partícula PEG-ICG-IMIQ-LM. La microscopía fluorescente (FL) equipada con un rayo láser demostró que la partícula LM mostraba una fuerte fluorescencia en varias longitudes de onda NIR e inmediatamente destruyó las células Colon26. Por lo tanto, las partículas LM no solo podrían administrar eficientemente el inmunomodulador, sino que también podrían permitir su seguimiento en tiempo real y eliminar células cancerosas específicas.
Finalmente, el equipo desarrolló un nanoestimulador inmunológico LM multifacético para la terapia del cáncer. Para hacerlo, agregaron el anticuerpo anti-ligando de muerte programada 1 (Anti-PD-L1), uno de los inhibidores de puntos de control inmunológico más prometedores, a la nanopartícula fluorescente LM existente. La partícula modificada, Anti-PD-L1‒PEG–ICG–IMIQ–LM, se dispersó eficientemente con una fluorescencia significativa. Con el aumento del tiempo posterior a la irradiación, la temperatura de la superficie del tumor aumentó linealmente, lo que indica el efecto antitumoral de la nanopartícula.
La adición de Anti-PD-L1 a la nanopartícula permitió la unión de la partícula LM a PD-L1 en las células cancerosas, marcándolas para la fagocitosis por macrófagos y células dendríticas (DC). Las partículas Anti-PD-L1–PEG–IMIQ–LM inducidas por láser exhibieron la eliminación más alta y completa del cáncer, junto con una curación y recuperación más rápidas.
Además, cuando el tumor reapareció, los ratones tratados con partículas Anti-PD-L1–PEG–IMIQ–LM inducidas por láser mostraron una eficacia antitumoral sostenida y una supervivencia prolongada.
Mientras analiza las implicaciones futuras del estudio, el Dr. Miyako dice:"Creemos que estos efectos inmunológicos sinérgicos y las nanofunciones ópticas de los LM tienen amplias aplicaciones terapéuticas y podrían contribuir a tecnologías teranósticas innovadoras contra el cáncer. Tenemos la esperanza de que esta tecnología esté disponible para ensayos clínicos en 10 años."
Más información: Yun Qi et al, Inmunoestimulantes de metales líquidos activables por luz para nanoteranósticos del cáncer, Materiales funcionales avanzados (2023). DOI:10.1002/adfm.202305886
Información de la revista: Materiales funcionales avanzados
Proporcionado por el Instituto Avanzado de Ciencia y Tecnología de Japón