Investigadores de la Universidad de Yale, New Haven, optimizaron un vehículo de ARNm basado en polímeros para su administración pulmonar dirigida y demostraron el potencial de la plataforma para la vacunación de las mucosas contra patógenos respiratorios.
En un artículo, "Las nanopartículas poliméricas administran ARNm al pulmón para la vacunación de las mucosas", publicado en Science Translational Medicine , el equipo presenta su creación de ARN mensajero inhalable (ARNm) para uso terapéutico.
La investigación clínica ha estado buscando una forma eficiente y específica de administrar ARNm a los pulmones para diversas aplicaciones terapéuticas, incluidas terapias de reemplazo de proteínas, edición de genes y vacunación. Los principales desafíos han sido mantener la estabilidad del ARNm y evitar la interferencia inmune.
El equipo de Yale creó formulaciones de polímeros PACE (conjugados de albúmina polimerizada para encapsulación de ARNm) para administrar ARNm local a los pulmones. Los investigadores optimizaron los poliplex PACE para mejorar la protección del ARNm, la eficiencia de la transfección y la presentación de antígenos para estrategias terapéuticas y de vacunación eficaces específicas de los pulmones.
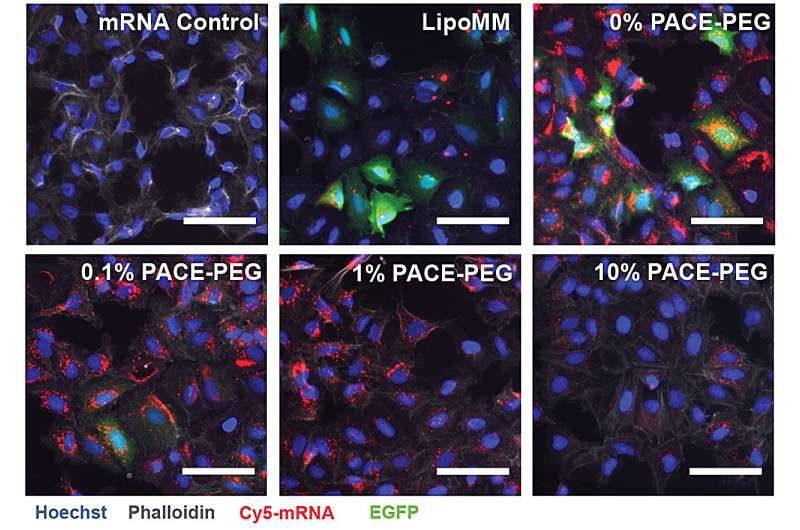
Para estabilizar PACE, se integró una proporción optimizada de moléculas de polietilenglicol (PEG) en la estructura del polímero durante el proceso de copolimerización enzimática, lo que estabilizó los poliplex y modificó las características clave. El PEG pudo afectar el tamaño, la carga superficial y otras propiedades de los poliplex, haciéndolos más adecuados para la carga y eficaces en la entrega de ARNm a las células pulmonares.
La formulación estabilizada tuvo un rendimiento deficiente en un experimento de cultivo celular in vitro. Los investigadores señalan que los métodos tradicionales de cultivo celular no son buenos predictores de los sistemas de administración, ni positiva ni negativamente. El entorno dentro del cuerpo, especialmente los pulmones, interactúa de manera muy diferente a un conjunto de células. Por ejemplo, faltan las superficies mucosas, y esas superficies son exactamente para las que está diseñado el sistema PACE-PEG. La prueba real se realizaría in vivo con un modelo de ratón.
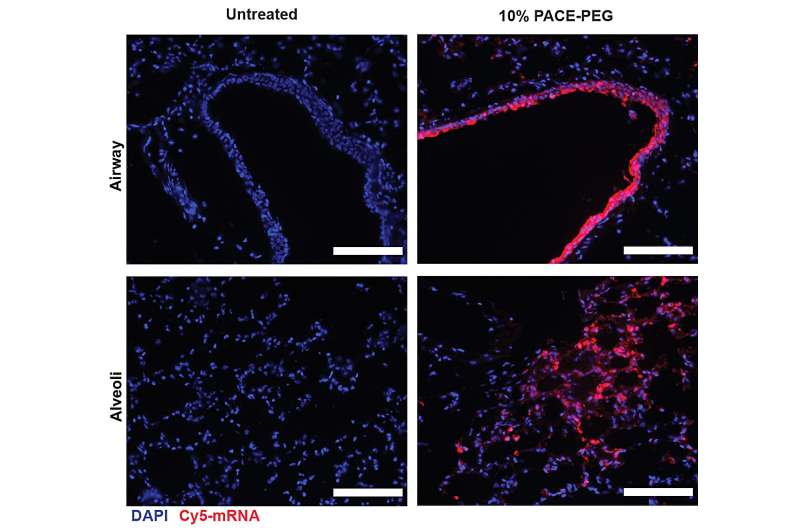
Los investigadores encapsularon ARNm que codifica la proteína de pico del SARS-CoV-2 en PACE e inocularon ratones susceptibles a la infección por SARS-CoV-2. Los ratones recibieron una dosis de 10 μg de ARNm de PACE administrada por vía intranasal los días 0 y 28. El desarrollo de inmunidad adaptativa en los ganglios linfáticos mediastínicos se probó y confirmó 14 días después del refuerzo.
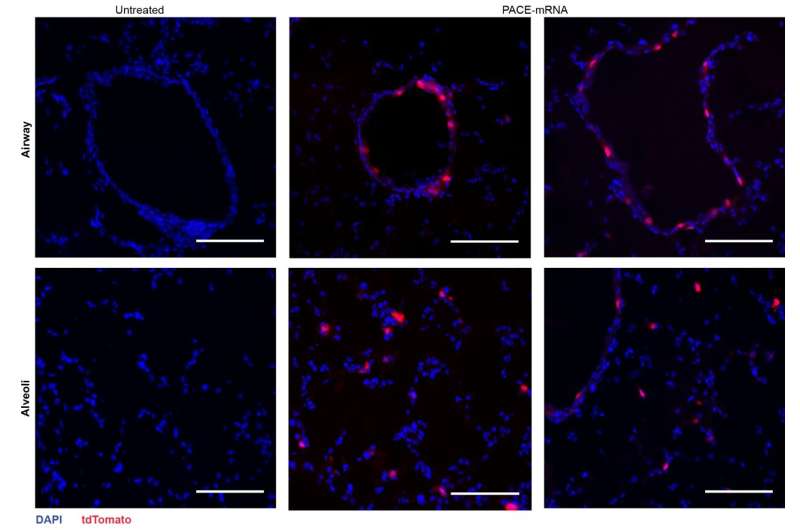
Después de evaluar la respuesta inmune local, los investigadores examinaron los tejidos pulmonares, el suero sanguíneo y el líquido de lavado broncoalveolar en busca de respuestas de anticuerpos y células T específicas de antígeno locales y sistémicos. La transfección se produjo principalmente en células epiteliales pulmonares y células presentadoras de antígenos, dos tipos de células que son objetivos relevantes para las enfermedades pulmonares
La vacunación aumentó con éxito el CD8 + específico de la proteína Spike Células T en el tejido pulmonar y CD8 circulantes + Células T en el torrente sanguíneo. CD8 + Las células T expresaron marcadores indicativos de memoria residente en el tejido. Se encontraron anticuerpos IgG tanto circulantes como mucosos en concentraciones significativamente más altas en ratones vacunados.
Luego se introdujo a los ratones una dosis letal de SARS-CoV-2. La vacunación con PACE-mRNA redujo significativamente la carga viral en los pulmones y mejoró el peso y la supervivencia de los ratones vacunados. Esta protección se atribuyó a la respuesta inmune específica de la proteína de pico inducida por la vacunación.
El grupo de control no mostró evidencia de una respuesta inmune específica de la proteína de pico y no mostró una carga viral reducida ni una mejor supervivencia después del desafío viral.
El estudio presenta los poliplexes de ARNm de PACE como un método prometedor para la entrega eficiente y dirigida de ARNm a los pulmones con beneficios potenciales tanto para la expresión de proteínas terapéuticas como para la vacunación de las mucosas contra patógenos respiratorios.
El estudio también ilustra la importancia de los modelos animales, a diferencia del cultivo celular únicamente, para determinar los efectos en el mundo real. Los resultados positivos indican que se necesita más investigación y se planean más pruebas en modelos animales más grandes.
Más información: Alexandra Suberi et al, Las nanopartículas poliméricas administran ARNm al pulmón para la vacunación de las mucosas, Ciencia y medicina traslacional (2023). DOI:10.1126/scitranslmed.abq0603
Información de la revista: Ciencia Medicina Traslacional
© 2023 Red Ciencia X