Los trastornos autoinmunes se encuentran entre las enfermedades crónicas más prevalentes en todo el mundo. Los tratamientos emergentes para los trastornos autoinmunes se centran en "terapias celulares adoptivas", o aquellas que utilizan células del propio cuerpo del paciente para lograr la inmunosupresión. Estas células terapéuticas son reconocidas por el cuerpo del paciente como "propias", lo que limita los efectos secundarios, y están diseñadas específicamente para localizar el efecto terapéutico deseado.
En el tratamiento de enfermedades autoinmunes, las terapias celulares adoptivas actuales se han centrado en gran medida en las células T reguladoras (Treg ), que se define por la expresión de la proteína 3 de la caja Forkhead, o Foxp3. Aunque Tregs ofrecen un gran potencial, utilizarlos con fines terapéuticos sigue siendo un gran desafío. En particular, los métodos de administración actuales dan como resultado una ingeniería ineficiente de las células T.
Treglas Sólo componen aproximadamente entre el 5% y el 10% de las células mononucleares circulantes en sangre periférica. Además, Tregs Carecen de marcadores de superficie más específicos que los diferencien de otras poblaciones de células T. Estos obstáculos dificultan la cosecha, purificación y cultivo de Tregs a cifras terapéuticamente relevantes. Aunque existen Tregs adicionales residentes en tejidos en órganos no linfoides como el músculo esquelético y el tejido adiposo visceral, estos Tregs son muy inaccesibles y son pocos.
Ahora, un equipo de investigación dirigido por Michael Mitchell, profesor asociado de Bioingeniería en la Facultad de Ingeniería y Ciencias Aplicadas de la Universidad de Pensilvania, ha desarrollado una plataforma de nanopartículas lipídicas (LNP) para entregar ARN mensajero (ARNm) de Foxp3 a las células T para aplicaciones. en autoinmunidad. Sus hallazgos se publican en la revista Nano Letters. .

"Los principales desafíos asociados con la ingeniería celular ex vivo (fuera del cuerpo) son la eficiencia, la toxicidad y la ampliación:nuestras nanopartículas lipídicas de ARNm (LNP de ARNm) nos permiten superar todos estos problemas", dice Mitchell. "La novedad de nuestro trabajo proviene de tres componentes principales:primero, el uso de ARNm, que permite la generación de células inmunosupresoras transitorias; segundo, el uso de LNP, que permiten la administración efectiva de ARNm y una ingeniería celular eficiente; y por último, la Ingeniería ex vivo de células T humanas primarias para enfermedades autoinmunes, lo que ofrece la vía más directa para la traducción clínica de esta terapia desde el laboratorio hasta la cabecera de la cama".
"Hasta donde sabemos, esta es una de las primeras plataformas LNP de ARNm que se ha utilizado para diseñar células T para terapias autoinmunes", continúa. "En términos generales, esta plataforma se puede utilizar para diseñar terapias celulares adoptivas para enfermedades autoinmunes específicas y potencialmente se puede utilizar para crear vías terapéuticas para alergias, trasplantes de órganos y más".
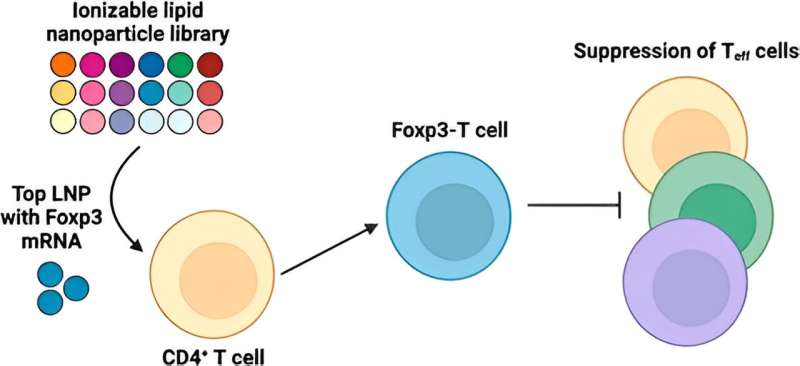
Entregar la proteína Foxp3 a las células T ha sido difícil porque las proteínas no cruzan fácilmente la membrana celular. "El ARNm codifica la proteína Foxp3, que es un factor de transcripción que hace que las células T sean inmunosupresoras en lugar de activas", explica el primer autor Ajay Thatte, estudiante de doctorado y miembro de la NSF en el Laboratorio Mitchell. "Estas células T diseñadas pueden suprimir la función de las células T efectoras, lo cual es importante ya que la hiperactividad de las células T es un fenotipo común en las enfermedades autoinmunes".
Además, el tamaño, la carga y la complejidad relativamente baja del ARNm permiten empaquetarlo fácilmente en sistemas de administración eficaces, como los LNP ionizables, que han demostrado ser una poderosa plataforma de administración, en particular para el ARNm, como lo demuestra el éxito de las vacunas COVID-19. .
En el nuevo estudio, Mitchell y su equipo examinaron primero una biblioteca de 18 LNP únicos para identificar un LNP de alto rendimiento para la entrega de ARNm a células CD4 + humanas. Células T. Luego reformularon este LNP para que el ARNm de Foxp3 generara células Foxp3-T, verificando que las células suprimieran efectivamente la proliferación de células T efectoras. Los resultados demuestran el potencial del uso de LNP de ARNm para diseñar terapias inmunosupresoras basadas en células para enfermedades autoinmunes y más.
En estudios futuros, el equipo planea examinar el efecto supresor de estas células Foxp3-T diseñadas sobre otras células inmunes como los macrófagos y las células dendríticas. Luego esperan transferir las células Foxp3-T diseñadas a modelos de ratón con enfermedades autoinmunes para probar su eficacia y efecto inmunológico. Finalmente, buscarán desarrollar LNP dirigidas a administrar ARNm de Foxp3 a las células T que circulan en el cuerpo, estableciendo una plataforma de ingeniería in situ para terapias de enfermedades autoinmunes.
"Aunque se ha explorado ampliamente en aplicaciones contra el cáncer, la ingeniería de células inmunes fuera del cuerpo ha sido menos explorada para aplicaciones de autoinmunidad. Además, lograr una alta eficiencia y baja toxicidad durante el proceso de ingeniería celular es extremadamente difícil", dice Mitchell. "Nuestra tecnología LNP permite la ingeniería fácil y eficiente de células T con baja toxicidad. Nuestras células T diseñadas se pueden utilizar en una variedad de trastornos inmunológicos hiperactivos".
Más información: Ajay S. Thatte et al, Nanopartículas lipídicas de ARNm para ingeniería ex vivo de células T inmunosupresoras para terapias de autoinmunidad, Nano Letters (2023). DOI:10.1021/acs.nanolett.3c02573
Información de la revista: Nanoletras
Proporcionado por la Universidad de Pensilvania