Desde la revelación de los inhibidores de la poli (ADP-ribosa) polimerasa (PARP) y sus notables resultados en el tratamiento de cánceres mutantes BRCA1/2, la letalidad sintética (SL) en la terapia antitumoral ha atraído cada vez más atención. SL es un fenómeno en el que un único evento genético es insuficiente para inducir la muerte celular, pero múltiples eventos genéticos conducen a la muerte celular.
La caracterización de las interacciones genéticas de SL con mutaciones específicas de tumores se puede utilizar para desarrollar un marco conceptual para abordar objetivos "no farmacológicos" como el gen supresor de tumores p53. El cáncer de vesícula biliar (GBC) es el tumor maligno más prevalente del sistema biliar y suele ser mortal debido a la eficacia limitada del tratamiento existente.
Se ha informado que p53 es uno de los genes mutados con mayor frecuencia y un marcador de mal pronóstico en el GBC. Por lo tanto, una estrategia basada en SL para atacar el GBC con mutación en p53 es un enfoque prometedor.
Un nuevo estudio sobre este tema dirigido por el Prof. Mingyu Chen, el Prof. Xiujun Cai, el Dr. Shjie Li, el Dr. Sarun Juengpanich y el Dr. Win Topatana, todos del Hospital Sir Run-Run Shaw de la Universidad de Zhejiang, y el Prof. Jicheng Yu. de la Facultad de Ciencias Farmacéuticas de la Universidad de Zhejiang aparece en Science Bulletin .
Estudios anteriores han demostrado que la reparación del daño en el ADN lograda por WEE1 mediante la regulación del punto de control G2 del ciclo celular es esencial para la supervivencia de las células mutadas en p53. Por lo tanto, adavosertib (ADA), un inhibidor de WEE1, tiene un efecto letal sintético significativo en los cánceres con mutación p53. Sin embargo, la resistencia a los medicamentos debido a las vías de compensación de la respuesta al daño del ADN (DDR) y la alta toxicidad limitan futuras aplicaciones.
Estudios recientes han indicado que el uso de factores físicos como la terapia fotodinámica (PDT), la terapia sonodinámica (SDT) y la gasoterapia en el tratamiento de tumores tiene efectos superiores y una gama más amplia de aplicaciones que los fármacos químicos convencionales. Los factores físicos que proporcionan condiciones irreversibles para mejorar el efecto letal sintético de la destrucción de tumores demostrarán ser una estrategia eficaz.
Por lo tanto, basándose en la capacidad de la estructura MOF para realizar varias condiciones adicionales mientras se administran medicamentos, este nuevo estudio seleccionó MOF como una herramienta junto con SDT para mejorar el efecto letal sintético entre WEE1 y p53 en GBC y obtuvo un resultado prometedor. P>
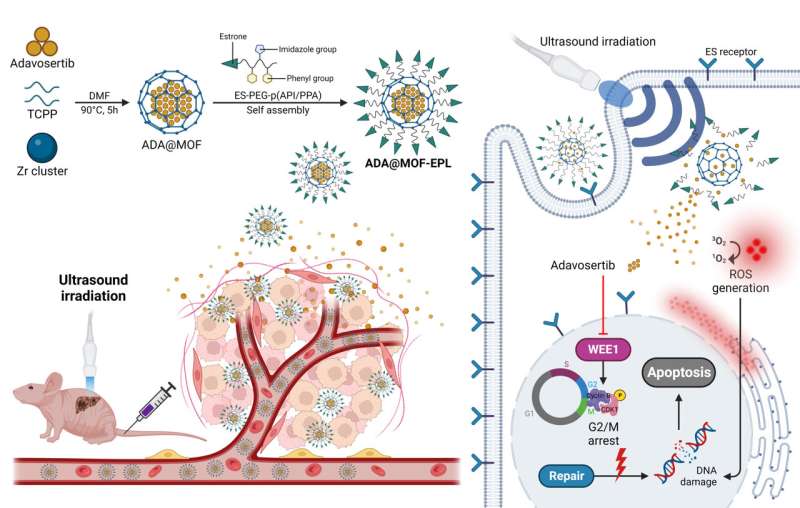
Específicamente, se usó una porfirina sonosensible (tetrakis (4-carboxifenil) porfirina, TCPP) que contiene Zr-MOF como columna vertebral orgánica para la terapia sonodinámica (SDT), seguida de la encapsulación de ADA durante la síntesis de MOF en un solo recipiente para aumentar la carga de ADA. de MOF (ADA@MOF). Además, la superficie de ADA@MOF se recubrió con ligandos poliméricos dirigidos a estrona (EPL) sensibles al pH para proporcionar a las nanopartículas una capacidad de dirección de tumores (ADA@MOF-EPL).
Debido a la alta expresión del receptor de estrógeno (RE) en GBC, la estrona funciona como un ligando dirigido a tumores, lo que permite que las nanopartículas ingresen y se acumulen cerca del núcleo celular de manera rápida y precisa. Al entrar en el microambiente ácido del tumor (TME), las interacciones iónicas debilitadas entre ADA@MOF y EPL aflojarán su estructura, lo que provocará la liberación inicial de ADA.
Posteriormente, la irradiación con ultrasonido (EE. UU.) para estimular el MOF sonosensible que contiene porfirina dará como resultado la liberación acelerada de ADA y generará ROS para dañar el ADN. Esto provocará una mayor sensibilidad de las células cancerosas con mutación p53 a ADA y evitará la resistencia a los medicamentos debido a las vías de compensación DDR en la fuente.
Por lo tanto, el efecto letal sintético mejorado entre ADA y p53 a través de una condición adicional de SDT tendría una sólida capacidad para matar tumores. Además, las nanopartículas también reducen en gran medida la reacción tóxica del fármaco. Lo más importante es que este nuevo estudio ofrece una perspectiva novedosa sobre el uso de sistemas de administración de fármacos basados en MOF en el tratamiento de diversos cánceres refractarios mediante SL mejorado.
Más información: Shijie Li et al, Marcos orgánicos metálicos encapsulados con adavosertib para el tratamiento del cáncer de vesícula biliar con mutación p53 mediante letalidad sintética, Science Bulletin (2024). DOI:10.1016/j.scib.2024.02.039
Proporcionado por Science China Press