El glicerol, un importante subproducto del refinado de biomasa que representa aproximadamente el 10% del rendimiento, presenta un desafío importante debido a su excedente global. La presencia de múltiples grupos hidroxilo activos en el glicerol revela un gran potencial para la producción de sustancias químicas de alto valor. El ácido fórmico (AG), un producto clave de la conversión de glicerol, es una materia prima química orgánica crítica con gran demanda en sectores como el de pesticidas, productos farmacéuticos y energía.
La oxidación del glicerol a FA no sólo mitiga el desperdicio causado por el excedente de recursos, sino que también satisface las necesidades futuras de las pilas de combustible de FA. Actualmente, la producción industrial de AG depende principalmente del metanol derivado del petróleo y del gas natural, lo que hace que la conversión electrocatalítica de glicerol a base de biomasa en AG sea muy prometedora.
Sin embargo, la reacción de oxidación electrocatalítica del glicerol (RGOR) es compleja e implica deshidrogenación, adsorción/desorción y ruptura de enlaces C-C de los intermedios de la reacción, lo que plantea desafíos a la eficiencia y selectividad de la reacción.
Recientemente, un equipo de investigación dirigido por el Prof. Kai Yan de la Universidad Sun Yat-sen, China, utilizando una combinación de cálculos de la teoría funcional de la densidad (DFT) y métodos experimentales, ha revelado el papel crucial de la especie activa OH* en el proceso EGOR. en la producción de AF. El análisis DFT, partiendo de una perspectiva termodinámica, investigó el mecanismo del OH* en el proceso EGOR.
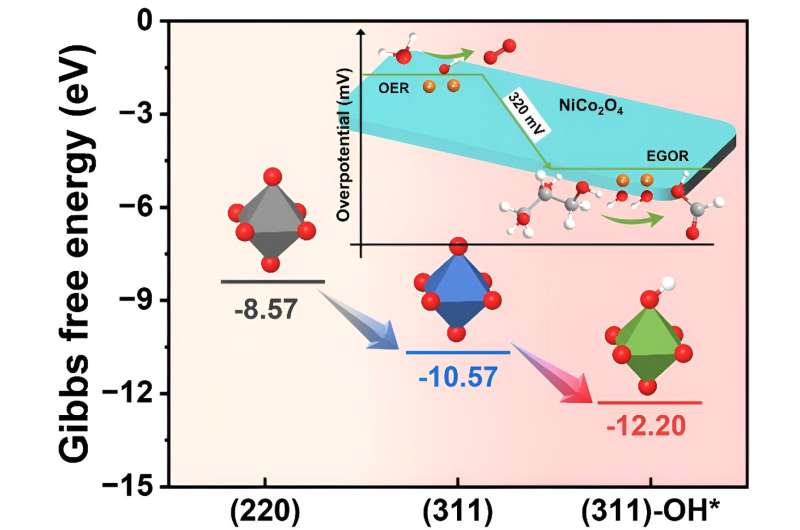
Se encontró que las especies OH* superficiales, al reducir la energía de adsorción del glicerol en el NiCo2 O4 superficie del catalizador (de -12,20 a -10,57 eV), facilitó el proceso EGOR y optimizó el paso determinante de la velocidad (RDS) al alterar la energía de adsorción de los intermedios, pasando de la deshidrogenación menos eficiente del ácido glicérico al paso de deshidrogenación más eficiente de gliceraldehído.
Además, la energía de adsorción de OH* durante el proceso EGOR fue significativamente menor en comparación con el proceso de reacción de evolución de oxígeno (REA) (0,66 frente a 2,70 eV), lo que indica la aparición preferencial de EGOR sobre REA.
Además, el rendimiento de un NiCo2 meticulosamente diseñado O4 El electrodo en EGOR se investigó mediante métodos electroquímicos. En un electrolito mixto de 1 mol L -1 KOH y 0,1 mol L -1 glicerol, el potencial de inicio del electrodo cayó a 1,16 VRHE , superando significativamente a los REA. Los experimentos con electrodo de disco de anillo giratorio (RRDE) también confirmaron la aparición preferencial de EGOR, lo que coincide con los hallazgos del análisis DFT.
Basado en el mecanismo convencional de transferencia de electrones acoplados a protones, se han investigado dos posibles vías de oxidación electroquímica (vía de oxidación directa y vía de oxidación indirecta) de OH* mediante el uso de métodos de potenciación de múltiples pasos y resonancia electrónica simultánea. Los resultados experimentales demostraron que el rendimiento excepcional del NiCo2 O4 El electrodo en EGOR está estrechamente relacionado con la generación in situ de OH* que participa directamente en la reacción.
En una prueba de estabilidad de ciclo a largo plazo de 120 h, el catalizador también mostró una tasa de conversión de glicerol eficiente y estable (89%) y una selectividad al ácido fórmico (70%). Este trabajo proporciona orientación e información valiosas para el diseño y desarrollo de catalizadores eficientes y estables para la oxidación de glicerol. Los resultados fueron publicados en el Chinese Journal of Catalysis. .
Más información: Yan Duan et al, Integración de la predicción teórica y la electrooxidación experimental de glicerol en NiCo2 O4 nanohojas, Revista China de Catálisis (2024). DOI:10.1016/S1872-2067(23)64585-1
Proporcionado por la Academia China de Ciencias