Varios tipos de terapias convencionales contra el cáncer, como la radioterapia o la quimioterapia, destruyen las células sanas junto con las cancerosas. En etapas avanzadas del cáncer, la pérdida de tejido debido a los tratamientos puede ser sustancial e incluso fatal. Las terapias contra el cáncer de vanguardia que emplean nanopartículas pueden atacar específicamente las células cancerosas, preservando el tejido sano.
Estudios recientes han demostrado que las nanopartículas de origen vegetal (pdNP) que tienen efectos terapéuticos pueden ser una alternativa eficaz a los tratamientos tradicionales contra el cáncer. Sin embargo, hasta la fecha no se ha aprobado ningún pdNP como agente terapéutico contra el cáncer.
El salvado de arroz es un subproducto generado durante el proceso de refinación del arroz que tiene una utilidad limitada y un valor comercial bajo. Sin embargo, contiene varios compuestos con propiedades anticancerígenas, como γ-orizanol y γ-tocotrienol.
Para explorar estas propiedades terapéuticas del salvado de arroz, un equipo de investigadores dirigido por el profesor Makiya Nishikawa de la Universidad de Ciencias de Tokio (TUS) en Japón desarrolló nanopartículas de salvado de arroz y probó su eficacia en modelos de ratones. Su estudio, publicado en el Journal of Nanobiotechnology el 16 de marzo de 2024, fue coautor del Dr. Daisuke Sasaki, la Sra. Hinako Suzuki, el profesor asociado Kosuke Kusamori y el profesor asistente Shoko Itakura de TUS.
"En los últimos años, se está desarrollando un número cada vez mayor de nuevas modalidades de medicamentos. Al mismo tiempo, los costos de desarrollo asociados con nuevas terapias han aumentado dramáticamente, contribuyendo a la carga de los gastos médicos. Para abordar este problema, utilizamos salvado de arroz, un residuos industriales con propiedades anticancerígenas, para desarrollar nanopartículas", explica el profesor Nishikawa.
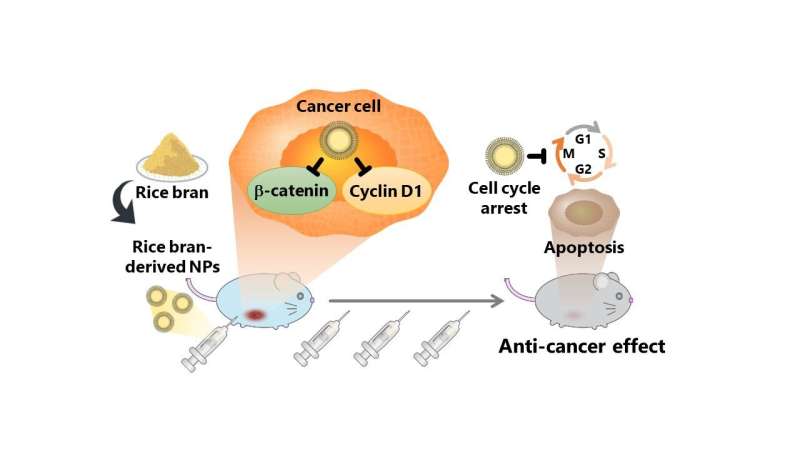
El estudio evaluó los efectos anticancerígenos de las nanopartículas derivadas del salvado de arroz (rbNP), que se obtuvieron procesando y purificando una suspensión de salvado de arroz Koshihikari en agua. Cuando una línea celular cancerosa llamada colon26 fue tratada con rbNP, se detuvo la división celular y se indujo la muerte celular programada, lo que indica fuertes efectos anticancerígenos de las nanopartículas. La actividad anticancerígena observada de las rbNP se puede atribuir al γ-tocotrienol y al γ-orizanol, que son absorbidos fácilmente por las células cancerosas, lo que provoca la detención del ciclo celular y la muerte celular programada.
Además, las rbNP redujeron la expresión de proteínas, como la β-catenina (una proteína asociada con la vía de señalización Wnt implicada en la proliferación celular) y la ciclina D1, que se sabe que promueven la recurrencia del cáncer y las metástasis. Además, las rbNP redujeron la expresión de β-catenina solo en las células del colon26 sin afectar a las células no cancerosas.
"Una preocupación clave en el contexto de las pdNP es su baja actividad farmacológica en comparación con los fármacos. Sin embargo, las rbNP mostraron una mayor actividad anticancerígena que DOXIL, una formulación farmacéutica liposomal de doxorrubicina. Además, la doxorrubicina es citotóxica tanto para las células cancerosas como para las no cancerosas. , mientras que las rbNP son específicamente citotóxicas para las células cancerosas, lo que sugiere que son más seguras que la doxorrubicina", afirma el profesor Nishikawa.
Para confirmar las propiedades anticancerígenas de las rbNP en el cuerpo vivo, los investigadores inyectaron rbNP en ratones que tenían un adenocarcinoma agresivo en su cavidad peritoneal (encerrada por el diafragma, los músculos abdominales y la pelvis y alberga órganos como los intestinos, el hígado y los riñones). Observaron una supresión significativa del crecimiento tumoral sin efectos adversos en los ratones. Además, las rbNP inhibieron significativamente el crecimiento metastásico de células de melanoma murino B16-BL6 en un modelo de ratón con metástasis pulmonar.
El salvado de arroz tiene varios atributos que lo convierten en una excelente fuente de pdNP terapéuticos. En primer lugar, es económico en comparación con muchas otras fuentes de pdNP. Casi el 40% del salvado de arroz se desecha en Japón, lo que proporciona una fuente de materia prima fácilmente disponible. En segundo lugar, la eficiencia de preparación de los rbNP es mayor que la de los pdNP informados anteriormente.
Además de ser práctico y seguro como terapéutico contra el cáncer, las propiedades fisicoquímicas de las rbNP son muy estables. Sin embargo, antes de los ensayos clínicos en humanos se deben investigar algunos parámetros, como el establecimiento de tecnologías de separación a nivel farmacéutico, la evaluación de los parámetros de control del proceso de producción y la evaluación de la eficacia y seguridad en líneas celulares de cáncer humano y modelos animales de xenoinjerto. /P>
En conclusión, el salvado de arroz, un producto de desecho agrícola, es una fuente de pdNP terapéuticos que son asequibles, eficaces y seguros, y tiene el potencial de revolucionar el tratamiento del cáncer en el futuro.
"Al establecer un método de fabricación de nanopartículas de salvado de arroz con calidad estable y confirmar su seguridad y eficacia, podemos desarrollar medicamentos para el tratamiento del cáncer que sean sostenibles, ecológicos y asequibles. En consecuencia, podremos ayudar a más pacientes con cáncer a mantener buena salud física y mental después del tratamiento", concluye el profesor Nishikawa.
Más información: Daisuke Sasaki et al, Desarrollo de nanopartículas derivadas de salvado de arroz con excelente actividad anticancerígena y su aplicación para la diseminación peritoneal, Journal of Nanobiotechnology (2024). DOI:10.1186/s12951-024-02381-z
Proporcionado por la Universidad de Ciencias de Tokio