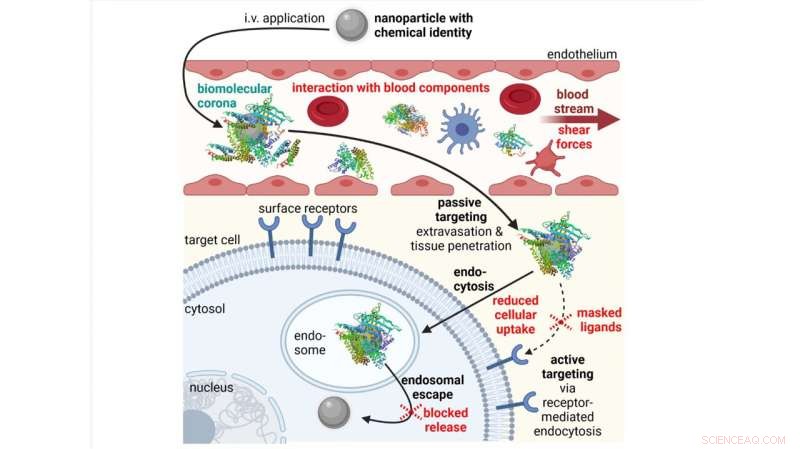
Obstáculos (en rojo) en el proceso de administración in vivo de nanopartículas aplicadas por vía intravenosa (IV). Crédito:Simone Berger, Martin Berger, Christoph Bantz, Michael Maskos y Ernst Wagner
Las vacunas de ARN mensajero (ARNm) son un excelente ejemplo del prometedor campo de la nanomedicina. Pero, lamentablemente, el progreso en el diseño y la aplicación de nanopartículas como vehículos de administración eficientes para productos biofarmacéuticos que contienen ácidos nucleicos o proteínas es notablemente lento.
Un obstáculo reciente para la investigación de administración de fármacos es una débil correlación observada entre in vitro (fuera de un organismo vivo) e in vivo (dentro de un organismo vivo) rendimiento. Este problema no estaba claro en las primeras etapas, cuando la entrega celular de un nanoportador de fármacos se probó principalmente dentro de un cultivo celular estándar. Con los estudios farmacológicos in vivo avanzados que surgen en ratones o pacientes humanos, la baja confiabilidad y validez de las pruebas de cultivo celular para aplicaciones terapéuticas se está volviendo evidente.
Cuando las nanopartículas se aplican por vía intravenosa, enfrentan varios obstáculos que difieren de las situaciones in vitro, como cuando se encuentran con componentes sanguíneos. Las nanopartículas suelen estar cubiertas por una multicapa biomolecular (una corona de proteínas), que altera las propiedades fisicoquímicas, la farmacocinética y el perfil de toxicidad de las nanopartículas.
En Reseñas de Biofísica , investigadores en Alemania proporcionan una caracterización de vanguardia de la corona de proteínas formada alrededor de las nanopartículas y su impacto en las propiedades fisicoquímicas y biológicas de estas nanopartículas.
"Al predecir el rendimiento in vivo a partir de datos in vitro, se recomienda combinar varios métodos de caracterización analíticos y biológicos para obtener una visión más detallada de las características y el comportamiento in vivo de las nanopartículas", dijo Simone Berger, coautora de Ludwig Maximilian. Universidad de Múnich.
La elección del biofluido (suero, plasma o sangre completa y de origen animal) y el establecimiento de protocolos estandarizados son de gran importancia para obtener resultados preclínicos más consistentes, sólidos y completos. estudios para derivar relaciones estructura-actividad e in vitro/in vivo correlaciones.
"El conocimiento adquirido sobre la formación de la corona de proteínas se puede explotar para optimizar los portadores para aplicaciones nanomédicas", dijo Berger.
La información como la biodistribución in vivo y los efectos fuera del objetivo no se pueden obtener de los experimentos in vitro, señalan los investigadores. Pero los nuevos métodos de detección de alto rendimiento, como el sistema de código de barras, pueden hacer in vivo investigaciones más efectivas, económicas y éticas.
Sigue existiendo cierta incertidumbre sobre la traducibilidad de animales pequeños a grandes y humanos, pero la bioinformática podría ayudar a identificar los modelos animales que mejor se adaptan a ciertas enfermedades.
"Las alternativas a los modelos animales, como la tecnología microfluídica de 'órgano humano en un chip' o las predicciones computacionales, pueden ser estrategias prometedoras para reemplazar los estudios con animales en el futuro", dijo Berger.
La nanomedicina muestra "un gran potencial para revolucionar el panorama terapéutico con una amplia gama de aplicaciones como vacunas contra el cáncer/inmunoterapia o tratamiento de trastornos genéticos", dijo Berger. "Con ensayos in vitro adecuados y más predictivos, la tubería preclínica será más eficiente, más rápida y económica. Y lo que es más importante, los experimentos con animales pueden reemplazarse o al menos reducirse". Un método para mejorar las pruebas in vitro